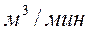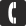Масса углекислого газа. Масса углекислого газа
Удельный вес углекислого газа. Вес 1 литра углекислого газа и его плотность

Углекислота, или углекислый газ, при естественных условиях находится в газообразном состоянии, не имеет запаха и цвета, на вкус кислая. Содержание диоксида СО2 (диоксида углерода) в атмосфере Земли составляет 0,03–0,04%, то есть от 0,3 до 0,4 мл на 1 литр воздуха и в жидкой форме при нормальном атмосферном давлении его не существует, переходит сразу из твердого состояния в газообразное. Он тяжелее воздуха в полтора раза. В естественных условиях плотность или удельный вес углекислого газа составляет 1,977 кг/м3.
Таблица перерасчета удельного веса углекислого газа (плотности) в метрической системе| т/м3 | кг/м3 | г/м3 | мл/м3 | кг/л | г/л | мл/л | г/дм3 | г/мл | мг/мл |
| 0.001977 | 1.977 | 1 977 | 1 977 000 | 0.001977 | 1.977 | 1 977 | 1.977 | 0.001977 | 1.977 |
Углекислый газ – важнейший компонент жизни человека
Источниками углекислоты, которой в доисторические времена в атмосфере нашей планеты содержалось более 80%, являются гнилостные процессы, вулканические выделения, процессы горения и окисления. Выделяют углекислый газ люди и животные в процессе дыхания. Многие не знают, но в ночное время растения тоже выделяют углекислоту в атмосферу.
СО2 выполняет основополагающую роль в жизни всей планеты и всех ее живых существ. Основным «заданием» можно считать поддержание процесса фотосинтеза, также он принимает участие во множестве метаболических процессов каждой живой клетки. Он не токсичен и не поддерживает дыхания, хотя играет важнейшую роль в самом его процессе.
Интересно, что в крови плода количество кислорода в 4 раза меньше, чем у взрослого человека, а углекислоты в 2 раза больше. При увеличении процентного соотношения кислорода, эмбрион погибает.
СО2 – один из необходимых факторов в поддержании кислотно-щелочного баланса крови, регулирует активность ферментов в организме. Для нормальной жизнедеятельности человеческого организма, количество углекислоты в крови должно быть на уровне 7–7,5 %, снижение этого уровня до 4 % грозит гибелью организма. Его нехватка включает защитную систему, начинаются спазмы сосудов и гладкой мускулатуры, увеличивается количество слизи в дыхательных путях, образуется больше холестерина, вследствие чего уплотняются клеточные мембраны, препятствуя транспортировке веществ. Все это приводит к глубокому кислородному голоданию (согласно эффекту Бора).
Итак, согласно результатам научных исследований, СО2 незаменим при:
- дыхании,
- метаболизме,
- регуляции внутренних гормональных процессов,
- возбуждении дыхательного центра,
- успокоении нервной системы,
- расширении сосудов.
СО2 необходим животным
Круговорот веществ в природе обеспечивает относительно стабильный уровень углекислоты в атмосфере. При содержании животных крайне важным является поддержания естественного уровня СО2 в помещении. Соответствующая чистота, вентиляция и правильное размещение животных решают проблему перенасыщения углекислого газа. Напомним, что его нормальное содержание – 0,3-0,4 мл на 1 литр воздуха. При несоблюдении условий содержания животных количество углекислоты может увеличиться до 1% и более.
Например, лошадь выделяет около 130 л СО2 в час, корова – до 200 л, овцы – до 30 л, свиньи – до 90 л. Если в закрытом помещении концентрация углекислого газа превысит 0,5%, это будет негативно сказываться на жизнедеятельности организма, наступает отравление, снижается продуктивность и иммунитет, проявляется вялость, апатия, потеря аппетита, животные худеют.
Углекислота жизненно необходима для всех живых организмов нашей планеты. Если его не станет, все живое погибнет, но если его будет очень много, результат окажется тот же.
naruservice.com
Масса углекислого газа
 Ф: Какова масса 500 моль углекислого газа?Ф: Какова масса 500 моль углекислого газа? Рымкевич 455.
Ф: Какова масса 500 моль углекислого газа?Ф: Какова масса 500 моль углекислого газа? Рымкевич 455.
 №35 Углекислый газ для растений Как обеспечить растение углекислым газомOur Commrades over at Groshop DzagiGrow in Russia explain how to bring CO2 to your plants. Carbon dioxide for plants is the second fertilizer. The plant ...
№35 Углекислый газ для растений Как обеспечить растение углекислым газомOur Commrades over at Groshop DzagiGrow in Russia explain how to bring CO2 to your plants. Carbon dioxide for plants is the second fertilizer. The plant ... Свойства углекислого газаhttp://paramitacenter.ru / Центр довузовской подготовки ПАРАМИТА.
Свойства углекислого газаhttp://paramitacenter.ru / Центр довузовской подготовки ПАРАМИТА.
 Моль. Молярная масса. Задачи по химии. Часть 2.Решаем 3-ю задачу на определение количества вещества (моль). Задачи по химии. Часть Б. Ссылки на дополнительн...
Моль. Молярная масса. Задачи по химии. Часть 2.Решаем 3-ю задачу на определение количества вещества (моль). Задачи по химии. Часть Б. Ссылки на дополнительн... Полезная хитрость для механизма подачи проволоки сварочного полуавтоматаКак продлить срок службы механизма подачи проволоки сварочного полуавтомата.
Полезная хитрость для механизма подачи проволоки сварочного полуавтоматаКак продлить срок службы механизма подачи проволоки сварочного полуавтомата. Галилео. Эксперимент. Опыт с углекислым газом592 от 24.06.2010 Эксперимент, демонстрирующий производство углекислоты. Невозможность горения в углекислом...
Галилео. Эксперимент. Опыт с углекислым газом592 от 24.06.2010 Эксперимент, демонстрирующий производство углекислоты. Невозможность горения в углекислом...
 Объём Моль газа. Рыбников Ю.СГруппа Вконтакте https://vk.com/club143089217 Однокласники https://ok.ru/group/55030175105038 Помощь каналу Сбербанк ViSA 4276 8380 8836 5087...
Объём Моль газа. Рыбников Ю.СГруппа Вконтакте https://vk.com/club143089217 Однокласники https://ok.ru/group/55030175105038 Помощь каналу Сбербанк ViSA 4276 8380 8836 5087... Гашение свечей углекислым газомВ аппарате Киппа углекислый газ получают реакцией между карбонатом кальция и раствором соляной кислоты....
Гашение свечей углекислым газомВ аппарате Киппа углекислый газ получают реакцией между карбонатом кальция и раствором соляной кислоты.... ХИМИЯ.Бинарные соединения. Оксиды,гидриды, вода и углекислый газ.
ХИМИЯ.Бинарные соединения. Оксиды,гидриды, вода и углекислый газ.
 Портативный автономный монитор углекислого газа (СО2) введениеУважаемые ! Очень нужна ваша помощь в разработке и изготовлении корпуса. Назначение прибора предъявляет...
Портативный автономный монитор углекислого газа (СО2) введениеУважаемые ! Очень нужна ваша помощь в разработке и изготовлении корпуса. Назначение прибора предъявляет...avtoclubvideo.ru
Молекулярный вес, определение углекислого газа
РАБОТА 2. ОПРЕДЕЛЕНИЕ МОЛЕКУЛЯРНОЙ МАССЫ УГЛЕКИСЛОГО ГАЗА [c.38]
Зная вес углекислого газа в определенном объеме при нормальных условиях, можно найти его плотность по водороду или воздуху и подсчитать его молекулярный вес. [c.63]
ОПРЕДЕЛЕНИЕ МОЛЕКУЛЯРНОГО ВЕСА УГЛЕКИСЛОГО ГАЗА [c.35]
Определение молекулярного веса углекислого газа. [c.69]
Для определения молекулярного веса углекислого газа им наполняют плоскодонную колбу с узким горлом емкостью 250 мл. Колбу предварительно моют, высушивают и подбирают пробку, плотно входящую в нее. Колбу с пробкой взвешивают на технохимических весах (с точностью до 0,01 г). Затем в колбу до дна вставляют газоотводную трубку и заполняют колбу углекислым газом из аппарата Киппа или из баллона. Для очистки и высушивания газа его пропускают последовательно через склянки с водой и серной кислотой. Колбу закрывают пробкой, взвешивают, снова пропускают в нее углекислый газ и еще раз взвешивают. По достижении постоянного веса (расхождение не более чем на 0,01 г) записывают этот вес и определяют объем колбы, заполнив ее водой и измерив затем объем воды мерным цилиндром. Отмечают температуру и давление воздуха и вычисляют мо- [c.70]
Для определения молекулярного веса углекислого газа собрать прибор по рис. 50. [c.63]
Для определения молекулярного веса углекислого газа взять сухую плоскодонную колбу емкостью 500 мл с хорошо пригнанной резиновой пробкой. При помоши резинового кольца или карандаша по стеклу сделать отметку на горлышке колбы в том месте, где кончается пробка. Взвесить с точностью до 0,01 г колбу с пробкой. При заполнении колбы углекислым газом газоотводную трубку аппарата Киппа или баллона с углекислым газом опустить до дна колбы. Когда колба заполнится углекислым газом (как это определить ), медленно вынуть газоотводную трубку, закрыть отверстие колбы пробкой и взвесить. Заполнение колбы углекислым газом производить несколько раз, до тех пор пока не будет получен постоянный вес. Определить объем колбы, наполнив ее водой до метки. Отметить температуру и давление. Вычислить молекулярный вес углекислого газа. [c.36]
Определение молекулярного веса углекислого газа Получение карбонатов и бикарбонатов и их взаимные [c.228]
Определение молекулярного веса хлора. Сущность метода та же, что и при определении молекулярного веса углекислого газа. Некоторое отличие заключается в том, что хлор собирают не в колбе, а в газовой пипетке. Газовая пипетка (рис. 17) представляет собой стеклянный баллон объемом 150—200 мл, снабженный двумя кранами для впуска и выпуска газа. К пипетке прикрепляется проволока с петлей на конце, которая позволяет подвешивать пипетку к крючку серьги весов при взвешивании. [c.33]
Определение молекулярного веса углекислого газа................34 [c.3]
ИЗ крови выделяются газы, которые проходят через осушительную трубку и вносятся в колонку потоком газа-носителя. Такая система позволяет за 5—6 мин разделить и определить кислород, азот и углекислый газ. Для разделения газов используют две последовательно включенные колонки, одна из которых заполнена силикагелем 950 (28/200 мейл), а другая — молекулярным ситом 13-Х (см. раздел Б, II, в, 2). Воспроизводимость метода более 1%, а результаты, полученные при определении углекислого газа и кислорода, совпадают с результатами, полученными по методу Ван-Слайка, с точностью 1% (по Объему). Когда мы писали настоящую книгу, еще не был известен состав гемолизирующего агента, и поэтому методика извлечения газов не включена в экспериментальную часть данной главы. [c.144]
Определение молекулярного веса углекислого газа. На техно-химических весах взвесить сухую колбу с воздухом, заключенным в ней, и с пробкой (вес вг). Пробка должна быть вдвинута в горло колбы до метки (резиновое кольцо). Опустить в колбу стеклянную трубочку, подводящую углекислый газ из аппарата Киппа через промывные склянки (с раствором соды и с концентрированной серной кислотой). Открыть кран аппарата Киппа и медленно пропускать углекислый газ в течение 7—8 мин. Закрыть колбу пробкой до метки и взвесить (вг). Вновь пропускать углекислый газ 3—4 мин., а затем взвесить (вз). Если два последних веса равны или отличаются друг от друга не более чем на 0,01 г, то наполнение колбы следует считать законченным. В противном случае повторить наполнение и добиться постоянного веса колбы. Отметить температуру по комнатному термометру и давление — по барометру. [c.27]
Знания газовых законов учащихся молопределения молекулярного веса некоторых газов. Удобнее взять углекислый газ или кислород. Работу можно организовать так. [c.55]
Опыт. Определение молекулярного веса углекислого газа. Определение молекулярного веса углекислого газа производится в том же приборе, что и определение химического эквивалента металлов. [c.42]
Определение молекулярного веса углекислого газа. На техно-химических весах взвесить сухую колбу с воздухом, закрытую пробкой (вес 65). Пробка должна быть вдвинута в горло колбы до метки (резиновое кольцо). Опустить в колбу стеклянную трубочку, подводящую углекислый газ из аппарата Киппа (см. рис. 19). Для промывки и осушки газ пропускают через промывные [c.30]
Количественное определение азота. Для определения количества азота органическое вещество окисляют в атмосфере углекислого газа над раскаленной окисью меди. Содержащийся в веществе азот выделяется в виде молекулярного, газообразного азота. Его собирают в специальном приборе — азотометре, позволяющем непосредственно отсчитывать объем газа. [c.9]
В качестве газов-носителей могут применяться водород, азот и углекислый газ. Найдено, что средняя ошибка при определениях молекулярного веса составляет около 4%. [c.270]
Линия № 2 служит для определения в реакционной смеси кислорода и углекислого газа. Газ-носитель (водород) после очистки разделяется на три потока. Первый поток проходит через сравнительную ячейку катарометра 9, пробоотборник 66, предварительную колонку с углем СКТ, 4-ходовой кран 76, основную колонку с углем СКТ, 4-ходовой кран 7в, предварительную Г и основную Д колонки с молекулярными ситами 6А, 4-ходовой кран 7г, рабочую ячейку катарометра 9 и реометр 12. Второй поток после регулятора скорости проходит через 4-ходовой кран 76. Третий поток проходит через 4-ходовые краны 7в и 7г. [c.475]
Выбор истинного числа делался на основании закона Авогадро. Так как в молекуле любого углеродного соединения не может содержаться меньше одного атома углерода, наименьшая доля этого элемента в молекулярном весе и должна соответствовать его атомному весу. Нужно было, следовательно, определить молекулярные веса различных летучих углеродных соединений, вычислить по их процентному составу в каждом случае долю углерода и выбрать из всех полученных чисел наименьшее. Такие определения давали число 12. Поэтому атомный вес углерода и следовало принять равным двенадцати. В качестве примера приведены расчетные данные для метана, эфира, спирта и углекислого газа [c.21]
Для определения количественного состава органических соединений пользуются особыми методами анализа, например сжигают вещество в специальном приборе и по массе выделившегося углекислого газа вычисляют содержание углевода, а по массе воды — содержание водорода в сожженном веществе. Затем по количественному составу и молекулярному весу определяют молекулярную формулу органического соединения Некоторые органические соединения содержат кислород, азот, серу, галогены и др. [c.286]
При определенных термодинамических условиях углекислый газ может смешиваться с нефтью и вообще с углеводородными жидкостями в неограниченных пропорциях. При полном смешивании обеспечивается. максимальный коэффициент нефтеотдачи. Экспериментальные исследования показывают, что величина давления смешивания, т. е. давления, при превышении которого происходит полное взаимное растворение нефти и СО2, зависит от типа нефти. Обобщенной характеристикой нефти при этом служит ее молекулярная масса. Условия смешиваемости нефти с углекислотой определяются по графику зависимости давления с>1ешивания от температуры и молекулярной массы (рис. 94). Значения давления смешивания составляют для условий Ромашкинского месторождения (молекулярная масса 238, пластовая температура 40 °С) [c.159]
Однако, как свидетельствует Зимаков [212], перекисных группировок на поверхности серебряных катализаторов образуется меньше, чем окисных. Последние более прочны, и на них этилен окисляется при более высоких температурах до СО2 и Н2О. Соотношением вероятностей числа соударений этилена с перекис-ныщ и окисными группировками и определяется в основном выход окиси этилена. Таким 0бра130м, реакция окисления этилена молекулярным кислородом на серебре в принципе может быть избирательной лишь до определенных пределов. В случае простой газовой смеси этилен + кислород, которая пропускается над чистым серебром, выход окиси этилена является минимальным и во всяком случае не превышает 50%. Это, так сказать, нижний предел избирательности. Последняя может быть повышена уменьшением числа соударений этилена с окисными группировками, т. е. путем блокировки окисных группировок на катализаторе различными примесями, отравляющими вредные участки поверхности. Такими примесями являются, в частности, хлористый водород и углекислый газ. Но они блокируют окисные участки лишь в узких температурных интервалах, поэтому работа с ними требует особой четкости. Кроме того, отравленные таким способом катализаторы быстро теряют свою искусственно повышенную избирательность. [c.348]
Аргоновый детектор Ловелокка проявляет одинаковую чувствительность ко всем веществам с молекулярным весом выше 100, поскольку чувствительность и линейность его реакции являются, главным образом, функциями напряжения на электродах. С газом-носителем аргоном этот детектор нечувствителен к тем веществам, потенциал ионизации которых выше 11,6 эв. Так, СН4, О2, N2, СО и вода почти не поддаются определению, за исключением того случая, когда кислородсодержащие молекулы дают отрицательный сигнал, соответствующий понижению фонового тока за счет захвата электронов. Нечувствительность детекторов ионизационного типа к воздуху и углекислому газу с успехом используется при анализе запахов, загрязнений воздуха и т. д. без применения обычных практически нежелательных операций концентрирования. [c.327]
Нельзя считать безнадежными и попытки использования атомной абсорбции для анализа газов по резонансным линиям, лежашим в вакуумной области спектра. В литературе описаны аналитические методики для определения концентрации водяного пара в воздухе [3], а также в азоте, кислороде и углекислом газе [3] по поглош,ению линии водорода Ь 1216 А) молекулярной полосой НгО с максимумом около 1220 А. Поэтому имеются все необходимые предпосылки для разработки [c.337]
В вышеприведенных примерах соединений с водою мы видели постепенное усиление связи между водою и телом, с которым она образует однородное вещество. Есть затем разряд таких соединений с водою, в которых вода удерживается с весьма большою силою, выделяется только разве при очень большом жаре, а иногда и вовсе не выделяется ни при каком жаре, без полного разложения состава. В таких веществах обыкновенно вовсе незаметно никаких признаков содержания воды. Из безводного вещества и воды обр 1зуется совершенно новое вещество, в котором иногда вовсе незаметно некоторых начальных свойств составных начал. В большинстве случаев, при таком соединении с водою, отделяется значительное количество тепла. Иногда это отделение столь велико, что при соединении происходит накаливание, выделяется свет. Немудрено, вследствие этого, что при таком соединении образуются прочные тела. Для разрушения их нужно прибавить много теплоты, нужно произвести большую работу, чтобы разъединить те части, из которых они образовались. Все такие соединения суть определенные и, обыкновенно, совершенно резко определенные. Такие определенные соединения с водою называются гидратами. Вода, в них находящаяся, носит нередко название конституциоивой воды, т.-е. воды, вошедшей в строение или состав взятого вещества. Этим хотят выразить, что в других случаях частицы воды как бы находятся отделенными от частиц того тела, с которым вода соединена (молекулярные соединения), напр., в кристаллогидратах. Можно привести многие примеры образования определенных и прочных гидратов. Наиболее известным в практике примером таких гидратов может служить гидрат извести, или так называемая гашеная известь. Известь получается чрез выжигание известкового камня, причем из него выделяется углекислый газ и остается белая каменистая масса, плотная и сплошная, довольно вязкая. В этом виде известь обыкновенно продается и носит название кипелки или негашеной извести. Если такую известь облить водою, то тотчас, или спустя некоторое время, замечается весьма большое повышен)1е температуры. Вся масса разгорячается, избыточная часть воды испаряется, каменистая масса, поглощая воду, рассыпается в порошок и, если воды взято достаточное количество, а известь [c.83]
chem21.info
масса углекислого газа Видео

2 г. назад
Ф: Какова масса 500 моль углекислого газа? Рымкевич 455.

3 г. назад
Углекислый газ для растений это второе удобрение. Растение растет благодаря фотосинтезу. Для него нужны...

6 мес. назад
Our Commrades over at Groshop DzagiGrow in Russia explain how to bring CO2 to your plants. Carbon dioxide for plants is the second fertilizer. The plant ...

3 г. назад
Урок физики в Ришельевском лицее.

8 г. назад
http://paramitacenter.ru / Центр довузовской подготовки ПАРАМИТА.

4 г. назад
Решаем 3-ю задачу на определение количества вещества (моль). Задачи по химии. Часть Б. Ссылки на дополнительн...

4 г. назад
592 от 24.06.2010 Эксперимент, демонстрирующий производство углекислоты. Невозможность горения в углекислом...

2 г. назад
Как продлить срок службы механизма подачи проволоки сварочного полуавтомата.

3 г. назад
Предприниматель (в машиностроительной отрасли) Бацуца Владимир Иванович рассказывает о своем опыте исполь...
2 г. назад
Задача: Определить объем, который занимает кислород массой 64 г (н.у.). Алгоритм решения задачи на определение...

2 г. назад
Ф: Сравните массы и объемы двух тел, сделанных соответственно из олова и свинца, если в них содержится равно...

4 г. назад
NaHCO3+h3SO4 35%=углекислый газ.

3 мес. назад
Уважаемые ! Очень нужна ваша помощь в разработке и изготовлении корпуса. Назначение прибора предъявляет...

3 г. назад
Настройка под свои величины расхода регулятора У-30/А-40 фирмы ПТК. Давление на цифровом манометре отображает...

6 г. назад
Самодельный генератор углекислого газа СО2 CO2 смесь сода сахар крахмал - получаем кисель - добавляем дрожжи....

2 г. назад
СПАСИБО ЗА ПОДПИСКУ! Приобрести курс тренировок на силу и массу "Переформатирование" https://bbright.club/?page_id=796...
3 г. назад
В видео предлагается решение задачи: Газовая смесь объемом 12,32 л состоит из водорода, сероводорода и углеки...
2 г. назад
Карбид кальция массой 6,4 г растворили в 87 мл бромоводородной кислоты (плотность 1,12 г/мл) с массовой долей...

8 г. назад
В аппарате Киппа углекислый газ получают реакцией между карбонатом кальция и раствором соляной кислоты....

1 мес. назад
Роголистник в аквариуме при подходе со вкусом, смотрится довольно хорошо и у него есть масса положительных...
turprikol.com
- Масса углекислого газа

- Устройство солнечной батареи

- Устройство солнечной батареи

- Асп 1

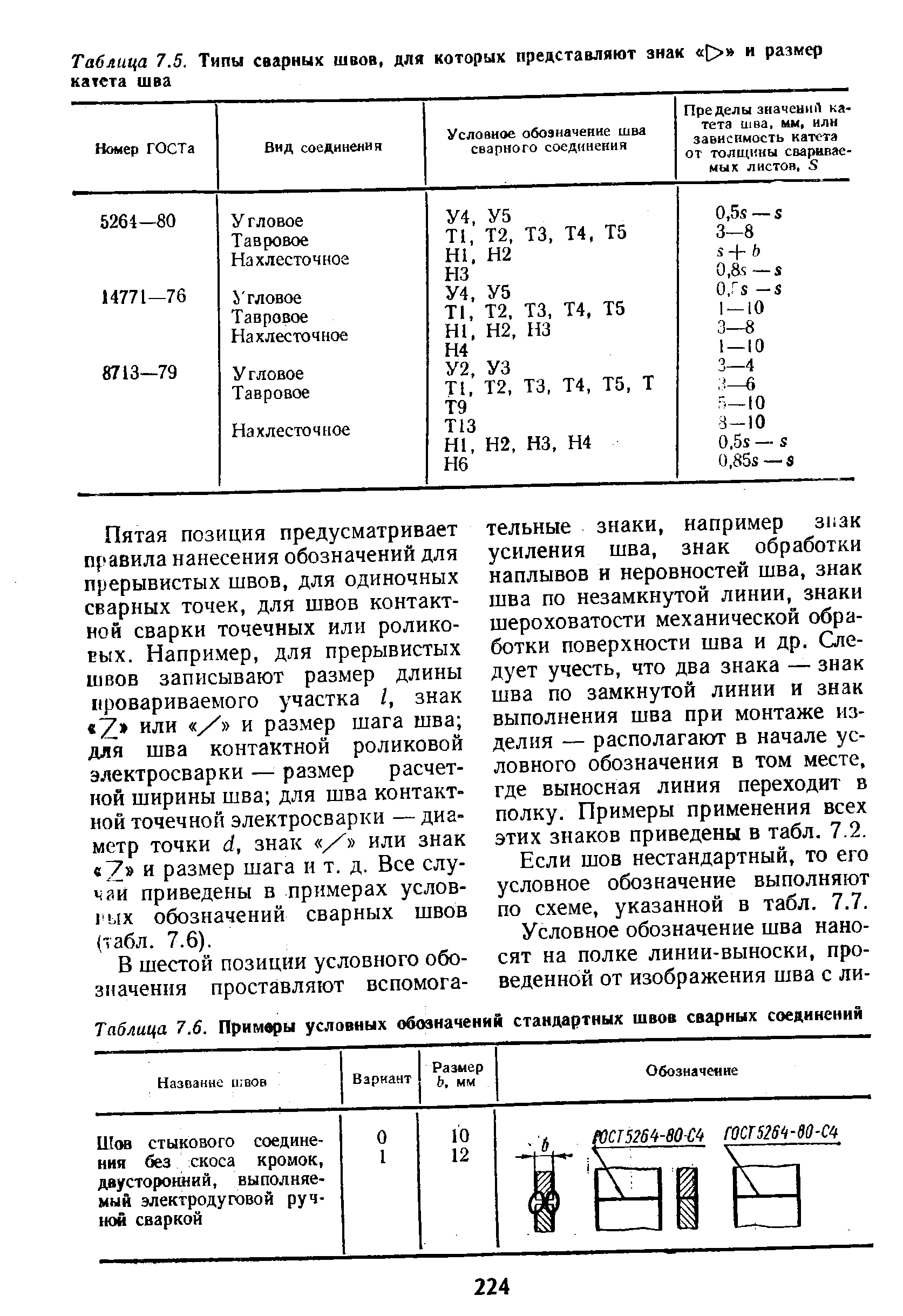
- Что такое катет шва
- Асп 1

- Что такое катет шва

- Дробеструйная обработка металла

- Дробеструйная обработка металла

- Принцип работы поршневого компрессора
- Принцип работы поршневого компрессора