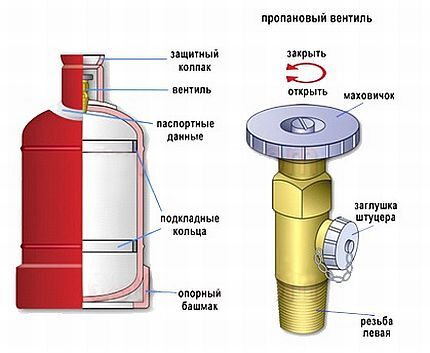
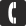Удельная теплоемкость углекислый газ. Температура замерзания углекислого газа
Удельная теплоемкость углекислый газ — сборник таблиц
Углекислый газ - бесцветный газ со слегка раздражающим запахом ( практически без запаха). При температуре -78.5 oC и атм. давлении формирует снег или лед углекислого газа ("сухой лед"). Название "сухой лед" объясняется тем, что при НУ замерзший углекислый газ переходит сразу в газовую фазу, минуя жидкую фазу.
В таблице ниже приведены значения удельной теплоемкости для газовой фазы CO2 в зависимости от температуры. Величины относятся к недиссоциированному состоянию газа. При температурах свыше 1500 °K (1227 °С) диссоциация для углекислого газа становится уже существенным фактором.
|
Температура |
Удельная теплоемкость, cp кДж/(кг*K) = кДж/(кг*С)
|
|
|
°C |
°K |
|
|
-98 |
175 |
0.709 |
|
-73 |
200 |
0.735 |
|
-48 |
225 |
0.763 |
|
-23 |
250 |
0.791 |
|
2 |
275 |
|
|
27 |
300 |
0.846 |
|
52 |
325 |
0.871 |
|
77 |
350 |
0.895 |
|
102 |
375 |
0.918 |
|
127 |
400 |
0.939 |
|
177 |
450 |
|
|
227 |
500 |
1.014 |
|
277 |
550 |
1.046 |
|
327 |
600 |
1.075 |
|
377 |
650 |
1.102 |
|
427 |
700 |
1.126 |
|
477 |
750 |
1.148 |
|
527 |
800 |
1.168 |
|
577 |
850 |
1.187 |
|
627 |
900 |
1.204 |
|
677 |
950 |
1.220 |
|
727 |
1000 |
1.234 |
|
777 |
1050 |
1.247 |
|
827 |
1100 |
1.259 |
|
877 |
1150 |
1.270 |
|
927 |
1200 |
1.280 |
|
977 |
1250 |
1.290 |
|
1027 |
1300 |
1.298 |
|
1077 |
|
1.306 |
|
1127 |
1400 |
1.313 |
|
1227 |
1500 |
1.326 |
|
1327 |
1600 |
1.338 |
|
1427 |
1700 |
1.348 |
|
1527 |
1800 |
1.356 |
|
1627 |
1900 |
1.364 |
|
1727 |
2000 |
1.371 |
|
1827 |
2100 |
1.377 |
|
1927 |
2200 |
1.383 |
|
2027 |
2300 |
1.388 |
|
2127 |
2400 |
1.393 |
|
|
2500 |
1.397 |
|
2327 |
2600 |
1.401 |
|
2427 |
2700 |
1.404 |
|
2527 |
2800 |
1.408 |
|
2627 |
2900 |
1.411 |
|
2727 |
3000 |
1.414 |
|
3227 |
3500 |
1.427 |
|
3727 |
4000 |
1.437 |
|
4227 |
4500 |
1.446 |
|
4727 |
5000 |
1.455 |
|
5227 |
5500 |
1.465 |
|
5727 |
6000 |
|
www.funtable.ru
Углекислота тройная точка - Справочник химика 21
Для СО2 тройная точка находится при давлении 5,11 атм. Поэтому при атмосферном давлении твердая углекислота (сухой лед) не переходит в жидкость, а возгоняется. На рис. 4.3 приведена диаграмма состояния СО2. Кривая ОВ для СО2 имеет положительный наклон. Значит, температура плавления с [c.158]
Если для некоторого вещества давление, соответствующее тройной точке, окажется выше 1 ат, то это вещество вообще нельзя расплавить под атмосферным давлением. Такие вещества, примером которых может служить углекислота, не имеют, следовательно, при нормальном давлении ни температуры плавления, ни температуры кипения. [c.44]В точке В Пересекаются три кривые равновесных состояний углекислоты. Эта точка характеризует такое состояние углекислоты, при котором в термодинамическом равновесии находятся одновременно три фазы. Параметрами этой точки, называемой тройной точкой, являются давление р = 517 кПа и температура [c.284]
Холодопроизводительность 1 кг углекислоты равна разности энтальпий парообразной углекислоты, имеющей давление И температуру охлаждаемой среды, и твердой углекислоты. Теплота плавления (или замерзания) углекислоты в тройной точке равна разности энтальпий жидкой и твердой углекислоты при давлении 517 кПа. Значение теплоты плавления в тройной точке составляет 195,7 кДж/кг. При давлениях выше 517 кПа и температурах выше —56,6 °С теплота плавления практически мало отличается от теплоты плавления в тройной точке. [c.285]
Снижение давления жидкой углекислоты от давления конденсации дс давления тройной точки может происходить как при однократном дроссели ровании (простой цикл), так и при многократном (цикл с промежуточным отводом пара). При этом давление конденсации может принимать следующие значения 6370—6860 кПа (цикл высокого давления), 1568—1960 кПа (цикл среднего давления), 736—882 кПа (цикл низкого давления). [c.288]
Схема производства сухого льда методом прессования с циклом высокого давления. Снег, получаемый при дросселировании жидкой углекислоты до давления ниже давления тройной точки, превращается в блоки сухого льда в результате его сжатия (прессования). Удельная масса сухого льда зависит от давления и продолжительности сжатия, а также от формы блока и практически составляет 1,4—1,6 кг/дм . Прн получении сухого льда методом прессования в специальных сухоледных прессах давление сжатия снегообразной массы больше, чем в льдогенераторах. Углекислый газ и отсасываемые из пресса пары (нижний отсос) поступают к всасывающей стороне основного компрессора, Которым они сжимаются до давления конденсации. Схема сжижения [c.288]
Полученные при дросселировании пары отсасываются третьей ступенью Дополнительного компрессора, а жидкая углекислота дросселируется до давления 980—1470 кПа во второй промежуточный сосуд. Образовавшиеся при дросселировании пары через теплообменник отсасываются второй ступенью дополнительного компрессора, а жидкая углекислота, пройдя мерный бачок, обеспечивающий заполнение пресса необходимым количеством жидкости, дросселируется в снеговые камеры сухоледного пресса до давления, равного давлению тройной точки, 517 кПа. [c.289]
Для анализа процесса сублимации используют диаграмму состояний температура — давление, представленную на рис. 14.13. На этой диаграмме линия Л5 (линия сублимации) характеризует равновесие между твердой и паровой фазами. Линия 5С (линия испарения) соответствует состояниям равновесия между жидкой фазой (расплавом) и паровой. Линия (линия плавления) определяет равновесие между твердым веществом и расплавом. При более низких давлениях, чем давление, соответствующее тройной точке 5, твердое вещество не может расплавиться, и в этих условиях осуществляется процесс перехода вещества из твердой фазы в паровую, минуя жидкую. Например, тройная точка для диоксида углерода характеризуется параметрами Тз = —57 °С, 5 = 0,5 МПа при давлениях ниже 0,5 МПа не может образоваться жидкая углекислота в результате нагрева твердой углекислоты, так как твердое вещество испаряется, минуя жидкую фазу. На диаграмме 1—р рис. 14.13 показан процесс сублимации твердого вещества при давлении ро в виде рабочей линии ВЕР. Отрезок ОЕ соответствует нагреву твердого вещества от температуры tD до температуры испарения tE. В точке Е происходит сублимация при температуре 1е, а отрезок ЕР соответствует перегреву паров до температуры tF. Процессу десублимации, как процессу, обратному сублимации, соответствует рабочая линия РЕВ. [c.363]
После наполнения ледогенератора жидкой углекислотой открывают диафрагмы,, создающие большое сопротивление для прохода жидкой углекислоты и вызывающие дросселирование ее. При этом давление падает ниже тройной точки, и углекислота начинает затвердевать. Ввиду перепада давлений жидкая углекислота кипит и пары ее отсасываются через поры твердого слоя. Необходимая для этого теплота парообразования отнимается от жидкой углекислоты, вследствие чего она затвердевает и получается уплотненный блок сухого льда. Продолжительность образования блока весом приблизительно 40 кг при размерах основания 190 X 190 мм и высоте около 800 мм составляет 40—60 мин. Пары из ледогенератора и промежуточных сосудов отсасываются компрессором, сжимаются в нем до 70 ата и направляются в конденсатор. [c.306]Производство сухого льда прессованием заключается-в дросселировании жидкой углекислоты из конденсатора при давлении около 70 ата в промежуточный сосуд до давления 16—20 ата и затем в полость пресса, в котором поддерживают давление, близкое к тройной точке. В результате внизу пресса образуется снегообразная углекислота и пары ее отсасываются первой ступенью компрессора. Затем эти пары вместе с парами из промежуточного сосуда сжимаются во второй ступени компрессора до 70 ата и направляются в конденсатор, а полученная в нем жидкая углекислота—на производство i снегообразной углекислоты- [c.309]
Тройная точка углекислоты [c.19]
В диаграмме фазового равновесия углекислоты (рис. 1) показано положение тройной точки. [c.20]
Плавление твердой углекислоты происходит дри температурах и давлениях, равных или выше тройной точки. Ниже тройной точки твердая углекислота непосредственно переходит в газообразное состояние (сублимирует). При этом температура сублимации является функцией давления при нормальном давлении она равна —78,5°, а при вакууме, в зависимости от его глубины, может быть равна —100° и ниже. [c.21]
Следует особо отметить, что при плавлении твердой углекислоты объем ее увеличивается в противоположность водному льду. В тройной точке это увеличение особенно существенно удельный объем твердой углекислоты 0,661 л/кг, жидкой — 0,849 л/кг. Увеличение составляет 28,5%, в то время как объем водного льда при превращении в воду уменьшается на 10%. [c.21]
Осушка сырьевого газа и освобождение его от сравнительно легко конденсирующихся примесей (углекислоты,. метана) не представляет больших затруднений и может быть осуществлена методами, хорошо разработанными в промышленном масштабе для воздухоразделительных установок. Наибольшие затруднения связаны с очисткой газа от азота и окиси углерода. Обе эти примеси весьма близки по своим физическим свойствам, и поэтому при затвердевании они образуют смешанные кристаллиты, имеющие температуру тройной точки, промежуточную между чистым N2 (63,ГК) и чистым СО (67,2° К), и упругость пара, также промежуточную между значениями ее для чистого N. и чистого СО [c.114]
В цикле получения твердой углекислоты используется то обстоятельство, что тройная точка имеет сравнительно высокую темпера-туру — 56,6°С при давлении 5,3 ата. [c.410]
В тройной точке газообразная, жидкая и твердая фазы находятся в равновесии. При давлении ниже 5,3 ата, т. е. после третьего дросселирования имеем уже двухфазную систему пар — твердая углекислота (сухой лед выпадает в специальном генераторе). Промежуточное охлаждение осуществляется за счет смешения. При определении количеств рабочего тела, циркулирующего через ступени низкого, среднего и высокого давлений, все потоки относят к 1 кг вещества, проходящего через цилиндр высокого давления и конденсатор. [c.410]
Физические свойства твердой углекислоты. Фазовая диаграмма для углекислоты приведена на рис. Х.23. Параметры тройной точки М для углекислоты давление 5,28 ата и температ фа —56,6° С. В связи с этим углекислота в жидком состоянии может существовать только при давлениях выше 5,28 атл, а при более низких давлениях, в том числе атмосферном, может быть или в твердом, или газообразном состоянии. [c.385]
Хотя все твердые тела при давлении более низком, чем давление соответствующее своей тройной точке, сублимируют в случае подвода тепла, а некоторые из них, в том числе и вода, совершают этот процесс при отрицательных температурах (т. е. тоже могут быть названы сухим льдом ), термин сухой лед укоренился только за твердой углекислотой. [c.386]
Третья стадия производства сухого льда — получение твердой углекислоты из жидкой — могла бы быть осуществлена путем замораживания жидкой углекислоты в формах подобно тому, как это выполняется при производстве водного льда. Однако такой способ оказался бы не только не интенсивным, но и потребовал бы дополнительную холодильную установку, работающую при температуре кипения более низкой, чем температура тройной точки [c.395]
Точка О, в которой существуют совместно все три фазы, называется тройной точкой. Обычно она лежит при давлении в 1 атм или меньше, но имеются интересные исключения. Из продуктов промышленного значения такое исключение обнаруживает, например, углекислота СОд, тройная точка которой находится при — 56,6°С и 5,1 атм, т. е. немного выше нормальной точки кипения — 78,5°С, которая, таким образом, становится точкой сублимации. [c.263]
Интересно отметить, что если в камере твердой углекислоты поддерживать давление, равное 5,28 ат (тройная точка), т. е. немного больше, чем в рассмотренном случае, то расширение приведет к образованию смеси жидкости и твердого вещества, которая легче уплотняется в твердый лед—СО2, чем твердая углекислота в виде снега. После того как образовалось необходимое количество смеси, давление для превращения жидкости в твердое вещество поднимается до 1 ат. Это является основой важного процесса производства СОг- [c.521]
Двуокись углерода (СОг) может находиться в газообразном (углекислый газ), сжиженном (углекислота) и твердом (сухой лед) состоянии. Агрегатное состояние двуокиси углерода зависит от его теплосодержания (энтальпии), температуры и давления. Так, в сжиженном виде двуокись углерода может находиться при давлении от 73 (критическое) до 4 28 ат (давление тройной точки) и температуре от 31 до —56,6°С. При температуре ниже —66,6°С двуокись углерода переходит в твердое состояние, а лри температуре выше 31°С может находиться только в газообразном состоянии. [c.182]
Зная весовые доли каких-либо других фаз, нетрудно рассчитать энтальпию углекислоты в тройной точке. [c.370]
По тепловым диаграммам для углекислоты легко определить теплоту сублимации сухого льда при различных давлениях, его холодопроизводительность, теплоту плавления в тройной точке и т. д. Например, теплоту сублимации при заданном давлении (р = 5,28 ата) определяют как разность энтальпий равновесных [c.370]
В отличие от обычной трехступенчатой машины, осуществляющей замкнутый холодильный цикл, холодильная машина для сухого льда работает разомкнутым циклом. Важной особенностью углекислоты является сравнительно высокое значение тройной точки, т. е. состояния, в котором газообразная, жидкая и твердая фазы находятся в равновесии. Тройная точка углекислоты характеризуется давлением 5,3 ата и температурой минус 56,6°. Заметим, что при давлении ниже 5,3 о/па углекислота не плавится, а сублимирует, образуя систему твердая фаза—пар. В этом свойстве—одно из серьезных преимуществ углекислотного льда как охлаждающего средства, благодаря которому он и получил название сухого. Теплота сублимации углекислоты при давлении 5,3 ama составляет 30 ккал/кг, а при 1 ата—137 ккал/кг. Принципиальная схема трехступенчатой машины, работающей разомкнутым циклом, показана на рис. 91,а, а ее процессы в энтропийной диаграмме на рис. 91, б. Машина работает следующим образом. Газообразная углекислота в состоянии О засасывается компрессором ступени низкого давления вместе с холодными парами состояния УУ, образовавшимися в дроссельном процессе 9—9. После смешения углекислота характеризуется состоянием У. Далее она последовательно адиабатно сжимается в трех ступенях (процессы 1—2, 3—4 и 5—6) и направляется в кон- [c.219]
В тройной точке для СОа температура —56,6° и давление 5,28 ama. Жидкая углекислота может иметь температуру выше —56,6°. Температура сублимации твердой углекислоты при атмосферном давлении — 78°. Сублимирующая твердая углекислота называется сухим льдом . [c.16]
Тройная точка углекислоты. Характеризуется давлением 5,28 ата и температурой —56,6°. [c.469]
Сведения о термодинамических свойствах углекислоты, таких, как I и 5, содержатся в — р- к Т — 5-диаграммах. Однако эти диаграммы не позволяют судить о количественном соотношении фаз в тройной точке, а следовательно, не дают возможности определить энтальпию или энтропию трехфазной смеси. В этом случае требуются дополнительные расчеты. Так, для определения энтальпии трехфазной смеси пользуются уравнениями Сх = 1"у + "г = 1, [c.284]
Тройная точка азота. В тройной точке азота, 63,Г К, давление паров углекислоты уменьшается до 10 2 мм рт. ст., а СО, в равновесии с твердой фазой [135], имеет еще давление 40 ммрт. ст. Поэтому, подкачивая жидкий азот в охлаждаемый отросток, можно удалить эту мешающую примесь окиси углерода. Чтобы подавить выбросы, следует соблюдать осторожность при пропускании азота в охлаждаемый отросток через капилляр при откачке. СО с той стороны вентиля, где имеется высокое давление, можно очистить даже в нормальной точке кипения азота (77,35° К). В ней давление паров СО2 равно 1,05-10" мм рт. ст., а давление паров СО — 453 мм рт. ст. Поэтому концентрацию СО2 можно свести к 2,3 частей на 10°. [c.279]
Сухой лед — твердая углекислота, которая при подводе тепла непосредственно переходит в парообразное состояние, минуя жидкую фазу. Поэтому твердая углекислота, не оставляюш,ая после себя жидкого следа, и называется сухим льдом. Такое изменение агрегатного состояния — сублимация твердой углекислоты — обусловлено ее физическими свойствами и положением тройной точки, характеризую-ш,ей равновесие твердой, жидкой и парообразной фаз (фиг. 208). [c.304]
Только 1в тройной точке углекислота находится во всесх трех состояниях твердом, жидком и газообразном. При давлениях ниже 5,28 ата (или при температурах ниже —56,6°) она не может находиться в жидком состоянии, то есть ниже тройной точки в равновесии могут быть только две фазы твердая и газообразная (табл. 6). [c.19]
При дросселировании жидкой углекислоты в снеговую камеру пресса в ней поддерживается давление нескдлько выше давления тройной точки (4,28—4,5 ати) получающийся при этом газ отсасывается первой ступенью дополнительного компрессора. Во вторую ступень компрессора поступают пары из первой его ступени и из промежуточного сосуда. Все пары в дополнительном компрессоре сжимаются до 60—70 ати, сжижаются в конденсаторе и в жидком состоянии направляются обратно в су.хо-ледный цикл. [c.128]
Однако в литературе существуют указания на то, что в некотором температурном интервале нихе тройной точки сорбированные вещества, такие как бензол, н.-гексан, углекислота, могут находиться в жидкоподобном состоянии [1,2,3,4]. Эти сведения основываются как на виде изотерм сорбции с явно вырахенныи гистерезисом десорбцион-ной ветви, так и на обнаруженном в результате термохических исследований фазовом переходе типа жидкость - твердое тело. Более того, Хигути из термодинамических соображений было выведено уравнение, позволяющее рассчитать понижение температуры тройной точки в зависимости от радиуса кривизны поверхности капиллярно-конденсированного вещества и вида этого вещества [5]. [c.163]
Для охлаждения калориметра вакуумная камера обычно погружается в охлаждаюущую ванну — сосуд Дьюара с подходящим хладоагентом. В качестве хладоагентов используют жидкий водород (иногда жидкий гелий), жидкий азот, твердую углекислоту в смеси, например, со спиртом, лед. Для еще большего понижения температуры часто практикуется испарение жидкого водорода или жидкого азота при пониженном давлении. При откачке паров азота или водорода насосом большой производительности, например ВН-2 или РВН-20, можно охладить азот или водород ниже тройной точки и достигнуть в ванне с твердым азотом температуры 50—52° К, а в ванне с твердым водородом 10—12° К. [c.307]
Свойство углекислоты сублимировать обусловлено положением тройной точки t = —56,6° С р = 0,516 Мн1м ). При рдвух агрегатных состояниях — твердом или газообразном, поэтому нельзя получить жидкую углекислоту при этом условии. Плотность углекислоты зависит от р, t VI агрегатного состояния, в котором она находится плотность углекислого газа при 0°С и р = 0,1 Мн/м равна 1,977 кг1м плотность твердой углекислоты колеблется в пределах l,3-f-l,6 кг/л и зависит от пористости, определяемой методом производства. Теплота плавления твердой углекислоты или замерзания жидкой при параметрах тройной точки равна разности между теплотой сублимации 545 кдж/кг=129,88 ккал/кг и теплотой парообразования 348 кдж/кг = 83, 2 ккал/кг и составляет 197 кдж/кг— 46,76 ккал/кг. При изменении давления и температуры величина теплоты плавления меняется незначительно. Теплота сублимации при давлении 0,098 Мн/м =1 ат и t = —78,9° С составляет 574 кдж/кг=136,89 ккал/кг. Холодопроизводительность сухого льда определяется с учетом теплоты сублимации и нагревания полученных холодных паров за счет окружающей среды до 0°С. Холодопроизводительность сухого льда составляет 638 к ( ж/ г= 162 ккал/кг, что в 1,9 раза больше холодопроизводительности водного льда при 0°С, равной теплоте плавления 333,2 кдж/кг=80 ккал/кг. [c.333]
Производство сухого льда. Наиболее распространенными способами получения сухого льда являются 1) дросселирование жидкой углекислоты до р ниже давления тройной точки и прессования полученного снега 2) испарение жидкой углекислоты, находящейся под р—0,7 0,9 Мн1м =7- 9 ат с частичной сублимацией образовавшейся твердой углекислоты и отводом паров через поры блока. [c.338]
Однако эти диаграммы не позволяют судить о количественном еоатношении фаз в тройной точке. Следовательно, они не дают возможности также определить энтальпию или энтропию углекислоты. В этом случае требуются дополнительные расчеты. Так, например, для определения энтальпии трехфазной смеси имеются два уравнения [c.370]
chem21.info
Почему весь углекислый газ не замёрз в Антарктиде?
Вопрос становится интересней и понятней, если говорить не об углекислом газе, а водяных парах. Водяного пара в атмосфере тоже много. По идее, из-за диффузии он проникает на полюса, где превращается в лед. При таком взгляде, все океаны на Земле рано или поздно должны испариться и замерзнуть ледяной шапкой на полюсах. Однако, это не происходит. Вопрос: почему? Речь идет о динамическом равновессии. Проще говоря, углекислый газ, который мог замерзнуть при экстремально низкой температуре рано или поздно испарится. Холодные воздушные фронты, идущие от полюсов возвращают замерзжую углекислоту в привычный газовый обмен земной атмосферы.
Температуры ниже минус семидесяти пяти и в Антарктиде бывают редко. Средняя температура на "полюсе холода" в Антарктиде в самый холодный месяц года - -66 градусов.
Антарктида принадлежит Гее, а не какому-нибудь из других "мужских" греческих богов, скажем, Юпитеру или Меркурию. Стало быть, она - Земля-Гея - может вполне претендовать на указанный зарегистрированный минимум температуры. Тогда ещё интереснее: почему до сих пор не замёрзли океаны?
Потому что -78 С - это для парциального давления СО2 в 1 атмосферу. А в воздухе его меньше процента и соответственно его собственное давление меньше и замерзнет он разве что в азотной ловушке с жидким азотом. А при -78 испарится и сухой лёд в открытой ёмкости.
Теория то хороша, вот только не надо забывать что замерзание зависит не только от температуры, но и от давления, а поскольку давление НАСТОЛЬКО сильно не увеличивается (можно считать за постоянное) , а разница температуры замерзания и температуры атмосферы не большое (к тому же она там не всегда равна указанной тобой температуре) , то равновесие "газ - твердое вещество" будет все таки в какой то степени смещенно в лево (к газу) , и весь газ не перейдет в твердое состояние.
СмЯшно. Про давление не забывайте, ага. Особенно - про парциальное.
Да там -80 редко бывает, не успевает весь замерзнуть, потом при замерзании таких объемов углекислоты должно выделяться много тепла соответственно температура повысится и все снова растает
там давление меньше атмосферного тк высота 4500метров
touch.otvet.mail.ru
Углекислый газ сухой лед - Справочник химика 21
Диоксид, обычно называемый двуокисью угле рода, СО2 образуется при полном сгорании свободного углерода в атмосфере кислорода. Он представляет собой бесцветный газ, в связи с чем и носит тривиальное название углекислый газ . Теплота образования двуокиси углерода из графита составляет 393,7 кдж г-моль. Плотность двуокиси углерода при н.у. 1,977 г/л (по воздуху 1,53). Двуокись углерода легко сжижается ее критическая температура 31,3° С, критическое давление 72,9 атм.. При сильном охлаждении она превращается в белую снегообразную массу (сухой лед), которая при нормальном давлении возгоняется (не плавясь) при —78,5 С. При давлении 5 атм твердая двуокись углерода плавится при —56,7 С. Теплота плавления двуокиси углерода 51 дж г, теплота испарения (при —56 С) 569 5ж/г. Жидкая двуокись углерода не проводит электрического тока. Кристаллическая решетка — молекулярного типа. [c.196]
Примем, что 10% кислорода топлива дадут ири сухом разложении углекислый газ по реакции [c.285]
В сухом колошниковом газе по объему до 32% оксида углерода (И), 9—14% углекислого газа, остальное — азот. Сколько ио расчету кубических метров кислорода требуется для сжигания 1000 м этого газа [c.131]
СО. СО, 0 и N2 — содержание (в % объ-змн.) соответственно углекислого газа, окиси углерода, кислорода и азота в сухих газах. [c.280]
В последнее десятилетие начал особенно интенсивно разрабатываться метод увеличения нефтеотдачи путем нагнетания в залежь углекислого газа. Углекислый газ непосредственно не смешивается в нефтью в пластовых условиях, но по мере продвижения по пласту в углекислом газе все больше растворяются легкие УВ нефти и одновременно газ растворяется в нефти. Этот процесс приводит к образованию переходной зоны, и при длительном контакте возможно полное смещение СО2 с нефтью. Так как углекислый газ растворяет УВ лучше, чем метан и сухой природный газ, то давление смесимости при нагнетании в пласт СО2 всегда ниже, чем при закачке сухого природного газа. [c.118]
Получение белого фосфора из красного. На дно сухой пробирки длиной 17—20 см поместите 0,3—0,5 г сухого красного фосфора так, чтобы он не попал на стенки пробирки. В течение 1 мин пропустите в пробирку сухой углекислый газ. Укрепите пробирку в лапках штатива, находящегося в вытяжном шкафу, в горизонтальном положении. Неплотно закройте ее пробкой из ваты и слегка нагрейте ту ее часть, где находится фосфор. Наблюдайте осаждение белого фосфора на холодных частях пробирки. В темноте мон но увидеть свечение белого фосфора, вызванное его [c.179]
Помещают в сухую пробирку кирпичик, приготовленный заранее из известкового раствора. Пропускают в пробирку углекислый газ до момента появления влаги на стенках пробирки. Обратить внимание на тепловой эффект реакции. Написать уравнение реакции карбонизации с учетом теплового эффекта. [c.112]
Углекислый кальций и углекислый магний (в сумме) в пересчете на сухое вещество. [c.63]
Механическое смешение фтористого натрия, талька, углекислого магния и сухих минеральных красок [c.233]
Модифицированный ТЗК. Перед приготовлением адсорбента из ТЗК его обрабатывают. Из порошка ТЗК отсеивают 500 г целевой фракции с частицами размером 0,25 — 0,5 мм. Отсеянную фракцию обрабатывают 2%-ным водным раствором углекислого натрия, затем воду испаряют в сушильном шкафу при 150 С и периодическом перемешивании порошка стеклянной палочкой. После удаления воды сухой порошок помеш ают в фарфоровую чашку и ставят в муфельную печь для прокаливания при 800 °С в течение 3 ч. Обработанный содой и прокаленный в муфеле ТЗК охлал дают в эксикаторе там же его хранят, используя по мере надобности. [c.98]
Высший оксид углерода (IV) СОг (углекислый газ) — бесцветный газ, имеющий слабокислый запах и вкус. Он в 1,5 раза тяжелее воздуха (р = 1,98 г/л). В одном объеме воды при 20 °С растворяется 0,88 объема СО2. При охлаждении в условиях нормального давления газ затвердевает при — 78,515 С, минуя жидкое состояние. Твердый оксид углерода (IV) — снегообразная масса, называемая сухим льдом. Жидкий СО2 образуется только под давлением (при 20 °С, 58,46-10 Па). [c.133]
Для некоторых природных газов характерно высокое содержание азота например, в султангуловском газе Куйбышевской области его 20%. В таких газах азоту часто сопутствуют редкие газы — гелий, аргон и др. Содержание гомологов метана в природном газе невелико этана от 0,1 до 8,0% (редко), пропана от 0,1 до 3%, бутана и высших, как правило, — доли процента. Примеси углекислого газа не превышают 2,5%. Ввиду резкого преобладания метана и небольшого количества углеводородов С4—С5 большинство природных газов относят к так называемым сухим газам. [c.22]
В пробирках находятся сухие хлористый кальций, углекислый натрий, сернокислый калий, хлористый барий. Как распознать эти вещества, не прибегая к помощи химических реактивов [c.76]
Хлористый кальций содержит всегда некоторое количество окиси кальция, поглощающей вследствие этого, кроме воды, также углекислый газ. Поэтому через трубкн с хлористым кальцием необходимо сначала пропустить сильный ток углекислого газа и затем продуть сухим воздухом. [c.187]
Значительно труднее отделить магний, так как для этого необходимо предварительно удалить аммонийные соли выпариванием раствора и прокаливанием сухого остатка. После этого магний отделяют от щелочных металлов путем осаждения раствором гидроокиси бария или, удобнее, спиртовым раствором углекислого аммония. Осадок углекислого магния отфильтровывают, фильтрат выпаривают, прокаливают и взвешивают сульфаты щелочных металлов. Ниже подробнее описан ход анализа этим методом. [c.470]
В небольших количествах (0,03% по объему) углекислый газ всегда содержится в воздухе. Он не имеет цвета и запаха. При —78,5° С превращается в твердую снегообразную массу, называемую сухим льдом , который возгоняется, не плавясь. [c.246]
Получение сухого льда . На вентиль баллона с СО2 наденьте мешок из плотной ткани и пропустите сильный ток газа. Наблюдайте образование в мешке сухого льда . Измерьте температуру твердого углекислого газа. [c.207]
Соберите прибор для получения чистого и сухого газа. Это могут быть кислород, водород, хлор, углекислый газ и др. Если Вы не будете пользоваться аппаратом Киппа, рассчитайте то количество исходного вещества (но в трехкратном избытке), которое потребуется для получения объема газа, соответствующего емкости колбы. [c.119]
Воздух имеет сложный состав. Его основные составные части можно подразделить на три группы постоянные, переменные и случайные. К первым относятся кислород (около 21% по объему), азот (около 78%) и так называемые инертные газы (около 1%). Содержание этих составных частей практически не зависит от того, в каком месте поверхности земного шара взята проба сухого воздуха. Ко второй группе относятся углекислый газ (0,02—0,04%) и водяной пар (до 3%). Содержание случайных составных частей зависит от местных условий вблизи металлургических заводов к воздуху часто бывают примешаны заметные количества сернистого газа, в местах, где происходит распад органических остатков, — аммиака и т. д. Помимо различных газов, воздух всегда содержит большее или меньшее количество пыли. [c.34]
Так как СОг не поддерживает жизнедеятельности бактерий и плесеней, сроки сохраняемости пищевых продуктов в атмосфере этого газа увеличиваются. С другой стороны, повышение содержания СОг в воздухе теплиц ведет к стимулированию роста растений ( углекислое удобрение ). Практически это достигается путем помещения в теплицы кусков сухого льда. Для большинства овош,ных культур наиболее благоприятным оказалось содержание СОг от 0,2 до 0,3%. [c.508]
Тпе . Твердый углекислый газ — удобный хладагент, так ч. ii i (1м > как у него большая энтальпия испарения, причем он переходит в газообразное состояние, минуя жидкое. Поэтому его называют сухим льдом. В промышленности СО2 получают как побочный продукт при производстве извести из известняка и при брожении сахара. [c.498]
ВЗЯТЬ не Б большом избытке, нагревание смеси с обратным холодильником приводит к образованию некоторого количества сложного эфира. Сообщение о получении алкилсульфонатов при нагревании сульфохлорида со спиртом [145] показывает, что в данном случае взято эквимолекулярное количество спирта или реакция велась короткое время. н-Пропиловый и н-бутиловый эфиры п-толуолсульфокислоты с выходом 25—30% получены при нагревании с обратным холодильником сульфохлорида с 10%-ным избытком спирта [146]. При пропускании сухого воздуха через смесь п-толуолсульфохлорида и и-пропилового спирта при 100—125° с целью удаления образующегося хлористого водорода [147] получается около 70% сложного и около 5% простого эфиров. К реакционной смеси добавляется небольшое количество углекислого натрия для нейтрализации п-толуолсульфокислоты, могущей образоваться в результате побочной реакции. Другим побочным продуктом является, повидимому, хлористый этил, хотя он и не упоминается в сообщении. При нагревании бензолсульфохлорида и метилового спирта в запаянной трубке до 160° единственными продуктами реакции получаются хлористый метил и бензолсульфокислота [144]. Вторичные и третичные спирты, вероятно, легче превращаются в хлориды при действии сульфохлоридов, чем первичные спирты, однако опытных данных по этому вопросу не имеется. Наличие й-атома хлора в молекуле спирта как будто уменьшает побочные реакции, и при нагревании с обратным холодильником п-толуолсульфохлорида и избытком этиленхлоргидрина образуется не простой эфир или дихлорэтан, а сложный эфир [148]. Такое же действие оказывает цианогруппа — при кипячении ксилольного раствора Р-цианоэтилового. спирта с п-толуолсульфохлоридом в течение нескольких часов образуется соответствующий сложный эфир с выходом 65% [149]. [c.336]
В лаборатории углекислый газ получают при дей-ствии разбавленных соляной или азотной кислот на 4401(110 (. (пропускают через воду (для удаления следов хлороводорода) и через концентрированную серную кислоту (для осушки) и собирают (рис. 23.5). [c.498]
Для ликвидации небольших загораний веществ, не поддающихся тушению водой или другими огнетушащими средствами, применяют твердые инертные вещества в виде порошков. К таким веществам относятся хлориды щелочных и щелочноземельных металлов (флюсы), альбуминсодержащие вещества, сухой остаток после выпарки сульфитных щелоков, карналлит, двууглекислый и углекислый натрий, поташ, квасцы. [c.446]
Промышленный генератор СО2 позволяет получать при сжигании чистых (неодоризованных) СНГ чистый углекислый газ исключительно простым способом. При окислении СНГ при избыточном количестве воздуха образуется смесь СО2, паров воды и азота, которая может сразу же компримироваться и вдуваться непосредственно в напиток, так как пары воды конденсируются, а азот, обладающий меньщей, чем СО2, растворимостью, пройдет через жидкость, не абсорбируясь. При другом способе получения СО2 накапливается за счет абсорбции в одном из многочисленных селективных растворителей (моноэтаноламин, модифицированный карбонат калия, некоторые аминоспирты, сульфинол и т. п.), а затем регенерируется в виде концентрированного газа из растворителя. Дальнейшая очистка осуществляется при глубоком охлаждении (СО2 затвердевает при —78,5 °С, при этом отделяется большая часть газообразных примесей, имеющих более низкую точку кипения). Твердая двуокись углерода (сухой лед) используется для газирования напитков, в частности в тех случаях, когда масштабы розлива по бутылкам невелики, а организация местного производства СО2 неэкономична. [c.272]
Оксид углерода(1У), или диоксид углерода, СО2 — бесцветный газ. Он известен также под названием углекислый газ. Прн пониженной температуре или повышенном давлении СО2 легко переходит в жидкое и твердое состояние. Твердый оксид углерода(IV) называется сухим льдом. В больших количествах оксид углерода(IV) вреден для человека и животных, может вызвать удушье. [c.173]
Вторая группа включает методы, основанные на взаимораст-воримости нефтн и вытесняющего реагента углекислого газа, углеводородных газов высокого давления, растворителей и т. д. В эту группу входят следующие методы закачка сухого газа высокого давления вытеснение нефти обогащенным газом закачка диоксида углерода [c.188]
Snyder life испытаиие (трансформаторных масел) на срок службы [на стойкость к окислению] по Снайдеру soap определение жёсткости котельной воды (с помощью стандартных растворов углекислого кальция и сухого мыла) [c.509]
В большинстве органических соединений, в растворах азотнокислых, сернокислых и хлористых солей, в окиси углерода, сухом хлоре и сернистом газе, окислах азота, сероводороде, углекислом газе и т, п. аустенитиые хромоиикелевые стали достаточно устойчивы. [c.227]
Методика оцределения температуры замерзания применялась следующая. Собранный прибор без охладителя и образца углеводорода продувался ТОКОМ сухого воздуха со скоростью от 10 до 20 мл/мин. Рубашка пробирки для замора ки1 апия заполнена воздухом, освобожденным от углекислого газа и паров поды. [c.349]
Паро-кислородо-углекислотная конверсия. Паро-кислородо-углеки-слотная (ПКУ) конверсия применяется для получения технологического газа для синтеза метанола и высших спиртов. При замене 0,3 объема водяного пара углекислым газом степень превращения метана и содержание его в сухом конвертирова1Шом газе практически не меняются.Но равновесие сдвигается в сторону образования СО. И если при низких температурах происходит конверсия СО, образовавшейся из метана, то при BH oioix температурах протекает конверсия Og с получением дополнительного количества СО. [c.105]
Азотистокислый калий дает приблизительно такие же выходы, как и азотистокислый натрий, но с нитритами кальция и бария получаются нейколько пониженные результаты. В процессе сплавления в значительных количествах образуется спирт. Поскольку исходные соединения, повидимому, были сухими, становится неясным источник воды, необходимой для гидролиза. В течение реакции непрерывно выделяется окись азота, и возможно, что алкилнитриты образуются за счет взаимодействия азотистой кислоты со спиртами, а пе из исходных реагентов. При сплавлении смеси, содержаш ей метилсульфат калия, в качестве побочного продукта выделяется метиламин. Полученный указанным способом нитроэтан содержит небольшое количество нитробутана, образование которого, равно как и образование метиламина, объяснить затруднительно. Реакция нитритов с алкилсульфатами, в зависимости от взятого соединения, начинается при 90—140°, причем температуру начала реакции можно несколько снизить, прибавляя к реакционной Смеси небольшое количество воды. Согласно патенту [123], повысить выход нитросоединения можно смешением реагентов с углекислым натрием. [c.23]
В трехгорлую колбу, снабженную обратным холодильником и мешалкой, помещают 14,8 г изобутилового спирта, 45 мл воды и 12 г углекислого натрия. В смесь при непрерывном перемешивании и охлаждении в ледяной воде постепенно приливают раствор 20 г мар-ганцевокислого калия в 400 мл воды остальную часть окислителя добавляют небольшими порциями в сухом виде через боковой тубус (температура не должна подниматься выше 5° С). [c.138]
Кислород, применяемый в аппаратах искусственного дыхания, часто содержит углекислый газ, возбулодающий дыхательный центр. Можно ли получить из такого кислорода чистый и сухой кислород путем пропускания газа через трубку, содержащую [c.118]
Приборы и реактивы секундомер, термометр до 150 С, технохимические весы, прибор для получения углекислого газа (см, рис, 16), фарфоровая ложка, микроскоп, стеклянная пластинка, воронка, спиртовка, фарфоровая чашка, часовое стекло, фильтровальная бумага, стаканы фарфоровые емкостью 150 мл и 500 мп, пробка с отверстием для термометра, цилиндр мерный емкостью 50 мл, колба коническая емкостью 250 мл, бюретка емкостью 25 мл, "кипелки, сухой теплоизолирующий материал (асбестовая крошка, опилки, стекловата), известь-кипелка, гцпс природный и синтетический, вазелин. Растворы соляной кислогы эквивалентной концентрации - 1 моль/л и J = 1,19 г/см фенолфталеина сульфата аммония с массовой допей 10 % гидроксида кальция (насыщ.) карбоната натрия, роданида калия - 0,5 мопь/л. [c.110]
Соли надугольной кислоты (надуглекислые, или перкарбонаты) известны для Ыа, К и РЬ. Они образуются в результате анодного окисления концентрированных растворов карбонатов при низких температурах (по схеме 2СО3 — 2е = С О ) и представляют собой бесцветные (или бледно-синеватые) кристаллические вещества, чрезвычайно гигроскопичные, но в сухом состоянии устойчивые. При нагревании эти соли переходят в карбонаты с выделением углекислого газа и кислорода, при [c.509]
В земной атмосфере углерод находится в виде углекислого газа СОа. Содержание его в сухом воздухе незначительно и составляет приблизительно 0,03 объемных %. Интересно, что атмосфера планеты Вешра на 97% состоит из оксида углерода (IV). Это было вгервые установлено с помощью автоматической станции [c.410]
Крупная компания ОМИ (Удилайт, г Детройт, шт. Мичиган), которая является поставщиком сырья ДЛЯ цехов электролитических покрытий, извлекает никель из осадков, образующихся из сточных вод от установок ее заказчиков. Никель, являющийся дорогостоящим металлом, удаляют из сточных вод, содержащих раствор сернокислого никеля, путем осаждения его бикарбонатом натрия в виде нерастворимого углекислого никеля. Последний осаждают и затем обезвоживают пресс-фильтром до содержания в нем 50 % твердых веществ. Сухой осадок отправляют обратно поставщику в один из четырех региональных центров, где углекислый никель превращают в высококачественный раствор сернокислого никеля [43]. [c.93]
chem21.info
Опыты с сухим льдом
Любите удивлять своих друзей разными интересными фишками? Это очень здорово, уметь делать что-то, что не умеют другие, знать какие-то секреты. Но иногда для того, чтобы удивить публику, не нужно ни обмана, ни особой ловкости или специальных навыков.
Достаточно лишь иметь хорошие знания химии и сухой лёд. С ним вы сможете творить настоящие чудеса.
Что такое сухой лёд?
 Привычный лед нас не интересует. Эта вещь представляет собой газ в замороженном состоянии
Привычный лед нас не интересует. Эта вещь представляет собой газ в замороженном состоянииПривычный для нас материал, представляющий собой h3O в замороженном состоянии – вот что обычно называется льдом.
Но эта вещь не представляет для нас сейчас особого интереса. Наш материал не имеет никакого отношения к воде. Это углекислый газ в твёрдом состоянии. Основная особенность его в том, что он не тает.
В жидком состоянии углекислый газ может находиться только под очень сильным давлением. Тем не менее, материал выглядит именно как замороженная вода. Он похож на замороженную воду ещё и тем, что сам по себе достаточно холодный и в тёплой окружающей среде теряет твёрдую форму.
Только вот в отличие от воды, углекислый газ переходит из твёрдого состояния в газообразное, минуя жидкую форму. По-научному это называется сублимировать. Именно на этом свойстве основано множество необычных экспериментов.
Некоторые опыты выглядят по-настоящему эффектными и, имея необходимы материалы, можно сделать настоящее шоу, состоящее из необычных трюков и спецэффектов.
Но будьте осторожны. Замороженный углекислый газ – очень холодный, его температура – минус семьдесят девять градусов. Используя его, ни в коем случае не сжимайте его в руках и вообще не держите долго. Можно получить обморожение.
5 удивительных фокусов с сухим льдом смотрите в видео:
Кипение
 Удивить публику бурлящей газообразной массой вы сможете благодаря отличному знанию законов физики
Удивить публику бурлящей газообразной массой вы сможете благодаря отличному знанию законов физикиДля опыта вам понадобится стакан с горячей или сильно тёплой водой и несколько кубиков твёрдого газа.
Вы берёте кубики, и просто бросаете их в воду. И тут же вода начинает очень сильно бурлить, а из стакана густыми клубами валит пар, который больше даже похож на туман, так как очень густой, белый и, выходя из стакана, стелется понизу. Незнающие люди будут поражены. Особенно, если они будут думать, что это обыкновенная замороженная вода.
Почему получается такая реакция?
- Температура замерзания углекислого газа очень низкая. Он сублимирует даже на воздухе.
- Попробуйте оставить стакан с кубиками на какое-то время, и вы увидите, что через определённый временной промежуток стакан станет пустым. А в тёплой воде процесс протекает быстрее.
- Так как из твёрдого состояния вещество сразу переходит в газообразное, получается то, что получается. При этом, чем горячее будет вода, тем сильнее будет эффект.
Для зрелищности можно добавить в воду немного жидкого мыла или шампуня. Тогда будет образовываться много пены с крупными пузырьками. Ей можно зачерпнуть в ладошку и размять в руках. Тогда из лопнувших пузырьков будет выходить туман.
Прыгающий кубик
 Поймать прыгающий кубик льда будет уже невозможно!
Поймать прыгающий кубик льда будет уже невозможно!Этот эксперимент надо проводить в тёплом помещении, так как вам понадобится тёплая металлическая поверхность, а если в помещении будет холодно, металл тоже будет холодным, и ничего не получится.
Вам будет нужна любая металлическая поверхность (покрытие раковины, дно алюминиевой кастрюли, металлический поднос – что угодно).
Главное, чтобы поверхность не была холодной. Вы кладёте на неё кубик. И он начинает прыгать. При этом поймать его, после того, как он начал прыгать, практически невозможно.
Такая реакция происходит опять из-за свойства твёрдой формы газа сублимировать. На тёплой поверхности это происходит быстрее. Пузырьки газа лопаются, и кусочек подскакивает. А со стороны выглядит, как настоящая магия.
Музыка с помощью льда
 Попробуйте извлекать музыку из льда — получится удивительное шоу!
Попробуйте извлекать музыку из льда — получится удивительное шоу!Ещё один трюк, который работает за счёт сублимации. Положите кусочек на какую-нибудь мягкую поверхность, возьмите металлический предмет, например, алюминиевую ложечку, и надавите на кубик.
- Предмет из металла будет продавливать поверхность, а сам кубик при этом будет дребезжать.
- Дребезжит, на самом деле, конечно, не кусочек, а газовые пузырьки, которые при испарении бьются о металлические стенки.
Вещество используют в своём ремесле профессиональные иллюзионисты. Например, на его применении основан известный фокус с картой и льдом.
Зная свойства этого вещества, можно творить настоящие чудеса и поражать зрителей своим искусством.
blog.turbomagic.ru