Способ получения ацетилена из метана. Получение ацетилена из метана
Получение ацетилена из метана - Справочник химика 21
При помощи ионизирующего действия СВЧ-излучепия (СВЧ-разряда) возможно осуществить следующие химико-технологические процессы [1—3] синтез аммиака, получение окислов азота из воздуха (в производстве азотной кислоты) синтез соляной кислоты, синильной кислоты получение серы из сероводорода и дымовых газов крекинг нефти и нефтепродуктов получение ацетилена из метана производство спиртов реакции хлорирования, нитрования, гидроксилирования, карбоксилирования пт. п. синтез бензола, дифенилена, фенола полимеризацию этилена в полиэтилен получение ситалов получение сверхчистых пленок и металлов и т. д. [c.233]
Наиболее экономически выгодным по сравнению с современным способом окислительного пиролиза является метод получения ацетилена из метана в плазменной струе водорода. Разложение метана плазмохимическим методом протекает полнее, содержание ацетилена в газе оказывается более высоким. Вредные для процесса газы СО и СО2 при этом не образуются. [c.17]
Использование этих данных зависит от возможности достижения на промышленных установках необходимых температур и давлений и, с другой стороны, от экономической эффективности, связанной также с выходом, степенью конверсии и продолжительностью процесса. Наибольшая температура, применяемая в промышленности органической химии достигает 1400 °С (при получении ацетилена из метана),, а самая низкая может достигать —200 °С (при выделении этилена из газов коксования или крекинга). Максимальные давления могут достигать 2000 ат (при полимеризации этилена), а минимальные — 10 мм рт. ст. (при производстве пенициллина). Однако аппаратуру для температур превышающих 600—700 °С, и давлений выше 500 ат изготовить довольно трудно. [c.27]
Термохимические и термодинамические характеристики некоторых реакций, протекающих при получении ацетилена из метана [c.101]
Углерод образуется, как при термическом разложении сырья — благодаря теплоте сгорания метана (аналогично процессу получения ацетилена из метана неполным сжиганием), так и за счет разложения [c.121]
По опубликованным данным, получение ацетилена из метана рекомендуется осуществлять при 1400—2000° и пониженном давлении причем пребывание газов в нагретой зоне должно быть очень коротким (доли секунды). Из уравнения (2) (табл. 57) следует, что возможная максимальная концентрация ацетилена равна 25%, однако на практике такая концентрация не достигается. [c.273]
Получение ацетилена из метана. В дуговом разряде ацетилен получается из метана с выходом (по току) 1,3-10 моль/кДж. Предполагается образование через свободные радикалы СН4 СНз- СНа СаН СаНа. [c.267]
Каким бы способом пи получался ацетилен, в результате образуется газ, содержащий сравнительно немного ацетилена (8—14%). В табл. III.2 приведены составы газов, получающихся при различных процессах. Поэтому выделение, очистка и концентрирование ацетилена занимают в технологической схеме получения ацетилена из метана большое место. В настоящее время существует довольно много способов выделения ацетилена из газов. [c.121]
При получении ацетилена из метана частичным сожжением необходимо тщательное отделение СН4 от Нг, и СО, примеси которых приводят к взрыву реактора-горелки. Опасна также и пыль окислов железа [5]. [c.145]
Внимательно рассмотрите промышленную установку для получения ацетилена из метана (цветная вклейка рис. 1). [c.170]
Абсорбционные и хемосорбционные процессы весьма распространены и применяются в производстве серной, соляной, азотной, фосфорной кислот, аммиака, кальцинированной соды, при переработке коксового газа и газов нефтепереработки, при очистке промышленных газов (коксового, нефтяного, генераторного и др.), в технологии основного органического синтеза (разделение газообразных углеводородов, получение формальдегида, дивинила, получение ацетилена из метана и т. д.), в производстве целлюлозы, при концентрировании газов и т. д. Хемосорбция является важным этапом ряда синтезов в жидкой фазе, например прямой синтез азотной кислоты происходит путем хемосорбции кислорода раствором четырехокиси азота в азотной кислоте под давлением процессы оксосинтеза основаны на хемосорбции водорода и окиси углерода жидкими олефинами с образованием альдегидов и кетонов. [c.114]
Получение ацетилена из метана [c.357]
Подобное упрощение кинетической схемы реакции получения ацетилена из метана не является необходимым для применения предлагаемого ниже метода расчета. Оно сделано для того, чтобы не усложнять проводимые расчеты излишними деталями, роль которых относительно невелика. Предлагаемая ниже методика расчета может быть применена для более сложной кинетической схемы [c.13]
Рассмотрим подробнее вопрос о воз.можном влиянии диссоциации молекул На на процесс получения ацетилена из метана в плазменной струе водорода. В точке г число молекул Н, в 1 = с- п. Молекулы Нз диссоциируют согласно схеме Нз 2Н. Поэтому в 1 см содержится Ле = 2 а Т)щ атомов Ни [1 —а Т)]щ молекул Но. Таким образом, вместо п- частиц На в 1 см газа в отсутствие диссоциации имеется число частиц Нз и Н, равное [c.38]
Отметим, что для практических целей проведения процесса получения ацетилена из метана в плазменной струе и управления им, а также для закалки полученных целевых продуктов существенное значение имеют именно правые ветви кривых. [c.40]
Принудительное изменение температурного режима плазменной струи как один из методов управления процессом получения ацетилена из метана [c.60]
В статье на стр. 34 была рассмотрена возможность управления процессом получения ацетилена из метана в плазменной струе путем изменения начальной температуры процесса и других начальных условий. Естественно, более эффективно можно управлять плазмохимическим процессом рассматриваемого типа путем принудительного изменения температурного режима не в одной точке г = О, а на различных конечных участках плазменной струи. [c.60]
Получение ацетилена из метана в плазменной струе [c.72]
В настоящей работе, наряду с экспериментальными исследованиями процесса получения ацетилена из метана в плазменной струе, выполнены необходимые термодинамические расчеты для определения теоретически возможных степеней превращения метана в ацетилен, рассмотрены кинетические уравнения процесса, а также обсуждены аэродинамические параметры реактора. [c.72]
Экспериментальное исследование процесса получения ацетилена из метана в струе водородной плазмы [c.86]
Результаты опытов по получению ацетилена из метана в струе водородной плазмы [c.90]На основании накопленного экспериментального материала можно, кроме того, составить энергетический баланс получения ацетилена из метана в водородной плазме (табл. 10). Как видно из этой таблицы, 45% всей затрачиваемой энергии расходуется непосредственно на целевую химическую реакцию. Заметим, что в обычном окислительном пиролизе метана на собственно получение ацетилена расходуется лишь 30—35% подведенной энергии. [c.91]
В случае получения ацетилена из метана количество бензола — порядка 5-10 % (см. стр. 89), в случае пиролиза бензина — не более 2% [4]. [c.110]
Получение ацетилена из метана — типичная реакция третьего типа, поскольку ацетилен является промежуточным продуктом при разложении метана до углерода и водорода. [c.241]
Аналогичный способ, при котором тепло, необходимое для эндотермической реакции получения ацетилена из метана, образуется за счет сжигания части газа в смеси с кислородом, так называемый Захсё-процесс, рассмотрен ниже. [c.49]
В Германии регенеративный процесс получения ацетилена из метана разработан фирмой Рурхеми А. Г. [3]. Метан подвергали пиролизу под давлением 0,1 ата в вертикальных башнях, футерованных алундом и силли- [c.274]
Исходя из изложенного, для самостоятельного изучения а классс предлагаются следующие темы и вопросы полиэтилен и полипропилен, получение ацетилена из метана, нефтепродукты и их применение, промышленный синтез этилового спирта, применение альдегидов (при наличии кинофильма Фенолфор-мальдегидные пластмассы ), муравьиная и уксусная кислоты, гидролиз жиров в технике, гидрирование жиров, аминокислоты, синтетическое волокно капрон. Остальные темы и вопросы, обозначенные в таблице 14, изучаются учащимися дома. [c.156]
Сырьем для производства ацетилена по карбидному методу являются каменные угли, так как СаСд образуется при сплавлении извести СаО с коксом и антрацитом. В последние десятилетия разработаны и внедрены способы получения ацетилена из метана и его гомологов (стр. 135). Для получения ацетилена может быть использовано также жидкое нефтяное сырье. [c.132]
Эндотермические реакторы также можно назвать автотермиче-скими, если тепло, необходимое для проведения процесса, будет доставляться присоединением к реактору экзотермической установки. Примером может служить автотермический крекинг углеводородов. В этом случае тепло для эндотермического крекинга получают от сжигания в печи части углеводородов (печь в данном случае — экзотермический реактор). То же самое относится К" получению ацетилена из метана, а также этилена из этана или пропана. [c.48]
Очевидно, что количество тепла, необходимое для образования 1 моля С2Н2, очень быстро приближается к предельному значению - 70 ккал. Первый способ получения ацетилена из метана, так называемый электродуговой способ, разработан фирмой Бадише анилин унд сода фабрик [20] и в настоящее время применяется на химических заводах в Хюльсе. Теплота реакции, необходимая для образования ацетилена, и требуемые температуры достигаются в вольтовой дуге. Несколько позднее также в Людвигсгафене был разработан так называемый способ Саксе, или способ частичного сжигания 121], согласно которому часть конвертируемых углеводородов сжигают в кислороде для обеспечения необходимых температур и теплоты реакции. В обоих способах в качестве побочного продукта образуется сажа. Другой способ получения ацетилена, по процессу Каупера, [c.341]
Синтез ацетилена из метанй (а также из смеси газов, содержащей метан) представляет собой один из примеров органического синтеза в электрическом разряде, осуществленного на практике в значительных масштабах и успешно конкурирующего с обычным, карбидным методом получения ацетилена. Для получения ацетилена из метана применялись различные формы электрического разряда. Так как однако, уже первые исследования показали, что в тихом разряде выход ацетилена ничтожно мал, то все дальнейшие попытки осуществления этой реакции с выходом С2Н2, представляющим практический интерес, в основном были сосредоточены на использовании тлеющего и дугового разрядов. [c.357]
Этот вид печи широко применяется в различных технологических процессах при получении ацетилена из метана и его гомологов, олефинов из природных и заводских газов, бутадиена и циклопепта-диена из средних фракций нефти и т. д. [c.44]
Процесс получения ацетилена из метана в водородной плазменной струе экспериментально изучался на установке, схема которой представлена на рис. 4. Установка состоит из плазмотрона 1, реактора 2, конструктивно объединенного с плазмотроном, закалочной камеры 3, в которой осуществляется закалка при похмощи струй воды, впрыскиваемых перпендикулярно газовому потоку, и газоотделительной камеры 4 с водяным затвором. Из камеры 4 газообразные продукты реакции, отделенные от закалочной воды, подавав-п ейся в избытке, поступали на факел для дожигания. Часть газа отбиралась на анализ. [c.86]
Под термином автозакалка понимается самопроизвольная закалка, происходящая без вмешательства извне либо в ходе самой реакции, либо в ходе процессов, протекающих в реакторе одновременно с ней. Автозакалка (хотя бы частичная) в ходе самой реакции возможна в том случае, когда суммарный тепловой эффект реакции достаточно велик и отрицателен. Автозакалка такого типа происходит, в частности, на начальных стадиях процесса получения ацетилена из метана в плазменной струе (см. стр. 32). [c.167]
В работах [20, 21] получение ацетилена из метана проводилось в аргоновой плазме. Закалка продуктов в первых опытах осуществлялась в темплообменнике. При работе в водородной плазме степень превращения метана в ацетилен на энергетически оптимальном режиме составляет 76%, концентрация ацетилена в продуктах— 15,5 об.%, расход электроэнергии 10,2— 0,7 квт-ч на 1 м" [c.245]
chem21.info
Получение ацетилена из метана - Справочник химика 21
из "Технология нефтехимических производств"
Основной целью термического разложения метана в промышленности является пр-оиззодство ацетилена и сажи. Получение этих продуктов в нефтехимии основано на частичном сжигании метана, прн котором термическое разложение одной части газа происходит зя счет тепла сгорания другой его части (аналогично автотермическому крекингу в нефтяной промышленности). [c.99] В прошлом были попытки провести пиролиз метана и для производства жидких углеводородов и водорода (одновременно с саже )), но эти работы не были осуществлены в промышленном масштабе. [c.99] Рост химической промышленности во всем мире и, в особенности, производство пластических масс стимулируют соответствующее увеличение производства ацетилена. [c.99] Выбор конкретного процесса получения ацетилена зависит от капиталовложений, себестоимости энергетических з.атрат, уровня производительности труда и требует изучения многих факторов. [c.99] В самом деле, в последние 10 лет постоянно проводились исследования и поиски новой технологии как для традиционного метода получения ацетилена (из карбида кальция), так и для процессов, основанных на метане, высших углеводородах и нефтяных фракциях. [c.99] Термодинамика термического разложения метана. Общее представление о термической стабильности метана и его гомологов, по сравнению с термической стабильностью ацетилена, можно получить, рассмотрев зависимость стандартной свободной энергии образования углеводородов из простых веществ, отнесенной к одному атому углерода, от температуры (рис. 33). [c.100] Как было показано (см. введение), метан становится термодинамически неустойчивым (по отношению к составляющим его элементам) при температуре выше 825 °К (552 °С), когда АО = 0. [c.100] Ацетилен термодинамически неустойчив в широком интервале температур (до 3923 °С). Интересно, что величина свободной энергии образования ацетилена и.меет положительные значения до 3923 С и уменьшается с увеличением температуры, в то время как для многих других углеводородов характер этой зависимости обратный (рис. 34). [c.100] Эти зависимости приведены в табл. 19. [c.101] Зависимость теоретических равновесных концентраций метана, ацетилена и водорода от температуры (в интервале 1000—1600 °С) представлена на рис. 35. На этой же диаграмме приведены концентрации ацетилена (гораздо меньшие), полученные в результате экспериментов, причем соотношение экспериментальной и термодинамической констант равновесия очень сильно зависит от рабочих условий. Максимальный выход ацетилена из метана, полученный экспериментально, достигает 17 6, в то время как термодинамически возможен выход 25%. В большинстве промышленных процессов, основанных иа метане, достигнута максимальная концентрация ацетилена 7 —12%. [c.102] Уменьшение давления способствует образованию ацетилена, так как реакция протекает с увеличением числа молей, однако влияние этого фактора на степень конверсии относительно невелико. Поэтому в промышленных условиях часто давление повышают, благодаря чему увеличивается производительность незначительным эффектом некоторого снижения конверсии при этом пренебрегают. [c.102] Оптимальная температура для этого типа реакций 1000—1100 °С. [c.103] Продукты пиролиза метана (например, ацетилен) могут разлагаться до углерода и водорода (табл. 20), поэтому применяют небольшое время контакта и быстрое охлаждение (закалку) реакционной смеси. [c.103] Безусловно, есть и другие возможные реакции (например, С-гНе СН4 + С + Но, для которой АО = О при 79 °С, или СгНц 2С -г ЗНо, для которой Д0° = О при 221 С), но они недостаточно характерны. [c.103] Кинетика пиролиза метана долгое время являлась предметом многочисленных исследований. Большая часть результатов не совпадает, так как применялись различные методы экспериментов (в динамической или статической системах, аналитические и т. д.) и рабочие условия различные материалы и соотношения поверхности и объема реакторов. При изучении опубликованных данных по кинетике пиролиза необходимо учитывать все эти факторы. [c.103] Значения к, рассчитанные по этим соотношениям, характеризуют обш,ую скорость разложения метана в широком интервале температур (900—1600 °С) и при различной степени конверсии. [c.104] В ходе исследований было установлено, что водород служит ингибитором разложения метана. Влияние индукционного периода следующее длительность его Еозрастает с уменьшением соотношения поверхности и объема реактора. Этот факт вероятнее всего связан с зависимостью скорости передачи тепла от соотношения поверхности и. объема реактора. [c.104] При термическом разложении метана образуются, с одной стороны, промежуточные продукты (СзНв, С2Н4, СаНд, СвНе) с малым временем существования и, с другой стороны, углерод и водород. Образование углерода и водорода — результат преимущественно последовательных реакций (разложения промежуточных продуктов) и, в меньшей степени, параллельных реакций разложения метана на элементы. [c.104]Вернуться к основной статье
chem21.info
СПОСОБ ПОЛУЧЕНИЯ АЦЕТИЛЕНА ИЗ МЕТАНА
Изобретение относится к области нефте- и газохимии, а именно к процессам получения ацетилена из метана.
Актуальность разработки новых методов синтеза ацетилена - ценного нефтехимического сырья - вызвана необходимостью вовлечения природного газа в сырьевую базу для нефтехимии, что обусловлено истощением легкодоступных запасов нефти.
Широко известны способы получения ацетилена из метана путем его окислительного пиролиза - процесса горения метана на факеле в условиях недостатка кислорода. Температура процесса при этом составляет 1200-1400°C, время пребывания компонентов в реакционной зоне - несколько миллисекунд. Обязательной стадией процесса является закалка продуктов, которая представляет собой их резкое охлаждение до температуры ниже 300°C путем введения в поток охлаждающей среды воды или масла, что необходимо для предотвращения разложения получаемого ацетилена на углерод и водород (В.Н. Антонов, А.С. Лапидус. Производство ацетилена. М.: Химия, 1970. - 415 с.).
Большинство известных методов повышения эффективности приведенных способов заключаются в оптимизации процесса горения метана путем совершенствования горелок (патент RU 2419599) или реакторных устройств (патент на полезную модель RU 122089).
Общими недостатками данных способов являются низкий выход целевого продукта (ацетилена), а также образование в результате реакции аэрозолей сажи, что создает известные трудности в процессе компримирования и разделения получаемых газообразных продуктов.
Также известны способы осуществления процесса окислительного пиролиза метана, основанные на применении твердых катализаторов при температурах 800-950°C. В качестве катализаторов могут быть использованы оксиды железа, никеля, кадмия, цинка, марганца и серебра, нанесенные на α-Al2O3 (G.E. Keller, M.M. Bhasin / Synthesis of Ethylene via Oxidative Coupling of Methane // Journal of Catalysis. 1982. V. 73. P. 9-19), или системы Bi2O3-MeO, где Me - Mg, Ca, Sr, Ba (a.c. СССР №1216937). Степень превращения метана в таких процессах не превышает 20%, а основными продуктами превращения являются этан и этилен, тогда как ацетилен получается лишь в следовых количествах.
Также известна возможность применения оксидов типа перовскита в качестве катализаторов окисления метана (патент RU 2440292), однако основным направлением превращения метана на катализаторах такого типа является его глубокое окисление с образованием CO2 и h3O.
Наиболее близким к предлагаемому является способ получения ацетилена из метана (патент RU 2409542, прототип), согласно которому ацетилен получают путем пропускания смеси метан-кислород-инертный газ над нагретым катализатором. В качестве катализатора предложено использование обработанного на воздухе при 900-1100°C фехралевого сплава в виде спиралей, лент, стержней и других форм. Нагревание катализатора осуществляют пропусканием через него электрического тока до температур 700-1200°C, а соотношение метан/кислород изменяют в интервале значений 5:1-15:1. Так как газовая смесь подается холодной, проскок части холодного газа приводит к резкому охлаждению продуктов реакции, образовавшихся при контакте с высокотемпературной фехралью, т.е. к закаливанию продуктов окислительного пиролиза и повышению выхода C2+ - углеводородов, в первую очередь, ацетилена. Описываемый способ позволяет получать углеводороды C2+ с максимальным выходом 25,5 мас. % при степени превращения метана 56,4%. Описываемый способ имеет существенные недостатки, главный из которых - образование углерода на поверхности катализатора в процессе окислительного пиролиза. Это приводит к быстрой (в течение нескольких минут) дезактивации катализатора, а также разрушению катализатора в результате углеродной коррозии и невозможности использовать его повторно в каталитическом цикле. Другой недостаток состоит в использовании в качестве сырья воздушно-метановых смесей, которые могут являться взрывоопасными при определенном соотношении компонентов.
Целью данного изобретения является повышение эффективности процесса синтеза ацетилена, а именно: повышение стабильности катализатора и исключение образования углеродных отложений на его поверхности, увеличение выхода ацетилена, а также обеспечение взрывобезопасности процесса.
Для достижения поставленной цели предлагается способ получения ацетилена окислительным пиролизом метана в присутствии кислородсодержащего газа с использованием мембранно-каталитического материала, обладающего одновременно электронной проводимостью и селективной проницаемостью по кислороду.
В качестве мембранно-каталитического материала используют оксиды со структурой перовскита с общей формулой Ba0.5Sr0.5Co0.8-xWxFe0.2O3-δ, где x=0-0,1; δ=0,4-0,6, формованные в виде трубок. Способ реализуется посредством пропускания кислородсодержащего газа по внутреннему пространству трубки, а метана - снаружи трубки, в результате чего происходит диффузия кислорода сквозь стенку трубки из потока кислородсодержащего газа в поток метана. При этом трубка нагревается посредством пропускания через нее электрического тока до температуры 750-1200°C.
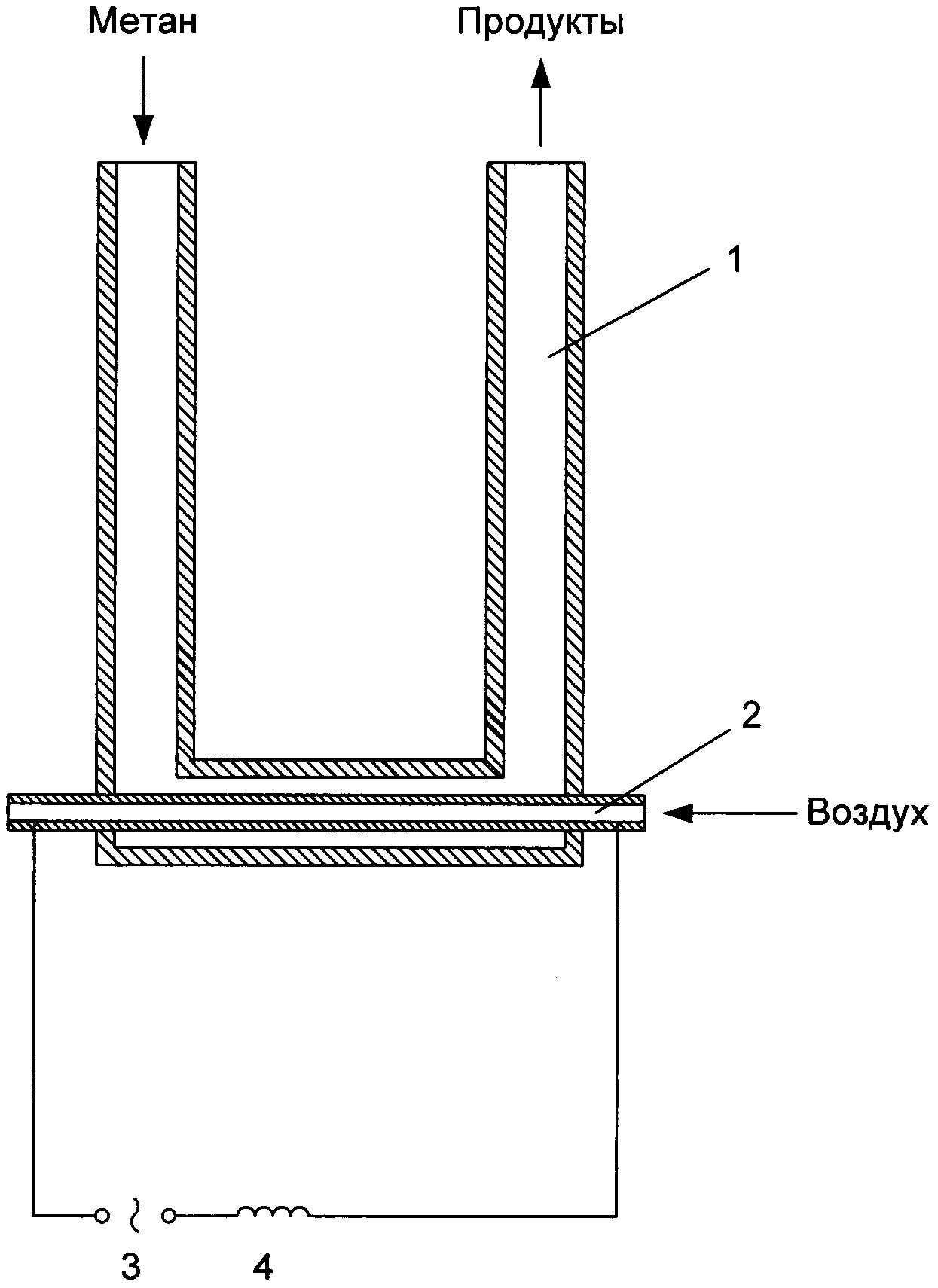
На чертеже представлена схема установки для осуществления способа. Установка состоит из реактора 1, катализатора, формованного в виде трубки 2, источника переменного тока 3 и индуктивного сопротивления 4.
Установка работает следующим образом. Метан подают в реактор 1, в нижней части которого располагается катализатор, формованный в виде трубки 2, во внутреннее пространство которой подается кислородсодержащий газ. Для осуществления нагрева концы трубки катализатора включены в электрическую цепь, состоящую из источника переменного тока 3 и индуктивного сопротивления 4, которое используется для регулирования силы тока.
Процесс проводится при температурах 750-1200°C. Кислород поступает в реактор, диффундируя через стенки трубки катализатора, при этом мгновенно расходуясь. Таким образом предотвращается образование взрывоопасных смесей. Соотношение метан/кислород регулируется посредством изменения расхода соответствующих газов.
Сущность изобретения иллюстрируется следующими примерами.
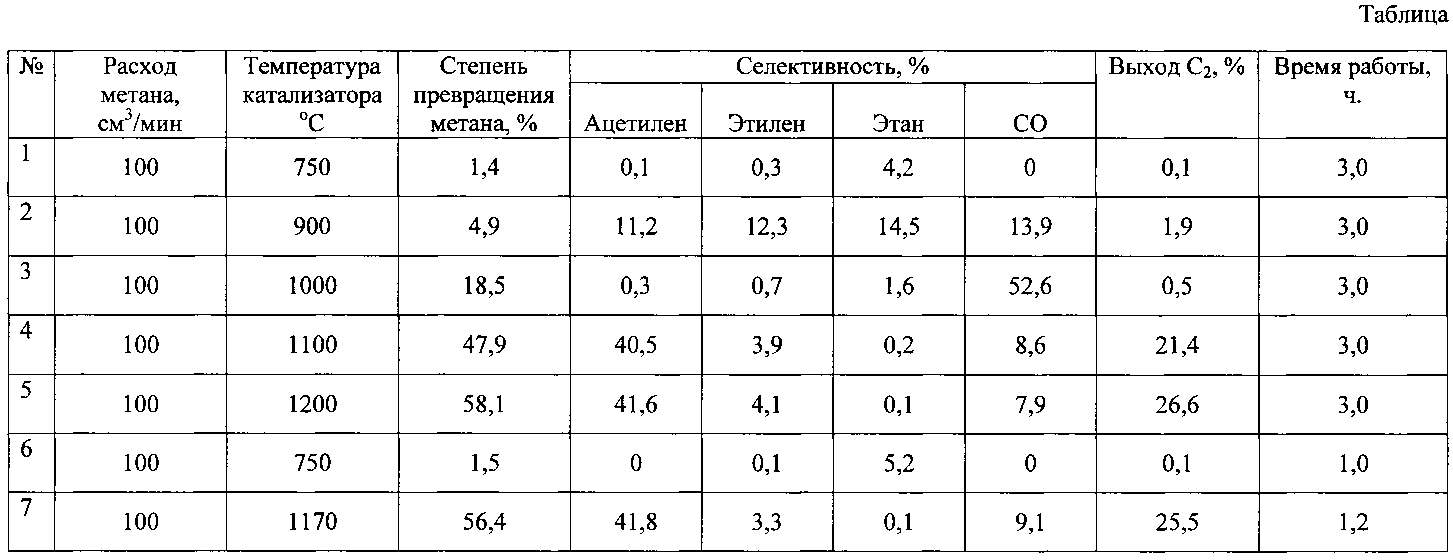
Пример 1. Процесс окислительной конверсии метана проводят в реакторе, изготовленном из кварцевой трубки внутренним диаметром 15 мм. Температура процесса составляет 750°C, метан подают в реактор с расходом 100 см3/мин, воздух подают во внутреннее пространство трубки из перовскита с расходом 33 см3/мин, соотношение метан/кислород составляет 15/1. Состав исходных веществ и газообразных продуктов процесса определяют методом газовой хроматографии. Для этого используется двухканальный хроматограф "Хромос ГХ-1000", оснащенный насадочной колонкой с сорбентом "Poropak-Q" и катарометром, а также капиллярной колонкой HP Pona и пламенно-ионизационным детектором. Количественный состав пробы определяют методом внутреннего стандарта, в качестве которого используют азот воздуха.
Превращение метана ведут в течение трех часов, при этом показатели процесса остаются стабильными.
Пример 2. Аналогичен примеру 1, но температура процесса составляет 900°C. Показатели процесса приведены в таблице.
Пример 3. Аналогичен примеру 1, но температура процесса составляет 1000°C. Показатели процесса приведены в таблице.
Пример 4. Аналогичен примеру 1, но температура процесса составляет 1100°C. Показатели процесса приведены в таблице.
Пример 5. Аналогично примеру 1, но температура процесса составляет 1200°C. Показатели процесса приведены в таблице.
Пример 6 (по прототипу). В качестве катализатора используют спираль из фехралевой проволоки диаметром 0,5 мм. Температура процесса составляет 750°C. Через 1 час работы катализатор покрывается налетом из углеродных отложений, что приводит к падению активности. Показатели процесса приведены в таблице.
Пример 7. Аналогичен примеру 6, но температура процесса составляет 1170°C. Через 1,2 часа работы спираль перегорает из-за воздействия углеродной коррозии. Показатели процесса приведены в таблице.
Как видно из данных таблицы, предлагаемый способ позволяет получать ацетилен с выходом 26,6%, степень превращения метана 58,1%, при этом время стабильной работы катализатора составляет 3 часа и более. Дополнительным преимуществом является возможность разделения потоков кислородсодержащего газа и метана, что снижает взрывоопасность метода.
Таким образом, предлагаемый способ позволяет повысить эффективность процесса синтеза ацетилена из метана по сравнению с существующими способами.
edrid.ru
Способ получения ацетилена из метана
Изобретение относится к способу получения ацетилена окислительным пиролизом метана в присутствии кислородсодержащего газа и катализатора, нагреваемого до температуры 750-1200°C путем пропускания через него электрического тока. Способ характеризуется тем, что в качестве катализатора используют оксиды со структурой перовскита с общей формулой Ba0.5Sr0.5Co0.8-xWxFe0.2O3-δ, где х=0-0,1; δ=0,4-0,6, формованные в виде трубок, метан пропускают снаружи трубки катализатора, а кислородсодержащий газ - внутри трубки катализатора. Использование настоящего изобретения позволяет повысить стабильность катализатора и исключить образование углеродистых отложений на его поверхности, что увеличивает выход ацетилена и обеспечивает взрывобезопасность процесса. 1 табл., 7 пр., 1 ил.
Изобретение относится к области нефте- и газохимии, а именно к процессам получения ацетилена из метана.
Актуальность разработки новых методов синтеза ацетилена - ценного нефтехимического сырья - вызвана необходимостью вовлечения природного газа в сырьевую базу для нефтехимии, что обусловлено истощением легкодоступных запасов нефти.
Широко известны способы получения ацетилена из метана путем его окислительного пиролиза - процесса горения метана на факеле в условиях недостатка кислорода. Температура процесса при этом составляет 1200-1400°C, время пребывания компонентов в реакционной зоне - несколько миллисекунд. Обязательной стадией процесса является закалка продуктов, которая представляет собой их резкое охлаждение до температуры ниже 300°C путем введения в поток охлаждающей среды воды или масла, что необходимо для предотвращения разложения получаемого ацетилена на углерод и водород (В.Н. Антонов, А.С. Лапидус. Производство ацетилена. М.: Химия, 1970. - 415 с.).
Большинство известных методов повышения эффективности приведенных способов заключаются в оптимизации процесса горения метана путем совершенствования горелок (патент RU 2419599) или реакторных устройств (патент на полезную модель RU 122089).
Общими недостатками данных способов являются низкий выход целевого продукта (ацетилена), а также образование в результате реакции аэрозолей сажи, что создает известные трудности в процессе компримирования и разделения получаемых газообразных продуктов.
Также известны способы осуществления процесса окислительного пиролиза метана, основанные на применении твердых катализаторов при температурах 800-950°C. В качестве катализаторов могут быть использованы оксиды железа, никеля, кадмия, цинка, марганца и серебра, нанесенные на α-Al2O3 (G.E. Keller, M.M. Bhasin / Synthesis of Ethylene via Oxidative Coupling of Methane // Journal of Catalysis. 1982. V. 73. P. 9-19), или системы Bi2O3-MeO, где Me - Mg, Ca, Sr, Ba (a.c. СССР №1216937). Степень превращения метана в таких процессах не превышает 20%, а основными продуктами превращения являются этан и этилен, тогда как ацетилен получается лишь в следовых количествах.
Также известна возможность применения оксидов типа перовскита в качестве катализаторов окисления метана (патент RU 2440292), однако основным направлением превращения метана на катализаторах такого типа является его глубокое окисление с образованием CO2 и h3O.
Наиболее близким к предлагаемому является способ получения ацетилена из метана (патент RU 2409542, прототип), согласно которому ацетилен получают путем пропускания смеси метан-кислород-инертный газ над нагретым катализатором. В качестве катализатора предложено использование обработанного на воздухе при 900-1100°C фехралевого сплава в виде спиралей, лент, стержней и других форм. Нагревание катализатора осуществляют пропусканием через него электрического тока до температур 700-1200°C, а соотношение метан/кислород изменяют в интервале значений 5:1-15:1. Так как газовая смесь подается холодной, проскок части холодного газа приводит к резкому охлаждению продуктов реакции, образовавшихся при контакте с высокотемпературной фехралью, т.е. к закаливанию продуктов окислительного пиролиза и повышению выхода C2+ - углеводородов, в первую очередь, ацетилена. Описываемый способ позволяет получать углеводороды C2+ с максимальным выходом 25,5 мас. % при степени превращения метана 56,4%. Описываемый способ имеет существенные недостатки, главный из которых - образование углерода на поверхности катализатора в процессе окислительного пиролиза. Это приводит к быстрой (в течение нескольких минут) дезактивации катализатора, а также разрушению катализатора в результате углеродной коррозии и невозможности использовать его повторно в каталитическом цикле. Другой недостаток состоит в использовании в качестве сырья воздушно-метановых смесей, которые могут являться взрывоопасными при определенном соотношении компонентов.
Целью данного изобретения является повышение эффективности процесса синтеза ацетилена, а именно: повышение стабильности катализатора и исключение образования углеродных отложений на его поверхности, увеличение выхода ацетилена, а также обеспечение взрывобезопасности процесса.
Для достижения поставленной цели предлагается способ получения ацетилена окислительным пиролизом метана в присутствии кислородсодержащего газа с использованием мембранно-каталитического материала, обладающего одновременно электронной проводимостью и селективной проницаемостью по кислороду.
В качестве мембранно-каталитического материала используют оксиды со структурой перовскита с общей формулой Ba0.5Sr0.5Co0.8-xWxFe0.2O3-δ, где x=0-0,1; δ=0,4-0,6, формованные в виде трубок. Способ реализуется посредством пропускания кислородсодержащего газа по внутреннему пространству трубки, а метана - снаружи трубки, в результате чего происходит диффузия кислорода сквозь стенку трубки из потока кислородсодержащего газа в поток метана. При этом трубка нагревается посредством пропускания через нее электрического тока до температуры 750-1200°C.
На чертеже представлена схема установки для осуществления способа. Установка состоит из реактора 1, катализатора, формованного в виде трубки 2, источника переменного тока 3 и индуктивного сопротивления 4.
Установка работает следующим образом. Метан подают в реактор 1, в нижней части которого располагается катализатор, формованный в виде трубки 2, во внутреннее пространство которой подается кислородсодержащий газ. Для осуществления нагрева концы трубки катализатора включены в электрическую цепь, состоящую из источника переменного тока 3 и индуктивного сопротивления 4, которое используется для регулирования силы тока.
Процесс проводится при температурах 750-1200°C. Кислород поступает в реактор, диффундируя через стенки трубки катализатора, при этом мгновенно расходуясь. Таким образом предотвращается образование взрывоопасных смесей. Соотношение метан/кислород регулируется посредством изменения расхода соответствующих газов.
Сущность изобретения иллюстрируется следующими примерами.
Пример 1. Процесс окислительной конверсии метана проводят в реакторе, изготовленном из кварцевой трубки внутренним диаметром 15 мм. Температура процесса составляет 750°C, метан подают в реактор с расходом 100 см3/мин, воздух подают во внутреннее пространство трубки из перовскита с расходом 33 см3/мин, соотношение метан/кислород составляет 15/1. Состав исходных веществ и газообразных продуктов процесса определяют методом газовой хроматографии. Для этого используется двухканальный хроматограф "Хромос ГХ-1000", оснащенный насадочной колонкой с сорбентом "Poropak-Q" и катарометром, а также капиллярной колонкой HP Pona и пламенно-ионизационным детектором. Количественный состав пробы определяют методом внутреннего стандарта, в качестве которого используют азот воздуха.
Превращение метана ведут в течение трех часов, при этом показатели процесса остаются стабильными.
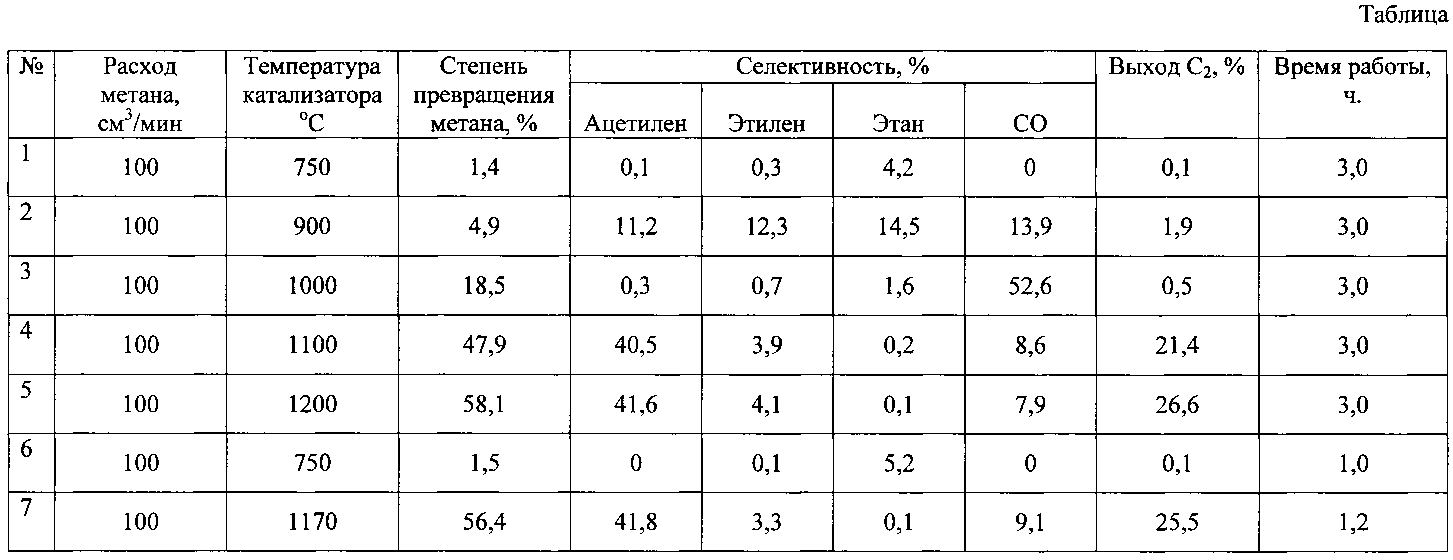
Пример 2. Аналогичен примеру 1, но температура процесса составляет 900°C. Показатели процесса приведены в таблице.
Пример 3. Аналогичен примеру 1, но температура процесса составляет 1000°C. Показатели процесса приведены в таблице.
Пример 4. Аналогичен примеру 1, но температура процесса составляет 1100°C. Показатели процесса приведены в таблице.
Пример 5. Аналогично примеру 1, но температура процесса составляет 1200°C. Показатели процесса приведены в таблице.
Пример 6 (по прототипу). В качестве катализатора используют спираль из фехралевой проволоки диаметром 0,5 мм. Температура процесса составляет 750°C. Через 1 час работы катализатор покрывается налетом из углеродных отложений, что приводит к падению активности. Показатели процесса приведены в таблице.
Пример 7. Аналогичен примеру 6, но температура процесса составляет 1170°C. Через 1,2 часа работы спираль перегорает из-за воздействия углеродной коррозии. Показатели процесса приведены в таблице.
Как видно из данных таблицы, предлагаемый способ позволяет получать ацетилен с выходом 26,6%, степень превращения метана 58,1%, при этом время стабильной работы катализатора составляет 3 часа и более. Дополнительным преимуществом является возможность разделения потоков кислородсодержащего газа и метана, что снижает взрывоопасность метода.
Таким образом, предлагаемый способ позволяет повысить эффективность процесса синтеза ацетилена из метана по сравнению с существующими способами.
Способ получения ацетилена окислительным пиролизом метана в присутствии кислородсодержащего газа и катализатора, нагреваемого до температуры 750-1200°C путем пропускания через него электрического тока, отличающийся тем, что в качестве катализатора используют оксиды со структурой перовскита с общей формулой Ba0.5Sr0.5Co0.8-xWxFe0.2O3-δ, где х=0-0,1; δ=0,4-0,6, формованные в виде трубок, метан пропускают снаружи трубки катализатора, а кислородсодержащий газ - внутри трубки катализатора.
www.findpatent.ru
Ацетилен из метана - Справочник химика 21
Переработкой нефтегазового сырья для получения целевых (конечных) продуктов или сырья для других химических производств занимается нефтехимическая промышленность. Она производит в больших количествах прежде всего углеводородное сырье простейшие парафиновые и этиленовые углеводороды, ацетилен (из метана), циклогексан, бензол. Из этого сырья получают синтетическое горючее, мономеры для пластиков, синтетических каучуков, фенол, ацетон, синтетические спирты, синтетический глицерин, кислоты, хлорпроизводные, нитропарафины. Многие из этих промышленных синтезов будут рассмотрены в дальнейшем. [c.272]
Химическая промышленность потребляет значительные количества пара и тепла. Наибольший расход пара характерен для производства химических волокон (например, на 1 т вискозных волокон расходуется 32 т пара, а на 1 т полиамидных и полиакрилонитрильных волокон — до 55 т тара), синтетического каучука, некоторых видов пластмасс и ряда органических продуктов, та ких, как ацетилен из метана, акрилонитрил, окись этилена и др. [4]. [c.500]Ацетилен из метана и других парафинов образуется по следующим обратимым реакциям [c.112]
Ацетилен из метана Окисление ацетальдегида 17,0 [c.18]
Ацетилен — бесцветный газ со слабым эфирным запахом. Впервые он был получен Э. Дэви в 1836 г. Однако свое название он получил лишь в 1860 г. после работ Вертело, предложившего электродуговой способ получения ацетилена из углерода и водорода. В том же году Велер показал, что карбид кальция, взаимодействуя с водой, дает легкий газ — ацетилен. В дальнейшем термическим крекингом этилена удалось получить незначительное количество ацетилена, а термическим путем был получен ацетилен из метана, этана и этилена. Вильсон в 1892 г. получил патент на производство карбида кальция в электропечи, что положило начало производству ацетилена из карбида кальция [65]. [c.3]
При аналогичных условиях — при температуре вольтовой дуги — можно получить ацетилен из метана, который в пламени вольтовой дуги разлагается на ацетилен и водород [c.90]
Ацетилен получают из метана методом частичного сожжения последнего в токе кислорода. В этом процессе наряду с ацетиленом образуются окись углерода и водород, являющиеся сырьем для синтеза аммиака, метилового спирта и реакции Релена. Отпускная цена на ацетилен зависит от того, какой именно продукт предполагается получать в основном по этому процессу ацетилен или водород. Во всяком случае, процесс частичного сожжения всегда применяют в сочетании с установками, на которых могут быть использованы для химических синтезов другие получающиеся в результате частичного сожжения газообразные продукты. Этот процесс используют в США, Италии и Германии. Даже в США ацетилен из метана составляет всего лишь 10% общего производства ацетилена в этой стране. При этом в США производство ацетилена из метана методом частичного сожжения дислоцируется только в штатах Техас и Луизиана, где условия для этого исключительно благоприятны. [c.406]
Анализом статистики потребления продуктов, проекты производства которых намечено разрабатывать, можно определить, относится ли спрос на них к периоду роста или стабилизации. Для проектируемых производств промежуточных продуктов следует анализировать статистику потребления тех веществ, которые изготовляются из данных полупродуктов, а также возможность их замены другими (например, ацетилена, получаемого из карбида кальция, ацетиленом из метана этилбензола, синтезируемого из бензола и этилена, нефтяным этилбензо-лом нафталина глксияолом и т. д.). [c.39]
chem21.info
Ацетилен производство из метана - Справочник химика 21
Производство карбида кальция термической реакцией между коксом и окисью кальция имеет широкое распространение. Так, в 1965 г. для этих целей потреблялось более 2 500 ООО т кокса во всем мире, из которых, вероятно, от 800 до 900 тыс. т в странах Западной Европы. Но не следует ожидать развития производства карбида кальция в ближайшие годы. Основной областью его применения является производство ацетилена, себестоимость которого по этому методу оценивается во Франции немногим больше 1000 франков/т. Во многих случаях ацетилен может быть заменен этиленом, который более экономичен. Кроме того, для производства ацетилена с карбидным процессом конкурируют другие процессы, принцип которых — пиролиз таких углеводородов, как метан, этап и легкие бензины. Этот пиролиз может происходить при внешнем обогреве, частичном сгорании или под действием электрического тока в форме дуги или разряда. Эти процессы обычно дают смеси ацетилена и этилена, пригодные для использования. Нельзя сказать, что эти процессы были хорошо отработаны и надежны к 1967 г., но можно надеяться, что многие из них позволят получать ацетилен с ценой менее 0,80 франков/кг в связи с этим будет ограничена замена его на этилен. [c.221]
Процесс получения ацетилена методом неполного сжигания, в котором сырьем являются метан из природного газа и 90—95% ный кислород, эксплуатируется в промышленном масштабе в США, Италии, а также в Германии. В этом процессе на каждую весовую часть ацетилена получают не менее 2 весовых частей газа синтеза (00 + На), поэтому описанный процесс применяют там, где одновременно имеется производство синтетического аммиака или синтетического метанола. Такое применение смеси СО и Иг более выгодно, чем использование ее в качестве энергетического топлива. Метод частичного сожжения углеводородного сырья можно рассматривать как вариант метано-кислородного процесса (гл. 3), в котором часть метана превращается в весьма ценный ацетилен. [c.279]
С промышленной точки зрения метан является более перспективным исходным материалом для синтеза цианистого водорода, чем ацетилен. Реакции (1) и (2) весьма эндотермичны, и в случае применения обычного трубчатого реактора интенсивный подвод большого количества тепла для поддержания температуры 1500° представляет в промышленных условиях очень значительные трудности. Выше упоминалось о проведении реакции в электрической дуге как об одном из решений этой проблемы. Вторым решением является сожжение части реагирующих газов внутри реактора. Последний способ был применен при осуществлении реакции (2) и используется сейчас при промышленном производстве цианистого водорода из нефтяного сырья. Этот метод разработан в начале тридцатых годов Андрус-совым [6], который пропускал при 1000° над платиновым катализатором смесь аммиака, кислорода и метана, полученного гидрированием угля или из коксовых газов. В смеси должно находиться достаточное количество кислорода, чтобы могла протекать реакция [c.376]
В то время как получение уксусной кислоты из метана является многостадийным (метан->ацетилен->-уксусный аль-дегид- -уксусная кислота), то окисление бутана в уксусную кислоту сокращает эту стадийность, что дает большой эко комический эффект при производстве многотоннажных веществ. [c.391]
Не умаляя большого практического значения способов получения молекулярного водорода методом конверсии водяным паром и двуокисью углерода и мономолекулярной дегидрогенизацией на активных катализаторах, следует отметить, что способ, связанный с получением водорода в результате полимолекулярных превращений углеводородов в настоящее время представляется все более и более перспективным. Это связано с тем, что водород получают здесь наряду с другими целевыми продуктами, в том числе с такими продуктами крупнотоннажного производства, как термическая сажа, пирографит и др., вместе с ароматическими углеводородами, ацетиленом и Т. д. Основным сырьем для получения водорода по этому способу может служить метан, являющийся главным компонентом природного газа, а также другие газообразные, жидкие и твердые парафиновые углеводороды, входящие в состав нефтей, т. е. все то же природное сырье, проблема рациональной переработки которого еще не решена полностью. Поэтому последнее обстоятельство делает любые работы, связанные с исследованием полимолекулярной дегидрогенизации углеводородов в ходе их поликонденсации при кок-сообразовании, весьма актуальными. [c.164]
Метан, этилен, ацетилен и бензол стали с течением времени основным сырьем органической химии. Особое значение как сырье в середине XIX в. приобрел бензол. В связи с бурным развитием металлургии потребовались значительные количества кокса, при производстве которого в качестве побочного продукта получали каменноугольную смолу, содержащую бензол. Именно в эти годы были открыты многие реакции бензола и его производных. [c.26]
Метан составляет сырьевую основу важнейших химических промышленных процессов получения углерода и водорода, ацетилена, кислородсодержащих органических соединений — спиртов, альдегидов, кислот. Получаемый при термическом разложении метана (реакция 1) мелкодисперсный углерод (газовая сажа) используется как наполнитель при производстве резины, типографских красок. Водород используется в различных синтезах, в том числе в синтезе аммиака. При высокотемпературном крекинге метана (реакция 2) получается ацетилен, необходимая высокая температура (1400—1600 С) создается электрической дугой. Одной из важных областей применения метана является получение так называемого синтез-газа — смеси оксида углерода(П) и водорода (реакции 3 и 4), используемого в дальнейшем для получения многих органических соединений. [c.69]
При возможности использования в качестве дешевого сырья парафиновых углеводородов большего молекулярного веса, чем метан, и при возможности сочетания установки по производству ацетилена с установкой, производящей аммиак и метанол, можно применять процессы пиролиза типа СБА. Объединение установок, производящих и потребляющих ацетилен, с установками для получения аммиака и метанола, ведет при полном использовании промышленных мопщостей к повышению их экономичности. Для создания таких комбинатов требуются очень большие капитальные затраты в течение довольно короткого времени, а также наличие рынков сбыта для всех продуктов. При наличии дешевых парафиновых углеводородов тяжелее метана возможно применение процессов тина процесса Вульфа для производства одного ацетилена (или ацетилена и этилена), не связанного с производством аммиака или другими процессами. Для процесса Вульфа не требуются установки, разделяющие воздух, и, следовательно, отсутствует побочный продукт такого разделения — азот, а выход остаточного газа в результате использования большей его части для обогрева печи и парообразования снижается до минимума. Возможно проведение процесса в таком режиме, когда весь остаточный газ будет расходоваться в самом процессе для обогрева печи, парообразования и для газогенераторного привода компрессоров. Этим обеспечиваются минимальные энергетические затраты и не остается побочных продуктов для использования за пределами установки. Возможно использование установок типа Вульфа или Копперс-Хаше для совместного производства ацетилена и бытового газа. [c.188]
В последние годы в промышленности широко применяется получение ацетилена нри неполном горении метана в кислороде. По технико-экономическим показателям этот процесс является одним из наиболее эффективных процессов получения ацетилена из метана. В Советском Союзе он внедряется на ряде заводов на основе переработки природного газа и последующего использования отходящих газов Для производства аммиака и метанола. Образующийся при неполном окислении метана в кислороде ацетилен является термодинамически неустойчивым он легко разлагается на углерод и водород, а также взаимодействует с углекислотой и водяным паром с образованием окиси углерода и водорода. Схема процесса приводится на рис. V. 2. Сырье (природный газ или метан), не содержащее окиси углерода, водорода и высших углеводородов (так как в противном случае оно преждевременно воспламенится), поступает через подогреватель 1, где нагревается до 600° С, в верхнюю часть реактора 3 (в смесительную камеру горелки), куда подается также подогретый до той же температуры кислород в количестве до 65 объемн. % от метана. В результате процесса горения температура в реакторе 3 поднимается до 1500° С продукты реакции охлаждаются до 80° С орошением водой. [c.148]
Помещения цехов, производств, установок с наличием горючих газов метан, этан, этилен, водород, ацетилен, бутадиен, аммиак, естественный газ и др. [c.84]
Широкое применение в нефтехимической промышленности находят также водород, метан и ацетилен. Большое количество водорода используется при получении аммиака из метана получают метанол, формальдегид и пластмассы ацетилен служит сырьем для производства акрилонитрила, тетрахлорэтана, моновинилацетилена, соответственно даюш,их бутадиен-акрило-нитрильный каучук, неопрен, раз-ати личные растворители и пр. [3 ]. [c.258]
Метан является главной составной частью природного газа-Природный газ — высококалорийное промышленное и бытовое топливо, а также ценное химическое сырье из него получают разнообразные продукты ацетилен, хлорпроизводные, метиловый спирт, муравьиный альдегид и т. д. Применение его в доменном производстве повышает магнитные свойства руд и качество чугуна. Дешевизна, простота транспортировки на далекие расстояния, полнота сгорания, приводящая к оздоровлению воздушных бассейнов, повышают значение природного газа по сравнению с другими видами горючих ископаемых каменным углем, сланцами, торфом. [c.43]
Этилен и пропилен для производства полимеров и сополиме ров должны быть исключительно чистыми, так как примеси (водород, окись углерода, метан, углеводороды С —С5, кислород, ацетилен и вода) ухудшают свойства полимеров и сополимеров. [c.168]
Огромное значение в качестве сырья для пластических масс имеют природные и, в частности, попутные газы. Основную часть природных газов составляет метан, из которого в результате электрокрекинга и окислительного крекинга получают ацетилен, являющийся, в свою очередь, основным сырьем для производства ацетальдегида, уксусной кислоты, уксусного ангидрида и виниловых соединений, например хлористого винила и винилацетата. Другими важными методами переработки метана в сырье для полимеров являются хлорирование, окисление и некоторые другие процессы. [c.12]
Рост производства пластмасс требует расширения сырьевой базы. Мощным источником сырья для производства синтетических материалов становятся нефтепродукты и природные газы. При переработке нефти методами термического и каталитического крекинга получается значительное количество жидких и газообразных веществ, например этилена и пропилена, на основе которых производят полиэтилен и полипропилен. Основную часть природных газов составляет метан, из которого получают ацетилен — сырье для синтеза ацетальдегида, уксусной кислоты, уксусного ангидрида и виниловых мономеров. [c.12]
Оба способа имеют свои преимущества и недостатки. Карбидный ацетилен дорог (на получение карбида кальция расходуется много электроэнергии), но легче поддается очистке. Метан — очень дешевое сырье, однако и его пиролиз требует немалых энергетических затрат, а кроме тоге , в ходе пиролиза образуется сложная смесь веществ, выделить из которой чистый ацетилен нелегко. В настоящее время доля карбидного ацетилена в мировом производстве составляет более половины. [c.309]
Производство ацетилена связано с применением взрывоопасных газов — исходных веществ (метан) и продуктов процесса пиролиза (ацетилен, водород, окись углерода, высшие ацетилены). [c.187]
Применение. Зная свойства метана, можно составить представление о его применении. Оно весьма разнообразно. Благодаря большой теплотворной способности метан в больших количествах расходуется в качестве топлива (в быту и в промышленности). Широко применяются получаемые из него вещества водород, ацетилен, сажа. Он служит исходным сырьем для производства формальдегида, метилового спирта, а также различных синтетических продуктов. [c.318]
Производство ацетилена связано с применением взрывоопасных газов (метан, водород, окись углерода, ацетилен, высшие ацетиленовые углеводороды) и токсичных веществ — газов пиролиза, содержащих окись углерода, растворители ацетилена. [c.84]
После этого газ проходит на установку 8 для выделения ацетилена селективным растворителем. Выделенный ацетилен осушается и направляется на переработку. Газ, содержащий этилен, сжимается и поступает на низкотемпературную установку 9 для выделения этилена. Остающийся газ, обогащенный окисью углерода и водородом, возвращается в качестве топлива в реактор, метан расходуется на производство аммиака, а этилен — на производство ацетальдегида и других продуктов. [c.108]
Органические хлоропродукты составляют подавляющую часть продукции хлорной промышленности. Поэтому ее развитие тесно связано с возникновением и развитием такой прогрессивной области химической технологии, как нефтехимия, а также с увеличением добычи и потребления природных и попутных газов. Эти сравнительно новые отрасли промышленности дают доступное и дешевое органическое сырье в виде газов (метан, ацетилен, этилен, пропилен и другие углеводороды) и жидких органических веществ (бензол, этиловый спирт, керосин и др.), пригодных для переработки в хлоропродукты. Все это определяет высокие темпы развития производства хлора в последние годы в США, Японии, ФРГ, Англии, Франции, Италии и других странах. [c.8]
Продукты эти большей частью вырабатываются в значительных количествах (отсюда и название — тяжелый органический синтез), и для их получения используются чаще всего непрерывные процессы с применением катализаторов нередко реакции протекают при высокой температуре, а иногда и при высоком давлении. В качестве сырья в основном органическом синтезе используют простые по строению веп .ества, преимущественно газы. Это углеводороды жирного ряда парафины (метан и его гомологи), олефины (этилен, пропилен, бутилены) и ацетилен, а также окислы углерода (окись и двуокись), водород, водяной пар. В меньших количествах применяются также ароматические углеводороды и их производные. Все эти вещества получают переработкой нефти, ископаемых углей, природного газа они содержатся в природном и попутном нефтяном га.зе (парафины), газах нефтепереработки (парафины и олефины) и в коксовом газе (этилен, пропилен, метан, водород). Двуокись углерода обычно выделяют из различных газов — отходов других производств. [c.254]
Сырьем для их получения служат водород, окись углерода, метан и его гомологи, этилен, пропилен, н-бутилен, изобутилен, ацетилен, бензол, толуол, нафталин и др., получаемые при переработке жидкого, твердого и газообразного топлив. В производстве синтетических органических продуктов используются процессы окисления и восстановления, гидрирования и дегидрирования, гидратации и дегидратации, сульфирования, нитрования, галоидирования и др. На их основе осуществляется синтез самых различных соединений, служащих сырьем для получения полимеров, синтетических красителей, ядохимикатов, смазочных, моющих, душистых и лекарственных веществ и т. д. Большинство органических процессов протекает в присутствии катализаторов. [c.320]
Большой практический интерес представляет получение ацетилена путем термического разложения углеводородов более тяжелых, чем метан, — пропана, бутана и др. Одновременно с ацетиленом в больших количествах получают этилен — ценное исходное сырье для производства этилового спирта и полиэтилена, широко используемых в производстве синтетических каучуков и других полимеров. Весьма существенно и то обстоятельство, что производство ацетилена из углеводородного сырья поддается автоматизации. [c.9]
Несколько отличаются от описанных технологические схемы на основе отходов производства ацетилена (синтез-газ). Этот газ содержит водород и окись углерода в соотношении, близком к двум,, однако присутствуют до 5,5 объемн. % СН4, 2—3 объемн. % N2, ацетилен и его производные, этилен и соединения азота. Это затрудняет использование газа без предварительной подготовки. Имеется несколько способов переработки синтез-газа в метанол. Обычно его подвергают паро-кислородной, паро-углекислотной или высокотемпературной конверсии. Одновременно с окислением метана конвертируется и большинство присутствующих в газе органических примесей. Существуют схемы, в которых компоненты газовой смеси разделяются на установках глубокого холода или метан выделяется промывкой жидким азотом. После конверсии газ очищает- [c.87]
Сырьем для производства продуктов основного органического синтеза являются водород, окись углерода, углеводороды — метан и его гомологи, этилен, пропилен, п-бутилен и изобутилен, ацетилен, бензол, толуол, ксилолы, нафталин и другие органические сравнительно простые соединения, получаемые при переработке твердого, жидкого и газообразного топлива. [c.196]
Основными недостатками карбидного метода получения ацетилена являются большой расход электроэнергии при производстве карбида кальция и значительное количество потребляемого сырья (известняка и кокса), перерабатываемого в несколько стадий. Достоинство этого метода состоит в получении концентрированного ацетилена, очистка которого от небольших примесей не представляет затруднений. При методах термического расщепления углеводородов используется меньшее количество сырья, которое превращается в ацетилен в одну стадию, но ацетилен получается разбавленным и требуется сложная система его очистки и концентрирования. Однако при этом побочно получаются смеси водорода с метаном или окисью углерода, утилизация которых снижает-себестоимость ацетилена. [c.107]
Метан и кислород подогревают до 600 С в трубчатых печах 1 и 2, обогреваемых газом, соответственно, и поступают в реактор 3. Из реактора пирогаз с температурой после закалки водой 80°С проходит полый, орошаемый водой, скруббер 4 и мокрый электрофильтр 5, в которых из газа осаждаются сажа и смола. Затем пирогаз охлаждается водой в холодильнике непосредственного смешения 6, промывается в форабсорбере 7 небольшим количеством диметилформамида (ДМФА) и поступает в газгольдер 8. Вода, стекающая из реактора 3, скруббера 4 и электрофильтра 5, содержащая сажу, поступает в отстойник 9, из которого водный слой возвращается в реактор для закалки, а собранная сажа с примесью смолы направляется на сжигание. Газ из газгольдера 8 сжимается в компрессоре 10 до давления 1 МПа и подается в абсорбер 11, где из него ДМФА извлекается ацетилен. Непоглощенный газ, состоящий из водорода, метана и оксидов углерода, поступает в скруббер 12, орошаемый водой, в котором из газа улавливается унесенный газом ДМФА. Оставшийся газ используют как топливо или в качестве синтез-газа. Раствор ацетилена в ДМФА из абсорбера 11 проходит дроссель 13, где давление снижается до 0,15 МПа, и поступает в десорбер 14. Десорбированный из раствора ацетилен промывается в скруббере /5 водой и выводится с установки. Основным аппаратом в производстве ацетилена окислительным пиролизом метана является реактор. [c.256]
Метан используется в основном как дешевое топливо. Из него также получают многие ценные химические продукты ацетилен, галогенопроизнодные, метиловый спирт (через синтез-газ, получаемый окислением метана), формальдегид и др. Метан служит для производства такого ценного сырья, как газовая сажа СН4 + 0г —"С + гИзО. [c.58]
Для синтеза хлорпроизводных метана исходят из метана 99%-ной чп-стоты. Метанол получается непосредственно из природного газа, но тщательно очищенного от сероводорода и органической серы [24]. Сероуглерод производится также из природного газа, содержащего преимущественно метан с минимальным количеством углеводородов Сз [24]. Для производства ацетилена окислительным крекингом метана необходимо отделение этого носледиего от и СО. В электрической дуге ацетилен успешно получается из 90—92%-ного метана, а в циклично действующих регенеративных печах Вульфа пиролизу подвергается природный газ без разделения его на фракции [24]. Для получения альдегидов окислением углеводородов также нет необходимости выделять метан из природного газа. Промышленный способ окисления СН4 па фосфатах алюминия и меди проводится на сырье, содержащем 60% СЫ4 [27]. [c.159]
Ацетилен является в настоящее время одним из важнейших сырьевых веществ в промышленности органического синтеза. Наиболее выгодно получать ацетилен из углеводородных газов (электрокрекинг метана и другие способы). При производстве ацетилена путем переработки углеводородных газов его концентрация в получающихся газообразных продуктах (водород, углеводороды и др.) относительно невелика. В то же время ацетилен в отличие от предельных углеводородов хорошо растворяется в воде. Он растворяется в воде примерно в 30 раз лучше, чем метан. Ацетилен очень хорошо растворяется также в диметилформамиде, ацетоне, метаноле, бутирол-актоне и других растворителях. Эти свойства ацетилена и используются сейчас для его выделения из газовых смесей. [c.62]
Универсализм водорода состоит в том, что он может заменить любой вид горючего в различных отраслях производства, в промышленности, на транспорте, в энергетике. Он способен заменить природный газ для бытовых целей, бензин — в двигателях внутреннего сгорания, специальные виды горючих — в ракетных двигателях, ацетилен — в процессах сварки металлов, кокс — в металлургических процессах, метан — в топливных элементах, углеводороды — в ряде микробиологических процессов, углерод — во многих процессах, требующих восстановителя. Водород может быть легко использован и на небольших передвижных или стационарных энергетических установках, в газовых турбинах для генерирования электроэнергии и в крупных топках и печах может и храниться в любых количествах. Его использование в качестве энергоносителя не потребует коренных изменений в современной технологии топливоиспользования. [c.42]
Установлена возможность переработки жидких хлорорганических отходов производств (шнилхлорида, дихлорэтана, эпихлоргид1ина, трихлорэтилена, метиленхлорида, хлорпропана, хлорбензола),а также твердых отходов производства перхлоруглеродов плазмохимическим методом. Часть опытов проведена при разбавлении хлорорганических отходов органическими отходами и углеводородными фракциями. Основными продуктами пиролиза жидких отходов являются ацетилен, хлористыя водород, этилен, метан, водород. [c.11]
Давно известно, что ацетилен присутствует в продуктах неполного сгорания углеводородов, например при проскоке пламени в бунзеновской горелке. Чтобы получить достаточно высокую концентрацию ацетилена в отходящих газах, обычно вместо воздуха применяют кислород, претем сырье и кислород должны быть предварительно подогреты. Определение режима подогрева, а также формы и размеров горелки, необходимое для получения стабильного пламени в промышленных условиях, потребовало. чначительпых исследований, прежде чем процесс был осуществлен фирмой I. G. Farbenindustrie (Германия) во время войны па установке, которая, по существу, являлась укрупненной пилотной установкой. Прошло еще десять лет прежде чем были пущены первые промышленные установки (в 1953 г.). В последнее десятилетие процесс быстро распространился, заводы появились в нескольких странах, причем были использованы различные модификации первоначально разработанного метода. К 1962 г. около 350 ООО т ацетилена, т. е. около одной седьмой его мирового производства, получали методом окислительного пиролиза, потребляя при этом 1,5 млн. т кислорода. Недавно было высказано предположение [1], что процесс пиролиза начинается по окончании процесса горения. Хотя это утверждение справедливо только приближенно (стр. 396), оно позволяет точно предсказывать результаты процесса. Поскольку кинетика пиролиза уже была рассмотрена (стр. 334), ниже обсуждается только кинетика стадии горения. Энергия активации для смесей, богатых метаном, составляет 62 ккал/молъ. Механизм горения был предложен Норришем [3] [c.380]
Углеводородные газы (метан, зтан, пропан, бутан, этилен, ацетилен) находят применение при производстве пластмасс, синтетических каучуков, химических волокон и т.д. Водород, хлористый водород, оксид углерода и другие широко используются при получении продуктов органического синтеза. Аммиак применяется в холодильной технике, при производстве удобрений и т.д. [c.280]
В настоящее время сырьем для производства ацетилена служит также метан. Из всех углеводородов метан наиболее терми-ческистойкий. Превращение его в ацетилен начинается при температурах выше 700°С и лишь при температурах 1400—1500 С выход достигает эффективных значений. Более высокие температуры ускоряют процесс распада метана на элементы. Необходимым условием для конверсии углеводородов до ацетилена является проведение процесса при высоких температурах, низком парциальном давлении сырья и конечного продукта, коротком времени контактирования и резком охлаждении (закалке) образующейся газовой смеси- Из уравнения распада метана видно, что реакция протекает с увеличение.м объема [c.269]
chem21.info
Способ получения ацетилена из метана и других газообразных углеводородов
№ 143377
Класс 124, 4
12о, 19з, сссо
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
К АВТОРСКОМУ СВИДЕ1 ЕЛЬСТВУ
Подггисные группы A 48 и 50
П. П. Карпухин и Л. И. Сломинский
СПОСОБ ПОЛУЧЕНИЯ АЦЕТИЛЕНА ИЗ МЕТАНА И ДРУГИХ
ГАЗООБРАЗНЫХ УГЛЕВОДОРОДОВ
Заявлено 22 февраля 1960 г. за ¹ 665844123 в Комитет ио «елам изобретений и открытий при Совете Миниегров С(СР
Опубликовано в «Бюллетене изобретений» № 24 за 1961
Известен способ получения ацетилена из метана в электрическом разряде под вакуумом с использованием высокотемпературного дугового разряда (1600 — 1800 ) и без применения в разрядном контуре конденсаторов и дросселей. При этом наряду с образованием ацетилена происходит распад его и распад метана и протекает ряд побочны., реакций, преимущественно реакций, ведущих к образованию сажи.
Выделение сажи в разрядной зоне существенно затрудняет работу и усложняет технологию производства ацетилена.
Известна также модификация электрокрекинга природных углеводородных газов, основанная на применении тихого электрического разряда при низкой температуре. Однако по этому способу за один проход через реактор происходит лишь незначительное превращение метана н ацетилен, сопровождаемое значительным выделением сажи. В связи с этим, такой процесс проводят в серии последовательно установленныA реакторов, работающих по указанному способу.
В промышленном масштабе (СССР, Румыния, ФРГ) реализован способ получения ацетилена из метана при давлениях выгпе атмосферного (около 1,5 ат) .
Предложенный новый способ получения ацетилена из метана и други, газообразных углеводородов в электрическом разряде переменного тока при низкой температуре до 500 обладает рядом преимуществ перед вышеописанными способами и заключается в том, что, - ц!.лыо получения газа с большим процентом ацетилена, не содержащего сажи, процесс проводят при атмосферном давлении в зоне электрического разряда, в котором фазовые изменения тока сглаживаются путем включения параллельно к разрядному промежутку емкости, а напряжение увеличивается за счет создания контура резонанса напряжений, л Ъ )43377
В предложенной схеме (см чертеж) благодаря установке в азрядном контуре Жответствующей емкости и индуктивного сопротивления создаются условия для получения в газовой зоне электронов с высокой энеpãèãé, что увсличиваеТ направленность реакции получения ацетилена, снижает температ)у1эу процесса и уменьшает сажеобразование. Это г)овышает вь)ход,.ацдцлсна и упрощает тсхнологичсску)О схему eio иолучения.
l1 р и м с р. В стеклянный реактор i¹ 1, снабженный двумя электродами, из которых один представляет собой металлический стержс)b Я второй трубку, присоединенную к ловушке, через боковые штуцеры А-А, подают тангенциально к боковой поверхности газ, содержащий метан и другие углеводороды. Одновременно на электроды подают ток высокоп) напряжения о1 трансформатора ¹ 2. После возникновения газового разряда на электродах создается напряжение 10000 — -!6 000 в. Заданную разность потенциалов поддерживают при помощи находящихся в разрядном ко)пурс дpocccля № 3 и конденсаторов № 4 за счет которых
1 сглаживаются также фазовыс колебания тока. Расстояние между э.тс)
При этом получают смесь газов, содержащу)о до 15 — 18% ацетилена; выход ацетилена 50 — 70% от теоретически возможного.
В составе получаемого газа содер>кится 50 — -65% водорода и () I
17 до 35% непрореагировавшсго метана, 1хупрен образ) ется в количестве около 3% от полученного ян(гн лена.
Прсдмет изобретения посоо получения ацетилена из метана и дру>гих газообразных углеводородов в электрическом ря: ряде переменного тока при низкой температуре, о т л и ч а ю щ и и ся тем, что, с целью получения ) язя с Оольшим процснтом яцстилсна, II(. Содержащего сН>КН, процесс и >Оводят при атмосферном давлении в зоне электрического разряда в ко7 тором фязовъ)е изм 11(. ния Iокя сгля>1
Дс л /в о ср Nl
= /)сну(.с.с
Гжссчст (и(


www.findpatent.ru
- Стабилизатор понижающий напряжения
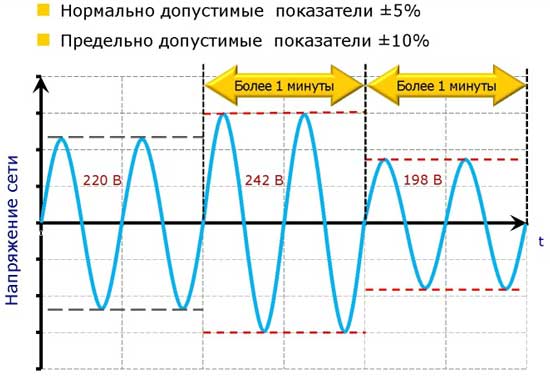
- Mma расшифровка

- Расшифровка mma

- Стабилизатор напряжения для котла отопления

- Бензогенератор как выбрать

- Сервоприводный стабилизатор напряжения

- Ацетилен газообразный технический

- Температура плавления кислорода
- Температура плавления кислорода
- Пищит бесперебойник

- Пищит бесперебойник