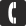Справочник химика 21. Азот вода
Публикации компании "Гидрология"
Добавлено: 28.03.2014
Каждый владелец искусственного водоёма, населённого рыбой, желает, чтобы он был максимально похож на естественный, но при этом вода в искусственном пруду была прозрачной, высшие водные растения вокруг росли нормально, а водоросли, наоборот, чтобы сильно не развивались, рыба была здоровой. Поэтому основная задача каждого владельца искусственного водоёма, чтобы пруд выглядел замечательно – добиться баланса замкнутой экосистемы водоёма.
Почему нарушается баланс азота в искусственном водоёме??
В воду искусственного пруда постоянно попадает корм и продукты жизнедеятельности рыб. В процессе разложения этих остатков в воде образуется большое количество фосфора (P) и азота (N) в виде аммиака (Nh4). Аммиак, в процессе окисления кислородом, преобразуется в нитрат (NO3). Фосфор и нитрат – это питательные вещества для растений. Правильное планирование искусственного водоёма позволяет удерживать количество нитратов и фосфатов в воде близким к нулю – и ваш искусственный водоём чувствует себя хорошо. Неправильное планирование приводит к сбою баланса и неспособности экосистемы искусственного пруда перерабатывать все поступающие питательные вещества. Происходит накопление их избытка и как следствие – неконтролируемый рост водорослей.
Эта опасность грозит любому виду искусственного водоёма – плавательному водоёму, декоративному водоёму, живому бассейну, садовому аквариуму, - неправильно спланированному и неправильно «настроенному» с точки зрения биологического баланса.
Азот.
Азот – важнейший элемент живой природы, поэтому важно правильно «настроить» его круговорот в любом искусственном водоёме.
Азот содержится в молекулах белка, пептидах, аминокислотах, в хлорофилле, в рибонуклеиновых кислотах, витаминах. Азот очень важен для жизни - без азота невозможен фотосинтез, образование хлорофилла, белка и продолжение рода. Азот в атмосфере находится в виде газа. Молекула азота состоит из двух атомов азота (N2) очень сильно связанных друг с другом. Редкие живые организмы имеют «механизм», позволяющий разорвать эту связь, поэтому газообразный азот, даже растворённый в воде не участвует в обороте питательных веществ. Вместо этого весь азот входит в оборот веществ в виде аммиака (Nh4).
Откуда азот берётся в воде искусственного водоёма?
Рыбы, поедая корм, загрязняют водоём экскрементами. 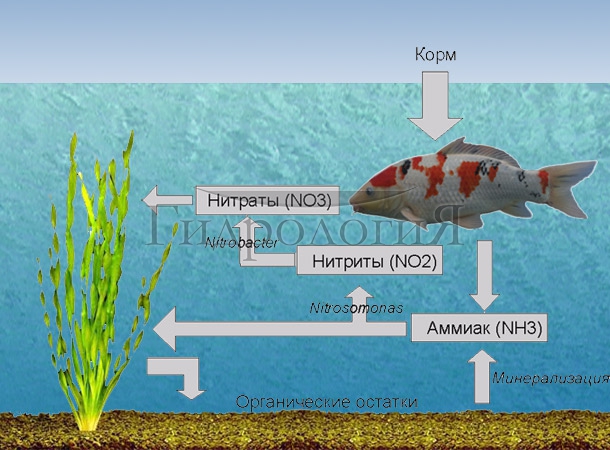 Растения обновляются, какие-то части их отмирают. В остатках корма, в продуктах жизнедеятельности рыб, в гниющих тканях растений, в прочих разлагающихся органических отложениях есть белок. Всё что содержит белок, содержит и азот. Бактерии минерализуют (минерализация это разрушение органической субстанции до неорганических веществ) все перечисленные органические остатки, в результате из белка получается аммиак (Nh4), который далее окисляется до аммония (Nh5+). Также, аммиак производится рыбами и выделяется в воду через их жабры, производится грибками и бактериями. Вообще аммиак это побочный продукт биологических процессов всех организмов. Азот в виде аммиака попадает в водоём и начинается процесс, который можно назвать «круговорот азота в природе» или азотный цикл.
Растения обновляются, какие-то части их отмирают. В остатках корма, в продуктах жизнедеятельности рыб, в гниющих тканях растений, в прочих разлагающихся органических отложениях есть белок. Всё что содержит белок, содержит и азот. Бактерии минерализуют (минерализация это разрушение органической субстанции до неорганических веществ) все перечисленные органические остатки, в результате из белка получается аммиак (Nh4), который далее окисляется до аммония (Nh5+). Также, аммиак производится рыбами и выделяется в воду через их жабры, производится грибками и бактериями. Вообще аммиак это побочный продукт биологических процессов всех организмов. Азот в виде аммиака попадает в водоём и начинается процесс, который можно назвать «круговорот азота в природе» или азотный цикл.
Круговорот азота в природе.
Круговорот азота состоит из двух частей – нитрификации и денитрификации.
Нитрификацией называется процесс, при котором аммиак (Nh4) преобразуется в нитрит (NO2), а нитрит преобразуется в нитрат (NO3).
Денитрификацией называется процесс, при котором нитрат (NO3) преобразуется в нитрит (NO2), а нитрит преобразуется в азот (N2).
Эти процессы в основном происходят в грунте искусственного водоёма.
Нитрификац ия.
ия.
Находящиеся в водоёме нитрифицирующие бактерии окисляют аммоний до нитрита, в результате реакции помимо нитрита получается водород и вода и выделяется энергия. Эту энергию бактерии используют для своей жизнедеятельности. Полученный нитрит другие нитрифицирующие бактерии окисляют до менее токсичного нитрата. Оба процесса проходят в водной среде и в верхних слоях грунта, для обоих процессов нужно, чтобы в воде было большое количество кислорода. По этой причине нитрификация – это так называемый аэробный процесс.
Большинство получившегося нитрата потребляется растениями для своего роста, часть выводится с ежедневными подменами воды, а часть участвует во втором процесс – денитрификации.
Денитрификация.
Денитрификация – это процесс анаэробный, проходящий без потребления кислорода. Если нитрификация проходит в воде и в верхних слоях грунта, то денитрификация проходит в нижних слоях грунта водоёма, куда не попадает кислород. Одни микроорганизмы, находящиеся в грунте, преобразуют нитрат (NO3), полученный в процессе нитрификации, в нитрит (NO2). Другие, находящиеся в грунте микроорганизмы – денитрифицирующие, преобразуют нитриты в газообразный азот (N2), который покидает водоём. И те и другие бактерии в этих процессах получают из соединений азота кислород для своей жизнедеятельности.
Баланс разных культур бактерий в грунте.
В грунте живут культуры множества бактерий. Есть бактерии анаэробные, а есть те, что в зависимости от содержания кислорода в воде становятся  или аэробными, или анаэробными. Аэробные бактерии не только поставляют нитрат для анаэробных, но и благодаря большому потреблению кислорода создают умеренноанаэробные условия. Возникает взаимновыгодный обмен между двумя типами бактерий живущих в нескольких сантиметрах верхнего слоя грунта (поэтому беспокоить субстрат в водоёме чисткой грунта водным «пылесосом» крайне нежелательно). Анаэробные бактерии разлагают нитрат до газообразного оксида азота [NO] - безвредного газа. Он растворяется в воде и выветривается в атмосферу, завершая круговорот азота.
или аэробными, или анаэробными. Аэробные бактерии не только поставляют нитрат для анаэробных, но и благодаря большому потреблению кислорода создают умеренноанаэробные условия. Возникает взаимновыгодный обмен между двумя типами бактерий живущих в нескольких сантиметрах верхнего слоя грунта (поэтому беспокоить субстрат в водоёме чисткой грунта водным «пылесосом» крайне нежелательно). Анаэробные бактерии разлагают нитрат до газообразного оксида азота [NO] - безвредного газа. Он растворяется в воде и выветривается в атмосферу, завершая круговорот азота.
Часть нитрата превращается анаэробными бактериями обратно в нитрит и аммоний. Если азот в этом случае не будет употреблен корнями растений, он превращается бактериями в газ азот [N2], химически инертный и безвредный, который растворяется в воде и выветривантся обратно в атмосферу. Со временем процессы выравниваются, и денитрификация протекает одновременно с нитрификацией в грунте в анаэробных зонах.
Важно!
Корни водных растений способны доставлять кислород в грунт, уничтожая анаэробные зоны. В субстрате из крупного гравия вообще не будет анаэробных условий. В субстрате, составленном из гравия разного размера вероятнее всего будут образовываться локальные бескислородные зоны, в которых возможно протекание денитрификации.
Конкуренция за аммоний.
Лабораторные тесты показали, что растения и водоросли НЕ потребляют нитрат в заметных количествах пока есть аммоний. Не стоит беспокоиться о полной нитрификации потому что в водоёме с большим количеством растений, любая дополнительная конкуренция за азот (в составе аммония) будет ухудшать рост растений. Слишком активное преобразование бактериями аммония [Nh5+] в нитрит [NO2] отнимает основной источник азота для питания растений.
Влияние уровня pH воды на круговорот азота.
Уровень pH играет решающую роль в нитрификации: интенсивнее этот процесс протекает при pH более 7,2 и достигает своего максимума при pH=8,3. При pH менее 7,0 интенсивность нитрификации составляет 50%, при pH=6,5 только 30%. Таким образом в водоёме в котором pH=6.8-7.2 создаются благоприятные условия для потребления аммония [Nh5+] именно растениями, а не нитрифицирующими бактериями в грунте и фильтре.
Нитрифицирующие бактерии плохо конкурируют за кислород с бактериями разлагающими органику в грунте - теми, что образуют "биологическую потребность в кислороде", что еще больше увеличивает шансы растений употребить весь доступный аммиак [Nh4] раньше нитрифицирующих бактерий.
В искусственном водоёме с большим количеством растений при pH=6.8-7.2 почти весь образовавшийся аммоний будет потреблен растениями до того, как его успеют переработать нитрифицирующие бактерии. Этим растения способствуют снижению уровня нитратов. Позднее при подрезке растений азот (нитраты) выведется из водоёма.
Вред, наносимый аммиаком.
Аммиак (Nh4) ОЧЕНЬ токсичен для рыб, уже при содержании аммиака всего около 0,05% у рыб возникает хроническое поражение жабр. Со временем оно становится необратимым. Поэтому важно, чтобы как можно быстрее попавший в воду аммиак преобразовался бактериями во много раз менее токсичное соединение – аммоний (Nh5).
Процесс преобразования аммиака в аммоний зависит от pH фактора воды. С падением pH все больше аммиака превращается в нетоксичный аммоний, например, при понижении pH на один градус токсичного аммиака становится в десять раз меньше. При pH=7.0 аммиака примерно 0,33%, при pH=6.0 - только 0,03%.
На деятельность нитрифицирующих бактерий, которые окисляют аммиак, также влияют температура воды и концентрация в воде кислорода.
Чем выше температура - тем больше доля токсичного аммиака. При 28 градусах в воде содержится вдвое больше токсичного аммиака, чем при 20 градусах (при равном pH).
Нитрифицирующие бактерии требуют много кислорода. Для протекания нитрификации содержание кислорода в воде должно быть не менее 1 мг/л.
Оценка количества, попадающего в воду, азота.
Белки в среднем содержат 16% Азота. Чтобы посчитать сколько Азота вы вносите в аквариум с кормом для рыб, посмотрите содержание белка в корме, посчитайте его массу и умножьте на 0,16. Вы получите количество азота в данном корме. Например, если на банке корма массой 1 кг. написано, что в корме содержится 48% белка, это значит, что в данной банке 1000 х 0,48 = 480 грамм белка, который содержит 16% азота, т. е. - 480 х 0,16 = 76,8 грамм азота.
Плюс к этому азот, получаемый из продуктов жизнедеятельности рыб и от гниющих остатков растений.
При неправильном планировании искусственного водоёма биологические процессы не нормализуются, и поступивший в пруд азот начинает потребляться водорослями. При этом, из 1 грамма азота получается до 3-х килограммов биологической массы. Ваш искусственный водоём быстро превращается в болото!
Подводя итоги.
Для того чтобы процессы в Вашем водоёме нормализовались быстрее необходимо учесть и провести следующие действия:
- запланировать достаточную зону регенерации – площадь зоны должна соответствовать площади открытой воды для купания
- при засыпке зоны регенерации использовать грунт разных фракций, для создания условий нормального существования анаэробных бактерий
- засадить зону регенерации достаточным количеством высших водных растений
- внести в воду комплекс прудовых бактерий
- создать условия для нормальной аэрации воды – фонтаны, аэраторы, циркуляция воды – ручьи, каскады
- не производить механическую очистку дна водоёма, чтобы не нарушить условия существования анаэробных бактерий
- вовремя осуществлять подрезку высших водных растений
- не добавлять в водоём химические вещества, применяемые для очистки воды в бассейнах.
- следить за pH фактором воды.


Ознакомьтесь также:
«Плавательный водоём: определение, состав, планирование, строительство»
«Растения в искусственном водоёме и вокруг него»
gidrologia.ru
Азот и вода - Справочник химика 21
Сырьем для производства аммиака является смесь азота и водо рода. Эту смесь получают разными способами. Наиболее распространенные из них газификация твердого и жидкого топлив с последующей конверсией окиси углерода, конверсия метана и других углеводородных газов, комплексная переработка природного газа в ацетилен и синтез-газ, фракционное разделение горючих газов, в частности коксового, методом глубокого охлаждения, разделение воздуха на азот и кислород с применением для этого глубокого холода и электрохимический способ получения водорода и кислорода. [c.151]
Какое количество электронных пар принимает участие Б образовании молекул брома, кислорода, азота и воды [c.68]Промышленные производства нитрата аммония полагались на исключении исходных веществ, возможности получения которых очень ограничены (аммиак с газового завода, натриевая селитра), и замене их основными исходными веществами, запасы которых практически неограничены (кислород, азот и вода), а также на нахождении такого решения, при котором используется теплота, выделяющаяся при проведении экзотермической реакции взаимодействия аммиака с азотной кислотой, для упаривания раствора нитрата аммония. [c.53]
При термическом разложении бихромата аммония образуется оксид хрома(III), выделяется азот и вода [c.93]
При взаимодействии олова с азотной кислотой образуются оловянная кислота, двуокись азота и вода. Написать уравнение реакции. [c.113]
Решение. Принимаем следующие упрощения 1) содержание примесей в расчете опускается 2) летучие части содержат только углерод (пренебрегаем содержанием водорода, кислорода, азота и воды в угле) 3) воздух состоит [c.124]
Обслуживающий персонал должен знать, что при истечении газов через неплотности в аппаратах и трубопроводах необходимо немедленно отключить поврежденные участки, чтобы предотвратить загорание и взрыв газа. В случае загорания газа, вытекающего в помещение через поврежденные трубопроводы и различного рода неплотности, запрещается сбивать пламя любыми средствами и способами, в том числе паром, двуокисью углерода, азотом и водой. [c.108]
В присутствии катализатора окисляется до оксида азота и воды [c.157]
Полное исключение токсичных выбросов возможно на установках каталитической очистки, когда в присутствии газа-восстановителя (водорода, природного газа и др.) происходит восстановление окислов азота до азота и воды, не загрязняющих атмосферу. При этом степень очистки составляет 98%. [c.211]
Формула (7.57) получена аналитически и откорректирована по экспериментальным данным при пленочном кипении углеводородов, азота и воды. [c.236]
При сгорании некоторого веш,ества в кислороде образуются углекислый газ, азот и вода. О присутствии каких химических элементов в веществе свидетельствует этот факт [c.8]
Почему хлорид и фосфат аммония прн нагревании разлагаются с образованием аммиака и соответствующей кислоты, а нитрат аммония — с образованием закиси азота и воды [c.74]
Запись данных опыта. Написать уравнение реакции разложения, учитывая, что одновременно образуются азот и вода. Указать окислитель и восстановитель. К какому типу окислительновосстановительных реакций относится данная реакция [c.230]
Дихромат аммония при нагревании до 200 С разлагается с образованием оксида хрома (III), азота и воды. Составьте уравнение этой реакции и укажите, к какому типу превращений она относится. [c.126]
Все платиновые металлы во многом сходны между собой. Это — благородные металлы, малораспространенные в природе. Встречаются только в самородном состоянии. Химически очень стойки. На воздухе и во влажных средах не тускнеют и не корродируют. Кислоты (НС1, НзЗО на них не действуют. Большинство платиновых металлов не растворяется даже в царской водке только платина в ней растворяется, а палладий растворим также и в НЫОз-Как и все металлы УИ1 группы, платина и ее аналоги — комплексообразователи и активные катализаторы. Как правило, они проявляют способность поглощать значительные количества газообразных На и Оа, переводя последние в химически активное состояние. Эта способность особенно сильно проявляется именно у платиновых металлов. Указанное явление носит название окклюзии-, оно имеет большое значение для катализации процессов гидрогенизации (присоединения водорода) или окисления. Так, например, Ре, Ки и Оз энергично катализируют процесс синтеза ЫНз чз азота и водо- [c.553]
При растворении свинца в концентрированной азотной кислоте образуются нитрат свинца, двуокись азота и вода. Написать уравнение реакции. [c.113]
Осмий в виде порошка взаимодействует с концентрированной дымящей азотной кислотой, образуя 0504, двуокись азота и воду. Написать уравнение реакции. [c.114]
При взаимодействии металлического магния с разбавленной азотной кислотой образуются нитрат магния, закись азота и вода. Написать уравнение. [c.59]
Амины на воздухе горят с выделением оксида угле- рода (IV), азота и воды, например [c.253]
Физические свойства. Азот — газ без цвета, запаха и вкуса, легче воздуха. Растворимость в воде меньше, чем у кислорода при 20°С в 1 л воды растворяется 15,4 мл азота (кислорода 31 мл). Поэтому в воздухе, растворенном в воде, содержание кислорода по отношению к азоту больше, чем в атмосфере. Малая растворимость азота в воде, а также его очень низкая температура кипения объясняются весьма слабыми межмолекулярными взаимодействиями как между молекулами азота и воды, так и между молекулами азота. [c.188]
Горение аммиака при обычных условиях приводит к образованию молекулярного азота и воды [c.81]
Малая растворимость азота в воде, а также его очень низкая температура кипення объясняются весьма слабыми межмолекулярными силами как между молекулами азота и воды, так и между молекулами азота. [c.105]
Определите, в какую сторону смещается равновесие реакции между двуокисью азота и водой при изменении температуры. [c.54]
Удельная поверхность окиси алюминия под действием температур в результате постепенного спекания мелких жается со 160—330 м /г свежего катализатора до 80—100 Количество перерабатываемого сырья на 1 кг катализа" ,ц ставляет от 70 до 200 м и более. Современные катализато Р со-форминга, содержащие рений, выдерживают многократнук Д ри-600 раз и более) регенерацию. Значительно менее требов З— к содержанию в сырье серы, азота и воды катализаторы, з 1>ны рых платина введена в цеолит. Катализаторы риформинга пр Т о рируют осушенными дымовыми газами, содержащими 0,5-- о/ Не лорода. Выгорание кокса происходит при равных условиях > цс ростью, значителшо большей (до двух порядков), чем при пр Но рации алюмосиликатов, так как платина является активнь Че [c.255]
Аммиак сгорает в кислороде и в воздухе (предварительно подогретом) с образованием азота и воды [c.191]
Амины горят на воздухе с выделением оксидам углерода (IV), азота и воды, например [c.241]
Наряду с жидкими и газообразными окислителями для очистки сточных вод применяются и твердые оксиды и гидроксиды металлов переменной валентности (никеля, кобальта, меди, железа, марганца). Гидроксид никеля высшей валентности легко окисляет тидразингидрат, спирты, альдегиды, алифатические и ароматические амины. Продуктами окисления являются в основном карбонаты, азот и вода. Метод рекомендуется для обезвреживания сточных вод с концентрацией токсичных соединений до 0,5 г/л, что является его недостатком. [c.494]
Как получить Nh5NO3, воспользовавшись в качестве исходных веществ атмосферным азотом и водой [c.231]
Реактор для производства концентрированной азотной кислоты из жидких окислов азота. Жидкие окислы азота и воду перемешивают с газообразным кислородом под давлением. Азотная кислота образуется по следуюпцей экзотермической реакции [c.172]
Реакции окисления—типичные высокоэкзотермические реакции — могут привести к выходу либо очень стабильных продуктов (например, превращение аммиака в азот и воду), либо промежуточных продуктов — селективное окисление (например, превращение аммиака в окислы азота, метана в формальдегид и пропилена в акролеин). [c.14]
При определенных условиях подачи тока на электродах электролизера возникают пузырьки газа, обеспечивающие реализацию электрофлотации, так, нахгример, если ввести в воду безбалластный реагент — нитрат аммония — в электролизере произойдет его разложение на азот и воду, что увеличивает количество флотирующего агента и интенсифицирует процесс (табл. 1.3). [c.17]
Установите формулу некоторого водородного соеди-иення азота, если при сжигании его образуются азот и вода в весовом отнощении соответственно 7 9. 320 мл паров исходного вещества при давлении 1 атм и температуре 117°С весят 0,32 г. [c.39]
Этот метод и до сих пор применяется на станциях малой мощности. Однако при сульфитной обработке воды повышается солесодержание, что недопустимо на электростанциях, работающих при высоком давлении пара. На таких станциях кислород удаляют при помощи гидразина ЫгН4,являющегося сильным восстановителем. При взаимодействии гидразина с кислородом образуются азот и вода по уравнению реакции [c.346]
Платина растворяется в царской водке (смесь кислот азотной и соляной). Образуются гексахлороплатиновая кислота, в которой окислительное число платины равно +6, окись азота и вода. Написать уравнение реакции. [c.114]
Поскольку азот в аммиаке имеет низшую степень окисления (—3), то последний проявляет восстановительные свойства. Так, аммиак реагирует с кислородом с образованием азота и воды 4Nh4 + 30, = 2Mj + 6H,0 [c.108]
Решая систему уравнений (а), (б) и (в), находим, что п(К)= 2 моль, п(П) = 4 моль, п(0) = 2 моль, т.е. формула соединения N211402 или Nh5N02. При нагревании этой соли образуются азот и вода [c.144]
Наконец, в пятую пробирку внести 6—8 капель концентрированной азотной кислоты (пл. 1.4). Наблюдать выпадение белого осадка. Написать уравнение реакции с учетом образования р-оло-вяной кислоты НзЗпОз, двуокиси азота и воды. [c.223]
Нитриты разрушают при осторожном нагревании их насыщенных растворов с твердым Nh5 I или (Nh5) .S04. При этом нон N0 реагирует с ионом NH.I, образуя свободный азот и воду [c.259]
chem21.info
Азотные ванны - Симптомы и лечение народными средствами в домашних условиях
Долгое время считалось, что наличие азота в минеральных водах ни как не влияет на человека, потому что азот – это индифферентный газ. Однако, проведенные исследования доказали, что это не так: действие азота в водной среде существенно отличается от такового в воздушной. Азот в экспериментах меняли на другие газы, и это приводило к изменениям в отрицательную сторону обменных процессов, снижался уровень эритроцитов и гемоглобина.
В азотных ваннах организм человека подвергается всем видам воздействия, которые возможны. Это механическое воздействие, возникает за счет того, что азот очень плохо растворим в воде и поэтому образуются пузырьки газа, которые покрывают тело пациента, находящегося в ванне, кроме того механический эффект подкрепляется ещё и гидростатическим давлением. В результате этого возникает раздражение различных нервных окончаний, которые в огромном количестве имеются в коже, мышцах, сухожилиях, помимо нервных структур механическому влиянию подвергаются и сосуды. И вот, со всей поверхности человеческого тела из-за этого раздражения возникают импульсы, также в большом числе, которые устремляются в головной мозг. А уже оттуда идут команды к внутренним органам, которые вызывают ответные реакции.
Кроме механического действия возникает и термический эффект вследствие того, что вода и пузырьки азота имеют разную температуру (отличается она примерно на 15 градусов), в результате чего также возникают импульсы и ответные реакции организма.
И последний – это специальный эффект, проявляющийся из-за специфического влияния азота на организм человека. Азот проникает внутрь через кожу и в меньшей степени через дыхательную систему. В основе этого специфического действия на организм и различных реакция, возникающих при влиянии этих ванн, находится седативный эффект, оказывающий воздействие на головной мозг (центральную нервную систему).
Кроме того, принятие азотных ванн окажет обезболивающее и десенсибилизирующее действия, улучшит метаболические процессы, мышечный тонус, состояние эндокринной системы (особенно хорошее действие будет оказано на щитовидную железу при тиреотоксикозе, эффект при этой патологии от азотных ванн будет существенно выше, чем при применении ванн, содержащих другие химические вещества), вызовет изменения в гемодинамике (за счет спазмирования капилляров).
Азотные ванны являются слабым раздражителем, но тем не менее (и в этом их уникальность) они могут ослаблять и снимать процессы возбуждения (раздражения), вызванные различными причинами.
Показания к использованию азотных ванн:
- заболевания сердечно-сосудистой системы (вегето-сосудистая дистония с пониженным давлением, гипотония, атеросклероз),
- патологические процессы в суставах (воспалительной причины – артриты, дегенеративно-дистрофического характера – артрозы),
- заболевания нервной системы (астенические состояния, неврастения по гиперстенческому типу),
- заболевания системы пищеварительной (нарушения моторики кишечника и желчного пузыря по гипомоторному типу),
- заболевания эндокринной системы (тиреотоксикоз).
Противопоказания для азотных ванн:
острые воспалительные процесс, беременность, патология крови в остром периоде, инфекционные заболевания, склонность к кровотечениям, мокнущая экзема, туберкулез, почечная недостаточность, злокачественные и доброкачественные новообразования, тяжело протекающая патология сердца и сосудов.
Методика применения азотных ванн
В домашних условиях азотные ванны приготавливаются путем насыщения воды азотом и баллонов при помощи специальных аппаратов (аппарат насыщения – 8 или 9). Нужно, чтобы температура воды в ванне была 36 или 35 градусов, каждый день необходимо принимать такую ванну для получения положительного результата на протяжении половины месяца, от 10 и до 15 минут.
Санатории и курорты с азотными водами
Азотные минеральные воды - азотно-кремнистые (азотные термы) - природные теплые и горячие щелочные воды малой минерализации (до 2,0 г/л), различного ионного состава, содержащие свободный азот до 20-25 г/куб дм и большое количество кремнистой кислоты (50-150 мг/л). Часто азотистым водам в природе сопутствует повышенная концентрация фтора и присутствие радона.
В России и странах бывшего СССР эти воды находятся в Нальчике, Горячинске, Абастумани, Цхалтубо, Кульдуре, Северобайкальске (Дзелинда) и в других. В странах Европы: много в Болгарии, Пиренейские во Франции, Вильбад и Виссенбад в Германии, Лондек в Польше, Гастейн в Австрии, Янские Лазни в Чехии.
Врач терапевт Наумов Ю.Н
xn----jtbaaldsgaoflxr4fyc.xn--p1ai
Азот водяной пар - Справочник химика 21
Горение большинства веществ прекращается при снижении содержания кислорода в окружающей среде (азоте) до 12—16% [284] (или 11,0—13,5% [285]), а этилена и бутадиена — 10,0— 10,4% [286]. Исключение составляют вещества, обладающие широкой областью воспламенения, — водород, ацетилен, оксид углерода для них эта величина не превышает 5%, но в газах битумного производства они не присутствуют или присутствуют. практически в незначительных количествах. При хранении битумов в резервуарах пожаробезопасное содержание кислорода зависит от природы инертного газа (азота, водяного пара, диоксида углерода), т. е. флегматизатора, и составляет от 10 до 15% [209]. Эффективность действия,флегматизатора зависит от его свойств и пропорциональна отнощению теплоемкости к теплопроводности [287]. [c.176]
Параллельно с этим в генераторах азота сжигают природный газ в присутствии воздуха, получая азот, водяной пар и СО по реакции [c.110]В газовой фазе остаются азот, водяной пар и в небольших количествах метан. Если.в сырье содержатся сернистые соединения, в газах находится еще сероводород и сероуглерод. [c.45]
Неконтролируемая газовая среда формируется из продуктов окисления топлива, оставшихся после окисления компонентов воздуха (азот, водяные пары н др.), а также газов, выделяющихся или образующихся при протекании термотехнологических процессов. [c.76]
Отработанные газы окисления, состоящие из азота, водяных паров, диоксида и оксида углерода, остаточного кислорода и органических веществ, выводят из окислительного аппарата на термическое обезвреживание — сжигание. [c.294]
Здесь (с )од, (с9 ) ,, (водяного пара и влажного воздуха. [c.33]
Вдо Н —при 32°С в SO2, при интенсивном перемешивании, тумане из серной кислоты, селенистой кислоты, окислов азота, водяных паров и газах различного состава, включая и отработанные газы для I Укп = 3,8 мм/год, для [c.412]
В качестве газа-разбавителя при восстановлении чаще всего применяют азот. Водяной пар, как разбавитель, в процессе восстановления оказывает влияние на структуру катализатора и вызывает снижение его прочности [3, 28]. В работе [6] объясняют отрицательное действие пара присутствием в нем большого числа примесей. Двуокись углерода при определенных условиях (температура ниже 160 °С и парциальное давление 2,94-10 Па, 3 кгс/см ) может реагировать с окисью цинка, содержащейся в катализаторе, что приводит к снижению механической прочности. При действии НаО и СОа на окиси цинка протекает процесс, аналогичный спеканию, только при более низких температурах [3]. [c.373]
В результате на этой стадии получается смесь водяного пара, оксида углерода (П) и азота. Водяной пар, в свою очередь, восстанавливается снова с образованием водорода, как на второй стадии по реакции (20.2). [c.258]
Чем больше в топливе горючих элементов, т. е. углерода, водорода и серы тем выше его теплотворная способность, а чем больше балласта и негорючих элементов, т. е. азота, водяных паров, углекислого газа и минеральных примесей, тем ниже теплотворная способность топлива. Поэтому любое жидкое и газообразное топливо в целях улучшения эффекта сжигания подвергается предварительной обработке, т. е. удалению негорючих элементов, сушке и обогащению. [c.25]
Кислород, воздух, азот, водяной пар, аммиак [c.312]
Кислород, воздух, азот, водяной пар, аммиак Алифатические и ароматические углеводороды спирты, двуокись углерода, карбюраторное и дизельное топливо минеральные масла Вода под давлением, питательная вода, нейтральные сточные воды, морская вода, минеральные масла [c.312]
Показатели Двуокись углерода Серово- дород Азот Водяной пар Гелий [c.11]
Образование аммиака начинается при температурах около 400° С, затем растет до температуры 700° С, стабилизируется при 900° С, а при дальнейшем повышении температуры аммиак частично разлагается на водород и азот. Водяной пар, выделяющийся вместе с газом, замедляет реакции пиролиза аммиака. Выход аммиака зависит также от содержания азота в угле, В аммиак переходит примерно 10—15% азота угля. [c.84]
Основными компонентами продуктов сгорания в трубах являются оксиды углерода и азота, водяной пар, диоксид серы, а также твердые частицы золы. [c.183]
К газо- и парообразным огнегасительным средствам относятся двуокись углерода, азот, водяной пар, дымовые или отработанные газы. Огнегасительное действие этих [c.279]
Аварийный слив может осуществляться самотеком или под давлением инертной средой. Выдавливание инертной средой более эффективно, так как требует меньшей затраты времени. В качестве инертной среды используют азот, водяной пар, диоксид углерода. [c.339]
Восстановление галогенидов торня до металла, в частности кальцием, рассматривается в разделе 8.4. Металлический торий сохраняет гранецентрированную кубическую структуру вплоть до 1400° С. Его удельный вес 11,7 при 25° С. При температурах выше 1400° С металл имеет объемноцентрированную кубическую структуру и плавится при 1750° С. Столь высокая точка плавления в сочетании с сильно электроположительной природой металла значительно усложняет металлургию тория. Чтобы защитить металл от возможного взаимодействия с кислородом, азотом, водяным паром или водородом, необходимо работать в вакууме или в атмосфере инертного газа. Большинство материалов тигля взаимодействует с расплавленным торием до 1950° С применяется окись бериллия ВеО. [c.91]
Показатели Углекислый газ Сероводород Азот Водяной пар [c.156]
При разбавлении взрывоопасных смесей инертными газами и парами (углекислый газ, азот, водяной пар и др.) область воспламенения резко сужается, что позволяет во многих случаях вести борьбу со взрывами и пожарами. Характерно, что инертные разбавители мало повышают нижний предел воспламенения и значительно уменьшают его верхний предел, что объясняется частичным уменьшением содержания кислорода в смеси. [c.266]
Присутствие в газовой смеси примесей хлористого водорода — в результате расщепления хлорпроизвод-ных водородом или промотирования платинового катализатора введением хлористых соединений в сырье, аммиака — в результате расщепления соединений азота, водяных паров — в результате расщепления кислородных органических соединений — практически не сказывается на высокотемпературной сероводородной коррозии. [c.142]
Сепаратор, в котором проводится разделение дисперсной и газовой фаз после сепаратора возникают два материальных потока поток дисперсного оксидного материала, являющегося целевым продуктом, и поток газовой фазы, содержащей, как видно из уравнения (4.1), оксиды азота, водяной пар, азот и кислород. [c.165]
Одновременно образуется большое количество двуокиси углерода, окислов азота, водяных паров, несгоревших углеводородов, окислов металлов. В такой системе происходит сложное физико-химическое взаимодействие, в результате которого, например, сернистый ангидрид может превратиться в серную кислоту, сульфиты и сульфаты и постепенно осесть на поверхность земли. [c.163]
Содержание кислорода в техническом азоте не должно превышать по объему для I сорта—1% и для П сорта—2,5%. Содержание влаги может соответствовать полному насыщению азота водяным паром при температуре газа в баллоне. [c.48]
Поместите стеклянную трубку в находящийся в электролизере раствор и пропускайте через него в течение 10 мин. ток азота. (На пути газа необходимо ввести промывалку, наполненную водой, для насыщения азота водяным паром. В противном случае концентрация образца вследствие испарения будет изменяться.) Повторите снятие полярограммы на участках, где ранее наблюдались максимумы. [c.441]
Изменение (повышение при + Ор или понижение при —Ср) температуры в слое уменьшается с понижением исходной концентрации основного реагирующего вещества С = С р/С. Поэтому в некоторых производствах специально понижают С , вводя избыток второго реагента или балластного газа (воздуха, азота, водяного пара и т. п.). [c.259]
При очистке газа с высоким содержанием соединений серы приходится осуществлять регенерацию поглотителя для повторного использования. Регенерация производится смесью азота, водяного пара и воздуха при 500—550 °С. Этот процесс экзотермичен. Перегрев поглотителя выше 550 °С приводит к снижению его активности. Поэтому при регенерации необходимо регулировать концентрацию кислорода в поступающей смеси так, чтобы в начале процесса она не превышала 0,5 объемн. %. Отходящие при регенерации газы содержат сернистый ангидрид. [c.218]
Конечные продукты зависят от полноты сгорания. Это обычные топочные газы, смесь азота, водяных паров, углекислого газа с небольшой примесью окиси углерода. Некоторая часть несгоревшего углерода (несущего адсорбированные смолы и углеводороды) может появиться в виде дыма и сажи. Водород, количество которого в топливах достигает 12%, сгорая, дает воду, которая уносится в виде водяных наров, так что теплота испарения ее теряется. Эта потеря составляет разницу между высшей и низшей теплотворной способностью топлива. Сера сгорает до сернистого газа. [c.472]
Самопроизвольно протеШющий нёобратамъш процесс разрушения металлов, превращения их в химические соединения вследствие химического воздействия внешней среды, сопровождающийся изменением их физикохимических свойств, называется коррозией (лат. orro-sio — разъедание). Скорость коррозии зависит от характера среды. В обычной атмосфере металлы могут разрушаться, взаимодействуя с кислородом, азотом, водяными парами, оксидом углерода (IV), В производственных же условиях металлоизделия могут контактировать с более агрессивными веществами — щелочами, оксидами азота и серы, кислотами и галогенами. Следовательно, с учетом еще высоких температур и давлений, при которых осуществляются производственные процессы, скорость коррозии металлоизделий заметно усиливается. [c.399]
Медь и ее сплавы при нагревании взаимодействуют с кислородом, парами серы, сернистым ангидридом, сероводородом и фосфором, но стойки против действия азота, водяного пара, окиси и дву-окисй углерода и восстановительных газов в случае отсутствия закиси меди (водородная хрупкость) или переменных окислительно-восстановительных условий. [c.272]
X — при 32°С в SO2 при интенсивном перемешивании, в тумане из серной кислоты, селенистой кислоты, окислов азота, водяного пара, газах различного состава, включая отрабо-тайные газы для карпентера 20СЬ Укп = 0,225 мм/год (умеренное питтингообразование), для ни-о-неля 1- кп = = 0,250 мм/год (умеренное питтингообразование). Оба материала склонны к коррозионному растрескиванию. [c.413]
Такими свойствами обладают многие вещества, но из них в лра.ктике пожаротушения нашли применение углекислый газ, азот, водяной пар, распыленная вода, продукты сгорания и др. Из этой группы способов тушения наиболее употребительными являются [c.224]
Из инертных газов для тушения пожаров объемным способом наибольшее распространение получили двуокись углерода, азот, водяной пар и выхлопные газы двигателей внутреннего сгорания. Наименьшая огнетушащая концентрация двуокиси углерода для пламени различных горючих жидкостей неодинакова для этилового спирта 22,4%, автомобильного бензина 19%. Однако на практике применяется более высокая концентрация, например для тушения пожаров иа морских судах концентрация должна быть равна 30% для всех горючих жиякостей. В соотаетствии с этим для трюмов. морских и других закрытых помещений рекомендуется норма расхода двуокиси углерода 0,495 кг/м , для наиболее пожароопасных помещений — 0,594 кг/м . Интенсивность подачи двуокиси углерода предусматривается не менее 0,01 кг/(м .с), продолжительность заполнения 30% объема защищаемого помещения не должна превышать 1 мин. В США и Англии расход двуокиси углерода определяют в зависимости от объема защищаемого помещения. Для помещений объемом 120, 1400 и свыше 1550 мз расход двуокиси углерода равен соотвегствен-но 0,9 0.8 и 0,73 кг/м В СССР в настоящее время приняты следующие нормы подачи двуокиси углерода. Для производственных помещений категории В огнетушащая концентрация и норма расхода равны соответственно 22,4% и 0,637 кг/мз, для помещений категорий А и Б — 30% и 0,768 кг/мз. [c.104]
Несконденсировавшиеся пары азотной кнслоты, оксиды азота, водяные пары и инертные газы из холодильника-конденсатора направляются в абсорб-адонную башйк), й которой образуется 40—45%-ная азотная кислота, на-лравляем ая внс вь на концентрирование или в хранилища производства разбавленной азотной кислоты. Газы после абсорбционной башни выбрасывают В атмосферу. [c.118]
Сернистым газом называют смесь диоксида серы SO2, кис лорода, азота, водяных паров и других примесей. Диоксид серы, или сернистый ангидрид SO2 имеет относительную молеку-ля рную массу 64,063. Это бесцветный газ с резким запахом., хорошо растБОряется в воде с образованием сернистой кислоты— нестойкого соединения. Объем 1 кг SO2 (идеального газа) [c.22]
Наиболее концентрированные абгазы - это так называемые сдувки из реакторов незаполимеризовавшегося ВХ, содержащие до 95% ВХ, азот, водяные пары и небольшое количество кислорода. Если подвергнуть эту газовую смесь сжатию в компрессоре до давления 0,6 МПа, то По соотношению (5.2) давление паров винилхлорида составит р = 0,95 0,6 = 0,57 МПа. При данном давлении температура насыщения Газообразного ВХ в соответствии с формулой (5.3) составит 38 °С. При охлаждении газовой смеси, например до температуры 10 °С, часть винилхлорида сконденсируется, а оставшаяся газообразная часть ВХ будет иметь согласно уравнению (5.3) давление рк = 0,245 МПа. Содержание ВХ в газовой смеси при этом согласно (5.2) составит Ук = Рк/Ро 0,245/0,6 - 0,41. [c.149]
Газовоздушная смесь, состоящая из азота и водяного пара или из азота, водяного пара и углекислого газа, пропускалась через слой зерненного продукта, помещенного на сетчатое дно цилиндрического реактора 1, находящегося в термостате 2. Газовая смесь подавалась снизу с удельной скоростью 0,6 л1мин см . Навеска вещества составляла [c.129]
Методы, применяемые для хлорирования метана, довольно разнообразны. В общем они сводятся к действию ка смесь метана и хлора света, богатого химически действующими лучами, тепла, катализаторов и других активаторов, как например тихого электрического разряда. Наибольшие затруднении возникают при регулировании процеоса с целью избежания взрыва и образования каких-либо других, кроме требующихся, продуктов хлорирования. Надлежащий контроль за концентрациями, температурой и действием активаторов на реакцию уменьшает, хотя и не устраняет совсем, последнее из затруднений опасности взрыва можно до некоторой степени избежать разбавлением углеводорода каким-либо инертным газом, как наприме р двуокись углерода, азот, водяной пар, хлористый водород, или хлорированным веществом, а также точнывд регулированием количества В1ВОЛИМОГО в реакцию хлора. При.меняется также хлорирование в инертных жидких растворителях [c.750]
Применимость теории полимолекулярной адсорбции к твердым непористым адсорбентам проверялась неоднократно. Так, Гаркинс и Юра[ ] провели систематические исследования адсорбции азота, водяных паров, п-бутана, п-гептана на кристаллических непористых адсорбентах (ТЮа, ггЗО , Ва304, 8Юг) Эммет и Де-Витт [ ] исследовали адсорбцию N3 и С Н о на гг8Ю4, Ва304, ТЮз, ЪпО Ван-Иттербик и [c.689]
Восплаиеяение аимиачвокислородных смесей. Смеси аммиака с кислородом способны воспламеняться со взрывом. Температура воспламенения таких смесей находится в пределах 700—800 °С. В этом температурном интервале самовоспламенение смеси происходит при любом содержании в ней аммиака. При более низких температурах аммиачнокислородные смеси взрываются под действием импульса (запала). Нижний и верхний пределы взрываемости газовых смесей изменяются в зависимости от направлений движения газа (вверх или вниз), от давления, мощности импульса (запала) и других условий. Добавление инертных газов (азот, водяной пар) приводит к сужению пределов взрываемости газовой смеси. [c.351]
chem21.info
Аммонийный азот в воде и земле
Биогенный элемент, который активнейшим образом участвует в процессах биогидроценоза, - аммонийный азот.

Экологическая ситуация
В водоёмах можно наблюдать изменение содержания этого элемента: весной его становится меньше, зато летом, в связи с благоприятным температурным режимом, значительно увеличивается его концентрация, поскольку массированно разлагаются органические вещества.
И это кардинальным образом влияет на санитарное состояние водоёмов, что заставляет усиливать контроль за жизнеспособностью экосистемы. Предельно допустимой концентрацией в водоёмах, где ловят рыбу, считается та, где аммонийный азот не превышает 0,39 миллиграммов на литр.
В воде
Скопление белкового азота подвержено аммонификации, и этот процесс разлагает белки до аммонийного состояния. Сточные воды очищают при помощи этого источника азота, если в них имеется источник углеродного питания для клеток. Интенсивное использование наступает в периодах фазы их роста , а когда начинается окисление, аммонийный азот высвобождается в виде аммиака. Далее он окисляется до состояния нитритов и затем нитратов, или же повторно участвует в уже новом синтезе.
Для того чтобы аммонийный азот удалить из водоёма, применяется клиноптилолит, тогда вода восстанавливает свои качества. Ставятся градирни в тёплое время года, а зимой их заменяют ионообменные установки, благодаря которым вредные вещества удаляются из сточных вод. Постоянно проводятся анализы, берутся пробы на азот аммонийный в воде, который из взятой пробы отгоняется, а затем в полученном дистилляте определяется его количество.

Как очистить водоём
Существует в природе ионообменный материал, который называется клиноптилолит (класс цеолитов). Именно с его помощью целесообразно восстанавливать чистоту воды. Азот аммонийный в воде растворяется не полностью, поэтому сначала нужно освободить её от всех взвешенных веществ, после чего подавать воду на клиноптилолитовые фильтры. Это довольно дорогая очистка, но зато самая эффективная - достигает девяноста семи процентов.
Регенерация потребует внесения раствора хлористого натрия - пяти- или десятипроцентного. Загрузку после этого нужно отмыть водой. Из раствора будет выделяться аммиак, который можно поглотить серной кислотой, чтобы образовался сульфат аммония, который очень хорош как удобрение. Азот аммонийный в сточных водах, а также азотосодержащие органические соединения удаляют различными видами перегонки, экстракции, адсорбции.

Способы получения удобрений
Этот метод хорош, если необходимо определение аммонийного азота. Другие его формы, которые встречаются в тех же удобрениях, - амидная, нитратная - именно этим методом определить нельзя. Сначала нужно извлечь азот аммонийный, в сточных водах, например, его предостаточно. Об этом методе написано выше. Далее навеску будущего удобрения нужно поместить в колбу и пролить раствором соляной кислоты (концентрация должна быть молярной - 0,05 моль на дм3). Колбу необходимо встряхивать специальным аппаратом не менее получаса, после чего можно настаивать до пятнадцати часов.
Далее раствор снова взболтать и отфильтровать сквозь складчатый сухой фильтр. Тем же раствором соляной кислоты промыть содержимое фильтра как минимум трижды, затем объём фильтрата нужно довести до первоначального опять же раствором кислоты. Таким образом, во-первых, состоялось определение азота аммонийного в воде, а во-вторых - определение количества его в полученном удобрении. Последнее колеблется от сорока до ста пятидесяти миллиграммов на литр, а капролактама в этом же растворе содержится от восьми до восьмидесяти миллиграммов на литр. Если содержание аммонийного азота - менее двадцати миллиграммов, то опыт не удастся, и этот метод не применяется.
Источники загрязнения
Самые характерные особенности производственных сточных вод - нестабильный химический состав, необходимый период адаптации для развития микрофлоры, избыток соединений органического и минерального происхождения азота. Перед произведением биологической очистки на очистных сооружениях сточные воды смешиваются с бытовыми и хозяйственными и таким образом усредняются. Азот аммонийный (формула Nh5+) является обязательным компонентом сточных вод.
Источниками загрязнения могут являться сточные воды самых разных отраслей промышленности - от пищевой и медицинской до металлургической, коксохимической, микробиологической, химической и нефтехимической. Сюда же можно отнести все хозяйственно-бытовые стоки, навозные, сельскохозяйственные - с полей. В результате разлагаются белковые вещества и мочевина, а нитриты и нитраты анаэробно восстанавливаются.

Влияние на организм
На человеческий организм такие соединения влияют крайне отрицательно. Аммиак денатурирует белки, вступая с ними в реакцию. Тогда клетки и, соответственно, ткани организма перестают дышать, наблюдается поражение центральной нервной системы, печени, органов дыхания, нарушается работа сосудов. Если использовать регулярно воду с высоким содержанием аммония, страдает кислотно-щелочной баланс, начинается ацидоз.
Поэтому нельзя допускать использование выше нормы органических и минеральных удобрений в землепользовании, нужно постоянно бороться с излишним содержанием вредных веществ: например, азот аммонийный в почве обладает высокой растворимостью, поэтому и пища, и вода буквально отравлены им, его концентрации часто достигают токсического уровня. Особенно страдают от этого дети. Развивается метгемоглобинемия, кислородный режим в организме быстро разрушается, первым начинает страдать желудочно-кишечный тракт.

Предельные дозы
Единичные случаи заболевания метгемоглобинемией начинаются уже при содержании нитратов в воде до пятидесяти миллиграммов на литр, а когда концентрация их достигает девяноста пяти миллиграммов на литр, болезнь принимает массовый характер. В США, Франции, Нидерландах, ФРГ проведены детальные обследования, которые показали, что более пятидесяти миллиграммов нитратов на литр можно встретить в пятидесяти процентах случаев. Грунтовые и колодезные воды несут в десятки раз превышающую предел концентрацию нитратов - до полутора тысяч миллиграммов на литр, в то время как Всемирная организация здравоохранения установила предел в сорок пять миллиграммов. И это вода, которую пьют люди!
А уж сточные воды очищаются многими способами - и биологической фильтрацией, и окислением озоном, и гипохлоритами щёлочноземельных металлов, и аэрацией, и сорбцией, при которой используются цеолиты натриевой формы, и ионообменными смолами, и обрабатывают сильными щелочами, и флотацией, и восстанавливают аммоний металлическим магнием, и добавляют растворы хлорида магния с тринатрийфосфатом. Однако технологии очистки всегда намного отстают от технологий загрязнения.
Биогенные вещества
В природных водах растворяется газ (Nh4) аммиак, когда происходит биохимический распад органических соединений, в том числе и аммонийного азота. Тогда образуются и накапливаются другие соединения - аммоний-ион и азот аммонийный. Растворённый аммиак попадает в водоёмы с подземным или поверхностным стоком, со сточными водами, с атмосферными осадками. Если концентрация иона аммония (Nh5+) превысит фоновое значение, это будет означать появление нового и близкого источника загрязнения. Это могут быть как животноводческие фермы или скопления навоза, так и бесхозно брошенные азотные удобрения, как отстойники промышленности, так и очистные коммунальные сооружения.
А соединения азота, углерода, фосфора, которые содержатся в сточных водах, попадая в водоёмы, приносят значительный ущерб экологии практически всех регионов России. Очистка сточных вод день ото дня становится всё более актуальной, поскольку концентрация вредных веществ, в том числе и азотных соединений, зачастую просто зашкаливает. Это сказывается не только на питьевой воде. Быстро накапливают нитраты практически все овощи и фрукты, они содержатся в траве и зерне, которые поедает скот.

Содержание в водоёмах Nh4 и Nh5
Водоёмы всегда в нескольких переходных формах содержат азот: аммонийных солей и аммиака, альбуминоидного азота (органического), нитритов (солей азотистой кислоты) и нитратов (солей азотной кислоты). Всё это образуется вместе с процессом минерализации азота, но в большей мере поступает со сточными водами. Теперь водоёмы необходимо чистить. Соединения азота приходят на очистные сооружения в виде азота нитратов, азота нитритов, аммонийного азота и азота, связанного органическими соединениями. Сточные воды хозяйственно-бытового плана имеют небольшую концентрацию таких веществ, большую часть отправляет в водоёмы промышленность.
В процессе очистки соотношение массовых концентраций всех форм азотных соединений постоянно изменяется. Состав сточных вод становится другим уже при транспортировке, потому что мочевина, которая содержится в бытовых и хозяйственных сточных водах, взаимодействуя с бактериями, распадается и образует аммоний-ион. Чем протяжённее сеть канализации, тем дальше зайдёт этот процесс. Иногда содержание аммоний-иона при входе на очистку составляет до пятидесяти миллиграммов на кубический дециметр, что очень и очень много.
Органический азот
Это азот, который находится в составе органических веществ - протеидов и протеинов, полипепсидов (высокомолекулярных соединений), аминокислот, карбамидов (низкомолекулярных соединений), аминов, амидов. Вся органика, в том числе и азотосодержащая, попадает в сточные воды, после чего азотные соединения подвергаются аммонизации. Органического азота в сточных водах много, иногда до семидесяти процентов всех азотных соединений. Но в результате аммонизации на канализационном пути к очистным сооружениям приходит органического азота не более пятнадцати процентов.
Далее происходит уже рукотворная биологическая очистка. Первый этап - нитрификация, то есть переделка соединений азота за счёт определённых видов микроорганизмов, которые азот аммония окисляют, в нитрат-ион и нитрит-ион. Нитрифицирующих бактерий можно не опасаться - они к внешним условиям очень восприимчивы и легко вытесняются. А вот нитраты, если попадают в водоём, приводят его к гибели, поскольку являются великолепной питательной средой для разнообразной микрофлоры. Именно поэтому из экосистемы нитраты необходимо выводить.

Нитриты и нитраты
Если сточные воды проникают сквозь почву, то аммонийный азот под влиянием некоторых бактерий превращается сначала в нитриты, потом в нитраты. Преобладание и содержание разнообразных форм зависит от тех условий, которые складываются на момент поступления соединений с присутствием азота в почву, а затем в водоём.
Во время паводка концентрация органических форм его значительно увеличивается, поскольку органические остатки бывают смыты с поверхности почвы, а летом уменьшаются так же значительно, потому что служат "едой" для различных водных организмов. Нитриты - промежуточная форма окисления аммонийного азота, стремящегося стать нитратами. В природных водах нитратов обычно не так много, если не случилось смыва удобрений с полей.
fb.ru
Окись азота в воде - Справочник химика 21
Окись азота Вода 1,8 1 И [c.410]
СЕРНАЯ КИСЛОТА-ОКИСЬ АЗОТА—ВОДА [c.385]
Окись азота, которая образуется за счет связывания азота при горении, также присутствует в небольших количествах в выхлопном газе [11, 12]. Наличие несгоревшего остатка можно объяснить возможностью реакции окиси углерода с водой по уравнению [c.389]
Окислы азота. В отработавших газах могут содержаться окись азота (N0), двуокись азота (ЫОа) и высшие окислы (до НаОа). Попадая в организм человека, они соединяются с водой, образуя соединения азотной, азотистой и других азотсодержащих кислот. Для человека окислы азота примерно в 10 раз опаснее окиси углерода. Зависимость количества окислов азота от регулировочных параметров двигателя носит сложный характер. При изменении состава смеси количество окислов азота в выпускных газах имеет максимум при значениях а = 1,05—1,10 и при угле опережения зажигания, близком по крутящему моменту к оптимальному. С ростом степени сжатия и коэффициента наполнения содержание окислов азота в отработавших газах увеличивается. [c.345]Решение. Реакцию непосредственного окисления аммиака мысленно представим следующим образом. Аммиак разлагается на азот и водород затем азот с частью кислорода образует окись азота, а водород с оставшимся кислородом соединяется в воду, которая превращается в пар. Так как эти реакции в сумме эквивалентны основной, то, приравняв их теплоты, получим [c.15]
ОКИСЬ азота, аммиак, сернистый газ, сероводород, кислород, хлор, хлористый водород, углекислый газ, метан, ацетилен— могут быть собраны а) над водой б) непосредственно заполняя сосуд на воздухе [c.75]
Над водой можно собирать те газы, растворимость которых в воде мала окись азота, кислород, метан. Непосредственно, заполняя сосуд на воздухе, могут быть собраны все газы, кроме окиси азота, которая взаимодействует с кислородом воздуха, образуя двуокись азота [c.216]
Донорами электронов могут служить молекулы соединений азота (аммиак, триметиламин, пиридин и др.), кислорода (окись углерода, вода, диметиловый эфир и др.), а также ионы галогенов. Благодаря этому они могут соединяться с подходящими акцепторами электронов, а некоторые из них служить мостиками между двумя частями различных структур, например, в многоядерных комплексах (I), в осадках гидроксидов металлов (II) и др. [c.88]
Окись азота снова быстро окисляется кислородом воздуха до двуокиси, а NOj, в свою очередь, окисляет ион йода. Таким образом, N0 является соединением, которое каталитически ускоряет реакцию между йодидом и кислородом воздуха присутствие даже незначительного количества NO приводит к выделению большого количества йода. Поэтому необходимо обращать серьезное внимание на полное удаление окислов азота. Для их удаления раствор нужно тщательно прокипятить. Еще лучше совершенно удалить азотную кислоту выпариванием раствора с серной кислотой до появления тяжелых белых паров H SO,. Следует убедиться в полноте удаления HNO, (пробой с дифениламином, проверяя содержание ее в парах серной кислоты). В случае положительной реакции раствор после охлаждения осторожно разбавляют водой и повторяют выпаривание. [c.412]
Оксид азота (11), или окись азота, N0 представляет собой бесцветный трудно сжижаемый газ. Жидкий оксид азота (II) кипит при -151,7 °С и затвердевает при -163,7 °С. В воде он мало растворим 1 объем воды растворяет при 0°С всего 0,07 объема N0. [c.435]
Окись азота представляет собой бесцветный газ, сравнительно малорастворимый в воде и химически с ней не взаимодействующий. Свой кислород она отдает лишь с трудом. Поэтому горящая лучина в атмосфере N0 гаснет. [c.414]
Проведение опыта. В колбу Вюрца поместить смесь эквимо-лярных количеств йодида и нитрита калия, а в капельную воронку— 50%-ный раствор серной кислоты. Прилить серную кпслоту небольшими порциями в колбу. Выделяющуюся окись азота собрать над водой в цилиндре с помощью резинового шланга, соединенного с колбой Вюрца. Закрыть цилиндр под водой стеклянной пластинкой и вынуть из кристаллизатора. Поставить цилиндр на стол и открыть его. Появляются бурые пары двуокиси азота, которые постепенно заполняют весь цилиндр. [c.64]
Опрокинем в ванну с водой цилиндр с окисью азота. Вода в цилиндр не входит. Значит, окись азота с водой не реагирует и, очевидно, очень мало растворима в ней. [c.52]
Газовая смесь, выходящая из трубки, попадает в склянку, в которой окись азота окисляется кислородом, оставшимся в смеси. В двугорлой склянке двуокись азота реагирует с водой с образованием водного раствора азотной кислоты. [c.65]
Индий устойчив и не тускнеет на воздухе. Выше 800° горит фиолетово-синим пламенем, образуя окись. В воде в присутствии воздуха медленно корродирует. Растворяется в серной и соляной кислотах и более быстро в азотной. В плавиковой кислоте медленно растворяется только при нагревании. Органические кислоты, как уксусная, щавелевая и лимонная, также растворяют его [4]. С хлором и бромом реагирует при комнатной температуре, с иодом — при нагревании с азотом и водородом не взаимодействует. В атмосфере SOj при 750—1000° превращается в смесь окиси и сульфида [c.282]
Окись азота — бесцветный газ, плохо растворимый в воде (его можно собирать в цилиндре над водой). [c.242]
Выделившуюся окись азота окисляют воздухом в двуокись азота и применяют для нитрования. Получается серная кислота более высокой концентрации, чем в отработанной кислоте, за счет воды, вступающей в реакцию [уравнение (2)]. [c.398]
В ряде работ [1, 51—53] описывается успешное разделение окислов азота на пористых полимерных сорбентах. Одна из хроматограмм приведена на рис. 29. Разделение осуществлено на колонке с порапаком Р длиной 5 м при температуре 30° С [52]. Однако Троуэл [53], определявший окислы азота в выхлопных газах, полагает, что при газохроматографическом анализе окислов азота на порапаке или хромосорбе 102 двуокись азота взаимодействует с указанными сорбентами. В результате образуются окись азота, вода и происходит нитрование ароматических колец полимерных сорбентов. [c.114]
Продолжая исследования возможности стабилизации политетрафторэтилена, Уолл и Михаельсен [116, 117] изучили влияние различных газообразных веществ на его термодеструкцию, исходя из предположения, что эти газообразные вещества должны диффундировать в полимере легче, чем упоминавшиеся выше твердые реагенты, а это должно было бы ускорить инактивацию свободных радикалов внутри твердого полимера. Газообразные вещества, использовавшиеся в этих ргсследованиях, могут быть разделены на три группы 1) кислород, окись азота, вода и двуокись серы, сильно катализирующие процесс термодеструкции 2) водород, хлор, четыреххлористый углерод и толуол, действующие как ингибиторы 3) азот и бензотрифторид, не оказывающие влияния на процесс термодеструкции политетрафторэтилена. В присутствии кислорода полимер во время термодеструкции сохранял белую окраску и твердость продуктами реакции были четырехфтористый углерод, углекислота и окись углерода, а мономер не образовывался. Кислород, по-видимому, с очень высокой скоростью реагирует с полимерными радикалами, а образующиеся лабильные продукты превращаются в стабильные конечные вещества на стенке стеклянного реакционного сосуда [c.58]
СЕРНАЯ КИСЛОТА-ОКИСЬ АЗОТА—ВОДА Нз804—N0—Н,0 =20 [c.386]
Газы нз аппаратуры, содержащие нитропарафины, избыточный парафиновый углеводород, воду, не прореагировавшую азотную кислоту, окись азота и небольшое количество альдегидов и кетонов (около 1 г м ), подвергают сильному охлаждению и при этом выпадают ннпропара-фииы. Жидкие продукты разделяются на два слоя. Нитропарафины промывают водой и перегоняют. [c.297]
Решение. Получение азотной кислоты из аммиака идет в несколько стадий сначала аммиак окисляется в окись азота, затем в двуокись азота, которая многократным поглощением водой или слабой азотной кислотой превращается в HNOз. Схематически это можно представить следующими реакциями [c.37]
Термическое окисление аммиака кислородом (без применения специальных катализаторов) протекает с измеримой скоростью только при температурах выше 300° С. Температура начала окисления аммиака в основном зависит от материала стенок реактора, которые, вероятно, оказывают каталитическое действие. При термическом окислении аммиака образуется вода и азот со Следами окиси азота. В присутствии катализаторов это окисление можно регулировать соответствующим подбором температуры и объемной скорости таким образом, чтобы получать либо закись, либо окись азота. Так при окислении аммиака на окисном марганцевом катализаторе нри температурах до 250° С образуется только азот и закись азота NjO. Дальнейшее повышение темнерату ры приводит к образованию окиси азота N0. На смешанном катализаторе (45% СиО -Ь 45% MnOj -h -Ь 10% СаСОз) ДО 350° С также образуется только азот и закись азота. При повышении температуры появляется окись азота, а доля азота и закиси азота снижается. На других катализаторах и в области более высоких температур ( 600° С) закись азота не образуется, но получаются одновременно окись азота и азот в различных соотношениях. [c.155]
Азотную кислоту получают абсорбцией окислов азота водой и водными растворами азотной кислоты. С водой реагируют высшие окислы азота NOj, N364 и N2O3, поэтому окись азота, образующаяся при конверсии аммиака кислородом, должна быть окислена. [c.256]
Азотистокислый калий дает приблизительно такие же выходы, как и азотистокислый натрий, но с нитритами кальция и бария получаются нейколько пониженные результаты. В процессе сплавления в значительных количествах образуется спирт. Поскольку исходные соединения, повидимому, были сухими, становится неясным источник воды, необходимой для гидролиза. В течение реакции непрерывно выделяется окись азота, и возможно, что алкилнитриты образуются за счет взаимодействия азотистой кислоты со спиртами, а пе из исходных реагентов. При сплавлении смеси, содержаш ей метилсульфат калия, в качестве побочного продукта выделяется метиламин. Полученный указанным способом нитроэтан содержит небольшое количество нитробутана, образование которого, равно как и образование метиламина, объяснить затруднительно. Реакция нитритов с алкилсульфатами, в зависимости от взятого соединения, начинается при 90—140°, причем температуру начала реакции можно несколько снизить, прибавляя к реакционной Смеси небольшое количество воды. Согласно патенту [123], повысить выход нитросоединения можно смешением реагентов с углекислым натрием. [c.23]
На полноту выделения меди оказывает вредное влияние присутствие в растворе даже незначительных следов азотистой кислоты. Это объясняется тем, что при взаимодействии меди с азотистой кислотой образуется окись азота N0, которая быстро окисляется кислородом воздуха до двуокиси. Последняя образует с водой азотную и азотистую кислоты, а НЫОз снова окисляет осажденную медь. Чтобы з далить азотистую кислоту, нужно перед электролизом тщательно прокипятить раствор. [c.206]
Свежий (пары) и возвратный (жидкий) винилацетилен поступает в нижнюю часть реактора-гидрохлоринатора У. Хлористый водород подается в трубу газлифта реактора, где поглощается катализатором. Образующиеся в реакторе хлоропрен и дихлорбу-тены вместе с непрореагировавшим винилацетиленом, парами воды и хлористым водородом направляются в колонну первичного разделения 2, где отгоняется основная масса непрореагировавшего винилацетилена. Винилацетилен конденсируется, отделяется от кислых вод и в жидком виде возвращается в реактор. Кубовая жидкость колонны 2 — влажный хлоропрен-сырец — поступает в сепаратор 3, где отделяется от воды, охлаждается в холодильнике 4 и поступает в осушитель 5, заполненный хлоридом кальция. Выделение чистого хлоропрена с концентрацией 99,95 % осуществляется последовательной ректификацией на двух насадочных колоннах 6 я 7, работающих под вакуумом. Для предупреждения полимеризации хлоропрена применяют ингибиторы, в частности окись азота. [c.230]
Платина растворяется в царской водке (смесь кислот азотной и соляной). Образуются гексахлороплатиновая кислота, в которой окислительное число платины равно +6, окись азота и вода. Написать уравнение реакции. [c.114]
Проведение опыта. Колбу предварительно заполнить окисью азота. Для этого наполнить колбу водой, закрыть пробкой с длинной стеклянной трубкой и укрепить колбу в П1тативе вверх дном. Соединить трубку с прибором для получения окиси азота. Подставить под боковой отросток кристаллизатор и открыть кран. Пропустить окись азота в колбу. Собирающийся в колбе газ вытесняет воду через боковую трубку. Оставить в колбе немного воды. Отсоединить колбу от источника окиси азота и закрыть кран на боковом отростке. [c.65]
Окись азота очень мало растворима в воде, поэтому ее мо фарфоровую чашку с водой. Коническую иробирку, наполненную водой, закройте пальцем, переверните вверх дном и опустите в приготовленную ванну с водой. Следите, чгобы в пробирку не проник воздух и чтобы из нее не вылилась вода. В микроколбу прибора (см. рис. 22) поместите 2—4 маленьких кусочка медной стружки и 4—6 капель разбавленной азотной кислоты (пл. 1,12 г/см ). Закройте колбу пробкой с газоотводной трубкой. Трубку опустите в чашку с водой. После того как воздух из прибора будет вытеснен (1—2 мин), конец газоотводной трубки подведите под пробирку с водой. Если реакция идёт недостаточно энергично, колбу слегка подогрейте. Наполните пробирку газом на объема, оставив в ней немного воды. [c.140]
Наконец третья макроскопическая стадия составляет лишь окисление ацетальдегида двуокисью азота до конечных продуктов, включающих метилнитрит, нитрометан и метилниграт, воду, окись азота, двуокись углерода и формальдегид. [c.75]
Для очистки от высших окислов азота и брызг HNO3 окись азота пропускают через промывную склянку с 5%-ным раствором NaOH и собирают над водой. При необходимости газ сушат, пропуская через трубку с твердыл КОН. [c.24]
Полученный газ сохраняют в сконденсированном виде при охлаждении жидким воздухом или жидким азотом, что, однако, затруднительно вследствие необходимости постоянного наблюдения за подачей охлаждающих агентов в осуд Дьюара, в котором помещается конденсатор с окисью аёога. Более удобно сохранять окись азота в газометре над ртутыЪ или прокипяченной водой. В последнем случае газ перед использованием должен быть высушен твердой плавленой щелочью и пятиокисью фосфора. [c.193]
В испаритель, где происходило испарение бензола, поступавшего с определенной скоростью из сборника. Образовавшуюся в испарителе смесь паров бензола и двуокиси азота направляли в реакционную камеру (стеклянную трубку со слоем катализатора длиной 110 см), которую нагревали в длинной электропечи. Шидкие продукты реакции и непрореагировавший бензол собирали в приемнике, соединенном с обратным холодильником и охлаждаемом льдом, а окислы азота, образовавшиеся во время реакции, вместе с избыточной двуокисью азота про ходили через поглотительную систему с водой, далее через растворы окислителей, где окись азота N0 окислялась до NOa, которая затем улавливалась 10%-ным раствором NaOH. [c.412]
chem21.info
ВОДА ПРИЙДЕТ – АЗОТ УВЕДЕТ
ВОДА ПРИЙДЕТ – АЗОТ УВЕДЕТ

Весна этого года была щедра на осадки и скупа на тепло. Поэтому вместо ожидаемой с нетерпением «пары дождиков в апреле, пары дождиков в маю» в апреле-мае на юге Украины осадков оказалось в два-три раза больше средней многолетней месячной нормы. Осадки были разные: снег, снег с дождем, дождь «грибной» и дождь проливной. В течение суток кое-где выпадало до 30-35 мм влаги. Вода не успевала впитываться и испаряться, поэтому многие посевы напоминали не поля в степи, а затопленные рисовые чеки. На некоторых затопленных полях посевы оказались под водой «с головой».
В многокомпонентной системе избыток одного компонента вызывает недостаток другого. Почва, как известно, состоит из трех фаз – твердой (минеральной), жидкой и газообразной.  Воздух и вода в почве занимают пространство между частицами твердой фазы. Поэтому влага обильных осадков вытесняет из почвы воздух. Часть кислорода почвенного воздуха растворяется в воде, но это – очень небольшая часть кислорода, необходимого для дыхания корневой системы растений. К тому же, чем выше температура почвы (и воды), тем меньше в воде растворенного кислорода, и тем выше в нем потребность растений. Поэтому переувлажнение почвы приводит к угнетению роста и развития растений, а в некоторых случаях – к гибели от удушья.
Воздух и вода в почве занимают пространство между частицами твердой фазы. Поэтому влага обильных осадков вытесняет из почвы воздух. Часть кислорода почвенного воздуха растворяется в воде, но это – очень небольшая часть кислорода, необходимого для дыхания корневой системы растений. К тому же, чем выше температура почвы (и воды), тем меньше в воде растворенного кислорода, и тем выше в нем потребность растений. Поэтому переувлажнение почвы приводит к угнетению роста и развития растений, а в некоторых случаях – к гибели от удушья.
Добро и зло – одна монета,А ляжет так, как повезло,Придя добром к кому-то где-то,Другому причиняет зло.(В. Поляков)
«Уход» воды с поверхности поля и подсыхание верхнего слоя почвы не гарантируют избавления от проблемы дефицита кислорода в почве. Высохшая поверхность затопленного поля часто покрывается плотной воздухонепроницаемой почвенной коркой, которая «не пускает» воздух в почву. Поэтому, кстати, подсохшую корку рекомендуется своевременно «разбивать» ротационными мотыгами или боронами.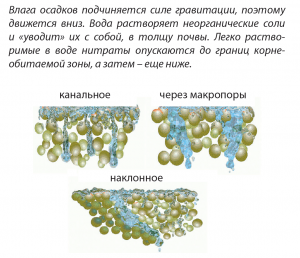 Ущерб от переувлажнения/затопления не ограничивается только дефицитом кислорода для растений. Существует еще одна «статья расходов», которая неизбежно активируется при выпадении обильных осадков. Вода растворяет минеральные удобрения. И уносит их с собой. Нитратный азот покидает корнеобитаемый слой как по вертикали (промывается при инфильтрации почвы), так и по горизонтали (смыв с поверхности почвы). Кроме того, в анаэробных условиях переувлажненной почвы нитратный азот подвергается денитрификации. То есть превращается в молекулярный азот и возвращается «в воздух».Как оценить вероятные потери? И что делать потом с этим знанием?
Ущерб от переувлажнения/затопления не ограничивается только дефицитом кислорода для растений. Существует еще одна «статья расходов», которая неизбежно активируется при выпадении обильных осадков. Вода растворяет минеральные удобрения. И уносит их с собой. Нитратный азот покидает корнеобитаемый слой как по вертикали (промывается при инфильтрации почвы), так и по горизонтали (смыв с поверхности почвы). Кроме того, в анаэробных условиях переувлажненной почвы нитратный азот подвергается денитрификации. То есть превращается в молекулярный азот и возвращается «в воздух».Как оценить вероятные потери? И что делать потом с этим знанием?
Нитраты! «На выход!»
День наступит – откроются люки,И вонючие руки утянут за брюки.И дурная вода унесёт нас туда,Где нам выпишут вечные муки…(В. Поляков)
Первой жертвой наводнения или переувлажнения становится наиболее мобильная форма азота – нитратная. В экстремальных условиях возможна потеря практически 100% нитратного азота, находящегося в корнеобитаемом слое почвы.Основным путем потерь нитратного азота на легких (песчаных и супесчаных почвах) является выщелачивание (промывание). Растворенные в воде нитраты мигрируют с потоком воды, опускаясь все ниже и ниже по мере инфильтрации почвы водой. Если на пути влаги не оказывается препятствий типа «плужной подошвы», то нитраты покидают пределы корнеобитаемого слоя и двигаются дальше. Кстати, при выращивании риса «плужная подошва» создается искусственно – для того, чтобы «не дать смыться» азотным удобрениям.Чем выше водопроницаемость почвы и чем хуже ее водоудерживающие свойства, тем больше потери нитратного азота от промывания. На плотных почвах тяжелого механического состава, хорошо удерживающих и плохо пропускающих влагу, потери нитратов от промывания возможны только при длительном периоде избыточного увлажнения. Потери нитратов в результате инфильтрации с влагой в нижние горизонты тяжелой суглинистой почвы примерно в 4-5 раз меньше, чем на легкой песчаной при сопоставимом количестве выпавших осадков.Плотные тяжелые почвы хорошо удерживают влагу, поэтому вода, залившая «с верхом» глинистое поле, долго не покидает такую «гостеприимную» почву. Из-за этого почву начинает покидать азот. Не через «дно» пахотного слоя, а через его «верх». И не с водой, а с воздухом. В результате процесса денитрификации.
Нитрификация с приставкой «де»
В моей частичке de знак чванства,Я слышу, видят: вот беда!«Так вы из древнего дворянства?»Я? Нет… куда мне, господа!(Пьер-Жан де Беранже)
Соединения азота трансформируются и «переформатируются» обитающими в почве микроорганизмами. В анаэробных условиях при достаточно высокой температуре и щелочной реакции почвы создаются условия для денитрификации – преобразования микрофлорой почвы нитратов в газообразные оксиды и молекулярный азот. В природе денитрификация имеет широкие масштабы. В результате в атмосферу ежегодно поступает 270-330 млн т N2, т.е. этот процесс сравним с азотфиксацией. Большая часть этого азота – потери из почвы.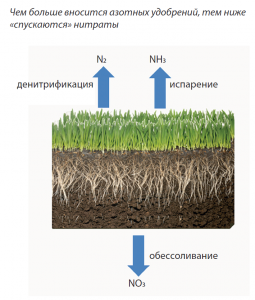 Первый этап денитрификации – переход нитратов в нитриты – способны осуществлять не только бактерии, но водоросли, грибы и дрожжи. На заключительном этапе денитрификации (до молекулярного азота) участвуют только прокариоты. Большинство из них – факультативные анаэробы, которые заменяют отсутствующий в анаэробных условиях кислород нитратами.Процесс денитрификации вполне корректно называют анаэробным нитратным дыханием. Нитраты в анаэробных условиях выполняют функцию акцепторов электронов, поступающих с окисляемого субстрата. Соответственно, субстрат окисляется, а нитраты восстанавливаются в последовательности: NO- –>NO- –>NO –>N2O –>N2. Энергетический выход при переносе электронов к NO- и N2O приблизительно одинаков и в сумме составляет около 70% энергетического выхода при дыхании с участием свободного кислорода. То есть нитратное дыхание на треть менее эффективно, чем «традиционное», с использованием кислорода. Поэтому микрофлора почвы использует нитраты только при дефиците азота. Соответственно, восстановление доступа кислорода в почву (аэрация) прекращает процесс денитрификации. Рыхление почвы (разрушение почвенной корки), например, не только улучшает снабжение корневой системы растений кислородом, но прекращает «вредительскую» деятельность нитрифицирующих бактерий.О том, что бактерия участвует в денитрификации, красноречиво свидетельствует ее «фамилия» с аристократической приставкой «де»: Thiobacillus denitriflcans, Thiomicrospira denitrificans, Paracoccus denitrificans Paracoccus denitrificans. Но есть бактерии (Pseudomonas studzeri, Pseudomonas fluorescens), «ФИО» которых не указывает на их потенциальные денитрифицирующие свойства.
Первый этап денитрификации – переход нитратов в нитриты – способны осуществлять не только бактерии, но водоросли, грибы и дрожжи. На заключительном этапе денитрификации (до молекулярного азота) участвуют только прокариоты. Большинство из них – факультативные анаэробы, которые заменяют отсутствующий в анаэробных условиях кислород нитратами.Процесс денитрификации вполне корректно называют анаэробным нитратным дыханием. Нитраты в анаэробных условиях выполняют функцию акцепторов электронов, поступающих с окисляемого субстрата. Соответственно, субстрат окисляется, а нитраты восстанавливаются в последовательности: NO- –>NO- –>NO –>N2O –>N2. Энергетический выход при переносе электронов к NO- и N2O приблизительно одинаков и в сумме составляет около 70% энергетического выхода при дыхании с участием свободного кислорода. То есть нитратное дыхание на треть менее эффективно, чем «традиционное», с использованием кислорода. Поэтому микрофлора почвы использует нитраты только при дефиците азота. Соответственно, восстановление доступа кислорода в почву (аэрация) прекращает процесс денитрификации. Рыхление почвы (разрушение почвенной корки), например, не только улучшает снабжение корневой системы растений кислородом, но прекращает «вредительскую» деятельность нитрифицирующих бактерий.О том, что бактерия участвует в денитрификации, красноречиво свидетельствует ее «фамилия» с аристократической приставкой «де»: Thiobacillus denitriflcans, Thiomicrospira denitrificans, Paracoccus denitrificans Paracoccus denitrificans. Но есть бактерии (Pseudomonas studzeri, Pseudomonas fluorescens), «ФИО» которых не указывает на их потенциальные денитрифицирующие свойства.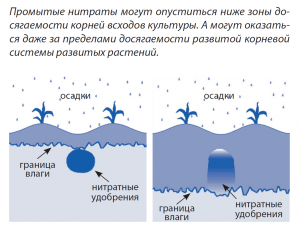 Более того, известный азотфиксатор Azospirillum lipoferum при наличии нитратов в анаэробных условиях проводит денитрификацию, а в аэробных – ассимилирует нитрат. Это вполне объяснимо. Ферменты азотного цикла (нитрогеназа азотфиксаторов, нитритоксидоредуктаза нитрификаторов, ассимиляторная и диссимиляторная нитратредуктазы) имеют общий «структурный элемент» — низкомолекулярный молибденсодержащий кофактор. Он может «переустанавливаться» микроорганизмом с одного фермента на другой, в зависимости от ситуации. Таким образом, процессы нитратредукции, азотфиксации и денитрификации взаимно связаны и могут осуществляться одними и теми же бактериями, но в разных условиях.
Более того, известный азотфиксатор Azospirillum lipoferum при наличии нитратов в анаэробных условиях проводит денитрификацию, а в аэробных – ассимилирует нитрат. Это вполне объяснимо. Ферменты азотного цикла (нитрогеназа азотфиксаторов, нитритоксидоредуктаза нитрификаторов, ассимиляторная и диссимиляторная нитратредуктазы) имеют общий «структурный элемент» — низкомолекулярный молибденсодержащий кофактор. Он может «переустанавливаться» микроорганизмом с одного фермента на другой, в зависимости от ситуации. Таким образом, процессы нитратредукции, азотфиксации и денитрификации взаимно связаны и могут осуществляться одними и теми же бактериями, но в разных условиях.
«Райдер» денитрифицирующих бактерий
Не жертвуй светом, добывая свет!Ведь ты не знаешь, что творишь на деле.Цель средства не оправдывает… Нет!У жизни могут быть иные цели.(Н. Коржавин)
На интенсивность денитрификации влияет:1. Продолжительность «безвоздушного» периода в переувлажненных, переуплотненных или заиленных почвах. Содержание кислорода в основном зависит от влажности почвы, которая, в свою очередь, определяется механическим составом и плоностью.2. Температурный режим. Скорость денитрификации увеличивается экспоненциально в интервале от 15°C до 30°C, максимальные потери нитратного азота отмечаются при температуре почвы от 23°C до 27°C.3. Содержание нитратов и органических веществ. Бактерии нуждаются в источнике легкодоступных органических веществ. Поэтому денитрификация интенсивно происходит на богатых органикой почвах. Запаханные растительные остатки и органические удобрения стимулируют процесс. И, конечно же, должно быть необходимое количество нитратов.4. рН почвы. Процесс денитрификации интенсивно происходит в щелочных почвах, в кислых почвах денитрификация очень медленная.Для того, чтобы начался интенсивный процесс денитрификации на затопленных почвах, требуется от двух до трех дней. За день теряется в среднем от 3% до 4% азота. При высокой температуре почвы (более 23°С) ежедневные потери от денитрификации могут «умножать на ноль» до 5-6% нитратного азота. Потери от 25% до 50% нитратного азота – вполне обычная «дань», которую аграрии платят почвенной микрофлоре. В США, например, средние ежегодные потери нитратного азота при выращивании кукурузы составляют 40-75 кг д.в/га за год.Можно сделать простой, и в какой-то мере правильный вывод: «Долой нитратные удобрения!». Но, как и любые громкие лозунги и скоропалительные выводы, он содержит только часть правды. И не содержит приемлемой альтернативы.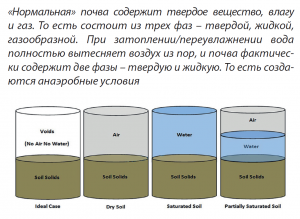 Нитратная форма азота – это «быстрый» азот, поэтому ее целесообразно использовать при «быстром» получении всходов и высоких темпах роста культуры. То есть для внесения под предпосевную культивацию/посев при относительно поздних сроках посева, при минимальной вероятности проливных дождей. Либо для подкормок вегетирующей кукурузы или подсолнечника с заделкой в почву междурядий.Заранее вносить большое количество нитратных форм азота под пропашные культуры – неоправданный риск «потерять» (более точное определение – сами знаете какое) большую часть нитратов еще до того, как культура будет готова их усвоить.До фазы 6 листка ни кукуруза, ни подсолнечник не потребляют сколь-нибудь значимых (около 5%) количеств азотных удобрений. При раннем посеве (в первой декаде апреля) всходы появляются не ранее, чем через 15-18 дней. Темпы развития в условиях холодной весны замедлены (как в этом году), поэтому интервал от появления всходов до 6-8 листка составляет около 3 недель. Итого – 1,5 месяца удобрения «легли и просят», пока до них доберутся корни культуры. А за это время шансы азота «промыться» и «испариться» становятся настолько велики, что практически гарантированы. Посевы в период интенсивного роста останутся «голодными»,а карманы агрария по итогам сезона – пустыми.
Нитратная форма азота – это «быстрый» азот, поэтому ее целесообразно использовать при «быстром» получении всходов и высоких темпах роста культуры. То есть для внесения под предпосевную культивацию/посев при относительно поздних сроках посева, при минимальной вероятности проливных дождей. Либо для подкормок вегетирующей кукурузы или подсолнечника с заделкой в почву междурядий.Заранее вносить большое количество нитратных форм азота под пропашные культуры – неоправданный риск «потерять» (более точное определение – сами знаете какое) большую часть нитратов еще до того, как культура будет готова их усвоить.До фазы 6 листка ни кукуруза, ни подсолнечник не потребляют сколь-нибудь значимых (около 5%) количеств азотных удобрений. При раннем посеве (в первой декаде апреля) всходы появляются не ранее, чем через 15-18 дней. Темпы развития в условиях холодной весны замедлены (как в этом году), поэтому интервал от появления всходов до 6-8 листка составляет около 3 недель. Итого – 1,5 месяца удобрения «легли и просят», пока до них доберутся корни культуры. А за это время шансы азота «промыться» и «испариться» становятся настолько велики, что практически гарантированы. Посевы в период интенсивного роста останутся «голодными»,а карманы агрария по итогам сезона – пустыми.
Денитрификация аммонийного азота
Дорогу свою выбирая,О лишних шагах не жалей,Короче – конечно прямая,Кривая, зато, – веселей…(В. Поляков)
При высоком риске затопления лучше использовать аммонийную или амидную формы азота. В тех регионах, где существует риск наводнений и затопления посевов, предпочитают использовать КАС, карбамид, сульфат аммония. Например, в северо-восточной части «болотного» штата Луизиана традиционно используют гранулированную мочевину (46-0-0) или КАС (32-0-0) в качестве основного источника азота. А при выращивании риса основными источниками азота являются сульфат аммония и карбамид.Это позволяет существенно сократить потери, но не избежать их полностью. Нитратная форма в КАСе, например, промывается и денитрифицируется так же легко, как и любой другой нитрат. Поэтому 25% азота из КАСа при затоплении поля исчезают в течение считанных дней.Аммиачная и амидная формы азота прочно удерживаются в почве, но в результате трансформаций со временем превращаются в нитратный азот. Выпадение обильных осадков через день-два после внесения КАСа или карбамида приводит к минимальным потерям азота.Но после нитрификации (перехода азота из аммиачной формы в нитратную) в течение 1-2 месяцев, затопление поля приведет к потере более 50% внесенного минерального азота. Чем больше интервал между внесением аммонийного азота и затоплением поля, тем больше аммония превратится в нитрат.Превращение аммония в нитрат являются результатом деятельности обитающих в почве нитрифицирующих бактерий. Для нитрификации очень важна температура почвы (быстрее проходит в «теплых» почвах, медленнее – в холодных) и наличие воздуха (аэробные условия). Гранулированная мочевина преобразовывается в аммонийную форму в процессе гидролиза. Поэтому карбамид превращается в нитрат медленнее, чем КАС.Средняя скорость нитрификации при температуре почвы 14-18°С составляет около 2,5%в день, а при более высокой температуре почвы превышает 4,5-5 % в день.Например, при внесении 200 кг д.в азота/га в форме КАС (32%) за три недели до «потопа», при температуре почвы около 15°С, в нитратную форму перейдет около 120 кг д.в азота (200 x 0,6). А при внесении того же количества азота в той же форме за неделю до затопления поля, в нитратную форму перейдет только 50 кг азота в д.в. (200 x 0,25). Сотрудниками университета штата Айова Р. Дж. Килдорном и С. Е. Тейлором была разработана компьютерная программа, прогнозирующая поведение внесенного в почву безводного аммиака. Эта программа позволяет рассчитать процент нитрификации внесенного азота в аммиачной/аммонийной форме при различных условиях. Например, при внесении аммонийного азота в почву в период с 1 октября до 1 ноября, по данным предварительных расчетов, к 1 мая весь азот преобразуется в нитратную форму.Использование ингибитора N-Serve существенно замедляет процесс нитрификации.Например, при внесении аммиака с ингибитором нитрификации 1 октября, в почве к 1 мая сохранится около 35% азота в аммонийной форме, а при внесении удобрений 1 ноября – 50%.Из этих предварительных расчетов можно сделать вывод: чем ближе к посеву вносятся азотные удобрения, тем больше шансов их «целевого использования» культурными растениями и меньше вероятность потерь. Это правило касается и КАСа, и карбамида, и сульфата магния.
Сотрудниками университета штата Айова Р. Дж. Килдорном и С. Е. Тейлором была разработана компьютерная программа, прогнозирующая поведение внесенного в почву безводного аммиака. Эта программа позволяет рассчитать процент нитрификации внесенного азота в аммиачной/аммонийной форме при различных условиях. Например, при внесении аммонийного азота в почву в период с 1 октября до 1 ноября, по данным предварительных расчетов, к 1 мая весь азот преобразуется в нитратную форму.Использование ингибитора N-Serve существенно замедляет процесс нитрификации.Например, при внесении аммиака с ингибитором нитрификации 1 октября, в почве к 1 мая сохранится около 35% азота в аммонийной форме, а при внесении удобрений 1 ноября – 50%.Из этих предварительных расчетов можно сделать вывод: чем ближе к посеву вносятся азотные удобрения, тем больше шансов их «целевого использования» культурными растениями и меньше вероятность потерь. Это правило касается и КАСа, и карбамида, и сульфата магния.
Занимательная арифметика
Как здоровье, так и счастье,Если есть – не замечаем,Лишь когда придут напастиИх нехватку ощущаем…(В. Поляков)
На потери от промывания и нитрификации существенно влияет содержание в удобрении нитратного, аммонийного и амидного азота. При этом необходимо предусмотреть трансформацию аммонийных/амидных форм в нитратную на протяжении периода от внесения удобрения до затопления поля.Процесс нитрификации зависит от внешних условий. Температура и влажность почвы важны для прогноза степени преобразования аммонийного или амидного азота в мобильную нитратную форму.Количество выпавших осадков и продолжительность затопления позволяют определить количество промытого нитратного азота и потери от денитрификации.Алгоритм расчетов можно продемонстрировать на примерах.Пример №1. Под предпосевную культивацию внесли 350 л КАС, то есть 100 кг азота д.в /га. Через 10 дней после посева выпали обильные осадки, затопившие поле на 2 дня. Температура почвы в этот период была около 17°С. Сколько было потеряно?Решение: При затоплении теряется азот в нитратной форме. Поэтому 25% азота КАС, то есть та часть, которая находится в нитратной форме, гарантированно теряется. Кроме того, теряется часть азота, который образовался в результате нитрификации аммонийного и амидного азота. Процесс нитрификации продолжался 10 дней, за день нитрификации подвергалось примерно 2,5% аммонийного азота.Таким образом, потери азота составят:(0,25 * 100 кг N д.в / га) + (10 дней * 0,025 * 75 кг N д.в / га) = 25 + 18,75 = 43,75 кг д.в N /га.То есть при заданных условиях ожидаются потери более 40% от внесенного с удобрением азота.Пример № 2. Под предпосевную культивацию внесли 175 кг д.в N / га в форме карбамида. Почва плохо дренированная. Через три недели после внесения удобрения поле было затоплено на протяжении семи дней. Сколько азота было потеряно?Решение: Определяем количество азота в форме нитрата. Согласно таблице, 50% мочевины будут в форме NO3-N. Через три недели после внесения карбамида 50% азота перешло в нитратную форму. То есть 175 кг д.в N x 50% = 88 кг д.в N.Чтобы бактерии начали процесс денитрификации, необходимо минимум два дня. Поэтому денитрификация происходила в течение пяти дней, каждый день терялось 4% нитратного азота. То есть за 5 дней потеряно 20% от общего количества азота в нитратной форме. Это составило 88 x 20% = 18 кг д.в N потеряно. При этом в почве осталось 157 кг азота в д.в. Кукуруза после такого продолжительного пребывания в затопленном состоянии, скорее всего, погибла бы.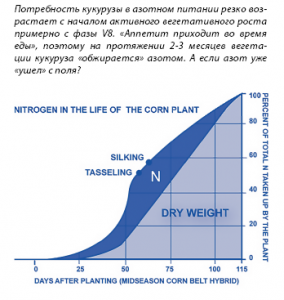 Подобная методика оценки потерь азота не претендует на точность, но дает хотя бы приблизительное представление о ущербе.Для получения точных данных о наличии азота необходимо провести анализ почвы.В почве достаточно доступного для растений азота, если почва содержит более 25 ppm нитратного азота. В такой ситуации проведение подкормок не является жизненно необходимым.Если содержание нитратного азота составляет от 11 до 25 ppm (частей на миллион), то целесообразно проведение подкормки азотными удобрениями в норме 30-100 кг д.в/азота /га.Если уровень нитратного азота в почве находится в интервале 18- 11 ppm, то необходимо вносить как минимум 50-70 кг д.в азота/га. При более высоком содержании нитратов можно обойтись внесением 30-40 кг д.в азота/га.Если содержание нитратов составляет менее 11 частей на миллион, целесообразно внести в виде подкормки от 100 до 150 кг д.в азота/ га.
Подобная методика оценки потерь азота не претендует на точность, но дает хотя бы приблизительное представление о ущербе.Для получения точных данных о наличии азота необходимо провести анализ почвы.В почве достаточно доступного для растений азота, если почва содержит более 25 ppm нитратного азота. В такой ситуации проведение подкормок не является жизненно необходимым.Если содержание нитратного азота составляет от 11 до 25 ppm (частей на миллион), то целесообразно проведение подкормки азотными удобрениями в норме 30-100 кг д.в/азота /га.Если уровень нитратного азота в почве находится в интервале 18- 11 ppm, то необходимо вносить как минимум 50-70 кг д.в азота/га. При более высоком содержании нитратов можно обойтись внесением 30-40 кг д.в азота/га.Если содержание нитратов составляет менее 11 частей на миллион, целесообразно внести в виде подкормки от 100 до 150 кг д.в азота/ га.
Компенсация потерь: чем, когда и как
Всё закончится очень удачно.Так пророчил восточный мудрец.Если в данный момент что-то мрачно,Значит это – ещё не конец(В. Поляков)
Способы компенсации потерянного при «потопе» азота можно рассмотреть на примере кукурузы.Кукуруза до стадии V6 потребляет примерно 5% азота от общей сезонной потребности. Но от стадии V6 до VT (появление метелки) у кукурузы «появляется аппетит», и она за месяц поглощает примерно 60% от сезонной нормы азота. То есть примерно 100-120 кг д.в азота/га. Период быстрого роста культуры продолжается около месяца, и если на протяжении этого периода кукуруза останется «недокормленной», то к уборке она «отомстит» существенным недобором урожая.Обильные осадки активно сокращают запасы азота, «промывая» нитратный азот из удобрений, внесенных до посева. Потери могут составлять 30-50%, то есть кукуруза остается на урезанном, «половинном пайке» азота. С вполне ожидаемыми последствиями в виде резкого уменьшения урожайности.Может ли подкормка компенсировать «потерянный» азот? По данным американских исследователей, дефицит азота в фазу V6 удавалось компенсировать подкормкой до фазы R1. Дефицит азота удается успешно «догнать» без уменьшения урожайности при внесении азотных удобрений до стадии роста V11. Применение азотных удобрений в фазу от V12 до V16 сопровождалось снижением урожайности на 3% -по сравнению с вариантом, где весь азот вносился при посеве и не был потерян. Лучшие результаты обеспечивало внесение разбрасывателем карбамида, обработанного ингибитором уреазы. При быстром подсыхании поверхности поля на легких, хорошо дренированых почвах целесообразно внесение аммиачной селитры в междурядья при высоте растений около 30 см.Тяжелые почвы после выпадения осадков остаются влажными на протяжении длительного времени. Поэтому внесение минеральных удобрений с заделкой в междурядья в таких условиях нецелесообразно: вовремя – невозможно, а поздно – напрасные траты. Поэтому для оперативного возмещения потерянного азота приходится полагаться на поверхностное внесение гранулированных минеральных удобрений: сульфата аммония (21-0-0-24) и мочевины (46-0-0).В пересчете на стоимость 1 кг д.в азота мочевина дешевле, чем сульфат аммония. Но газообразные потери азота (в виде аммиака) из карбамида могут достигать 20-30%, а сульфат аммония более стабилен.Мочевина, внесенная на сухую почву, начинает постепенно улетучиваться. Скорость испарения достигает максимума примерно через три дня после внесения и зависит от типа почвы и ее влажности. Как правило, на щелочных почвах газообразные потери азота выше, чем в кислых. А при внесении мочевины на поверхность влажной почвы потери азота существенно выше, чем при разбрасывании по сухой почве.Потери азота при поверхностном внесении мочевины можно сократить за счет обработки гранулированной мочевины ингибитором уреазы (NBPT или NPPT). Ингибитор уреазы временно замедляет превращение мочевины микроорганизмами в аммонийную форму (гидролиз мочевины) и поэтому сокращает потери от улетучивания аммиака (конверсия амидной формы азота в газообразный аммиак). Ингибиторы уреазы уменьшают потери аммиака в течение 10 дней при нанесении на сухую почву. При внесении на влажную почву время защитного действия сокращается вдвое (максимум до 5 дней), а при попадании карбамида в воду ингибиторы уреазы теряют свои свойства.Ингибиторы нитрификации (действующие вещества нитрапирин или DCD) временно препятствуют процессу нитрификации. Исследования на северо-востоке Луизианы показали, что ингибиторы нитрификации могут приостановить этот процесс в течение 10-30 дней, в зависимости от факторов окружающей среды и почвы.Если почва слишком влажная для внесения минеральных удобрений в междурядья, а кукуруза остро нуждается в азоте, то придется делать выбор между поверхностным внесением гранулированного сульфата аммония или карбамида. При внесении карбамида лучше подождать, пока поверхность почвы подсохнет. Карбамид, обработанный ингибитором уреазы, можно внести на влажную поверхность почвы без значительных потерь азота в течение нескольких дней.
РЕКОМЕНДАЦИИ ПО АЗОТНОМУ ПИТАНИЮ ПРОПАШНЫХ КУЛЬТУР ПРИ ВЫСОКОЙ ВЕРОЯТНОСТИ ЗАТОПЛЕНИЯ
Правда конца – это тоже возможность начала.Кто осознал пораженье, – того не разбили…Самое страшное – это инерция стиля.(Н. Коржавин)
— Вносить удобрения, содержащие преимущественно аммонийный или амидный азот. То есть использовать безводный аммиак, аммиачную воду, карбамид, сульфат аммония или КАС.— Вносить удобрения непосредственно перед посевом для исключения нитрификации аммонийного азота и его преобразования в мобильную нитратную форму.— При высокой вероятности обильных осадков после посева заранее планировать дробное внесение азотных удобрений. При использовании нитратных удобрений (аммиачной или кальциевой селитры) их целесообразно вносить в междурядья вегетирующей кукурузы до формирования на растениях 6 листьев.— При затоплении или переувлажнении поля необходимо оценить потери азота в зависимости от сложившихся условий (продолжительность периода переувлажнения, температура почвы и воздуха, степень дренирования почвы), а также количества и формы внесенного в минеральных удобрениях азота.— При необходимости срочно компенсировать дефицит азота целесообразно провести поверхностную подкормку разбрасывателем. Можно использовать гранулированный сульфат аммония или карбамид. При внесении карбамида на влажную почву оправдано использование ингибиторов уреазы.— На быстро высыхающих полях целесообразно компенсировать потерянный азот за счет внесения в междурядья КАС или аммиачной селитры.
Александр Гончаров специально для «Инфоиндустрии»
infoindustria.com.ua