Свойства и применение кислорода. Применение кислорода
Кислород (O, Oxygenium) - влияние на организм, польза и вред, описание
История кислорода
Открытие кислорода произошло дважды, во второй половине XVIII столетия с разницей в несколько лет. В 1771 году кислород получил швед Карл Шееле, нагревая селитру и серную кислоту. Полученный газ был назван «огненным воздухом». В 1774 английский химик Джозеф Пристли проводил процесс разложения оксида ртути в полностью закрытом сосуде и открыл кислород, но принял его за ингредиент воздуха. Только после того, как Пристли поделился своей находкой с французом Антуаном Лавуазье, стало понятно, что открыт новый элемент (calorizator). Пальма первенства данного открытия принадлежит Пристли потому, что Шееле опубликовал свой научный труд с описанием открытия лишь в 1777 году.
Общая характеристика кислорода
Кислород является элементом XVI группы II периода периодической системы химических элементов Д.И. Менделеева, имеет атомный номер 8 и атомную массу 15,9994. Принято обозначать кислород символом О (от латинского Oxygenium – порождающий кислоту). В русском языке название кислород стало производным от кислоты, термина, который был введён М.В. Ломоносовым.

Нахождение в природе
Кислород является самым распространённым элементом по нахождению в земной коре и Мировом океане. Соединения кислорода (в основном – силикаты) составляют не менее 47% массы земной коры, кислород вырабатывается в процессе фотосинтеза лесами и всеми зелёными растениями, большая часть приходится на фитопланктон морских и пресных вод. Кислород – обязательная составная часть любых живых клеток, также находится в большинстве веществ органического происхождения.
Физические и химические свойства
Кислород – лёгкий неметалл, состоит в группе халькогенов, имеет высокую химическую активность. Кислород, как простое вещество, представляет собой газ без цвета, запаха и вкуса, имеет жидкое состояние – светло-голубая прозрачная жидкость и твёрдое – светло-синие кристаллы. Состоит из двух атомов кислорода (обозначается формулой О₂).
Полезные свойства кислорода и его влияние на организм
Кислород участвует в окислительно-восстановительных реакциях. Живые существа дышат кислородом воздуха. Широко используется кислород в медицине. При сердечнососудистых заболеваниях, для улучшения обменных процессов, в желудок вводят кислородную пену («кислородный коктейль»). Подкожное введение кислорода используют при трофических язвах, слоновости, гангрене. Для обеззараживания и дезодорации воздуха и очистки питьевой воды применяют искусственное обогащение озоном.

Биологическая роль кислорода
Кислород – основа основ жизнедеятельности всех живых организмов на Земле, является основным биогенным элементом. Находится в составе молекул всех важнейших веществ, которые отвечают за структуру и функции клеток (липиды, белки, углеводы, нуклеиновые кислоты). Каждый живой организм содержит гораздо больше кислорода, чем какого-либо элемента (до 70%). Для примера, организм взрослого среднестатического человека массой 70 кг содержит 43 кг кислорода.
Кислород поступает в живые организмы (растения, животные и человек) благодаря органам дыхания и поступлению воды. Помня о том, что в организме человека самый главный орган дыхания – это кожа, становится понятно, сколько кислорода может получать человек, особенно летом на берегу водоёма. Определить потребность человека в кислороде достаточно сложно, ведь она зависит от многих факторов – возраст, пол, масса и поверхность тела, система питания, внешняя среда и т.д.
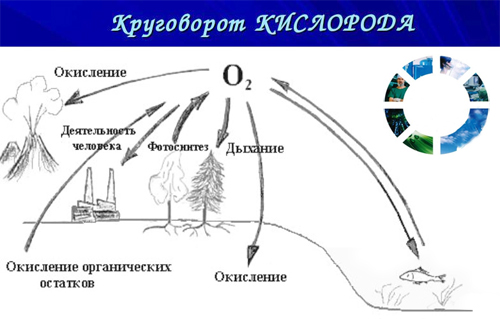
Применение кислорода в жизни
Кислород применяется практически повсеместно – от металлургии до производства ракетного топлива и взрывчатых веществ, применяемых для дорожных работах в горах; от медицины до пищевой промышленности.
В пищевой промышленности кислород зарегистрирован в качестве пищевой добавки E941, как пропеллент и упаковочный газ.
Автор: Виктория Н. (специально для Calorizator.ru)Копирование данной статьи целиком или частично запрещено.
www.calorizator.ru
Сообщение о применении кислорода | Kratkoe.com

Доклад на тему «Применение кислорода» кратко изложенное в этой статье, расскажет Вам о сферах промышленности, в которых это невидимое вещество приносит невероятную пользу.
Сообщение о применении кислорода
Кислород является неотъемлемой частью жизнедеятельности всех живых организмов и химических процессов на планете. В этой статье мы рассмотрим наиболее частые области применения кислорода:
Применение кислорода в медицине
В данной области он чрезвычайно важен: химический элемент используется для жизненного поддержания людей, страдающих на затрудненное дыхание и для лечения некоторых недугов. Примечательно, что при нормальном давлении чистым кислородом дышать долго нельзя. Это небезопасно для здоровья.
Применение кислорода в стекольной промышленности
Данный химический элемент в стекловаренных печах используется в качестве компонента, улучшающего горение в них. Также благодаря кислороду промышленность уменьшает выбросы оксидов азота до уровня безопасных для жизни.
Применение кислорода в целлюлозно–бумажной промышленности
Данный химический элемент используется при спиртовании, делигнификации и в других процессах, таких как:
- Отбеливание бумаги
- Очистка сточных вод
- Подготовка питьевой воды
- Интенсификация горения мусоросжигательных печей
- Переработка покрышек
Применение кислорода в авиации
Поскольку человек не может дышать вне атмосферы без кислорода, то ему необходимо брать запас данного полезного элемента с собой. Искусственно полученный кислород используется людьми для дыхания в чуждой среде: в авиации при полетах, в космических аппаратах.
Применение кислорода в природе
В природе существует круговорот кислорода: в процессе фотосинтеза растения на свету превращают углекислый газ и воду в органические соединения. Данный процесс характеризуется выделением кислорода. Как человек и животные, растения в темное время суток потребляют кислород из атмосферы. Круговорот кислорода в природе определяется тем, что человек и животные потребляют кислород, а растения производят его днем и расходуют ночью.
Применение кислорода в металлургии
Для химической и металлургической промышленности нужен чистый кислород, а не атмосферный. В мире каждый год предприятия получают больше 80 млн. тонн данного химического элемента. Он израсходуется в процессе получения стали из металлолома и чугуна.
Какое применение кислорода в машиностроении?
В строительстве и машиностроении он используется для резки и сварки металлов. Данные процессы осуществляются при высоких температурах.
Применение кислорода в жизни
В жизни человек использует кислород в различных сферах, таких как:
- Выращивание рыбы в прудовых хозяйствах (вода насыщается кислородом).
- Обработка воды во время изготовления пищевых продуктов.
- Обеззараживание хранилищ и производственных помещений кислородом.
- Разработка кислородных коктейлей для животных, чтобы те прибавляли в весе.
Применение кислорода человеком в электроэнергии
Тепловые и электрические станции, которые работают на нефти, природном газе или угле, для сжигания топлива используют кислород. Без него все производственные промышленные заводы просто бы не работали.
Надеемся, что сообщение на тему «Применение кислорода» помогло Вам подготовиться к занятию. А рассказ о применении кислорода Вы можете дополнить через форму комментариев ниже.
kratkoe.com
Применение кислорода - Наука и образование
Первые исследователи кислорода заметили, что в его атмосфере легче дышится. Они предсказывали широкое применение этого живительного газа в медицине и даже в повседневной жизни как средства, усиливающего жизнедеятельность человеческого организма.
Но при более углублённом изучении оказалось, что длительное вдыхание чистого кислорода человеком может вызвать заболевание и даже смерть: организм человека не приспособлен к жизни в чистом кислороде.
В настоящее время чистый кислород применяется для вдыхания лишь в некоторых случаях: например, тяжело больным туберкулёзом лёгких предлагают вдыхать кислород небольшими порциями. Аэронавты и лётчики при высотных полётах пользуются кислородными приборами. Бойцы горноспасательных отрядов часто принуждены работать в атмосфере, лишённой кислорода. Для дыхания они используют прибор, в котором сохраняется нужный для дыхания состав воздуха добавлением кислорода из баллонов, находящихся в том же приборе.
Основная масса получаемого в промышленности кислорода применяется в настоящее время для сжигания в нём различных веществ с целью получения очень высокой температуры.
Например, горючий газ ацетилен (C2h3) смешивают с кислородом и сжигают в особых горелках. Пламя этой горелки имеет такую высокую температуру, что в нём плавится железо. Поэтому кислородно-ацетиленовой горелкой пользуются для сварки стальных изделий. Такая сварка называется автогенной.
Жидкий кислород применяется для приготовления взрывчатых смесей. Особые патроны набивают измельчённой древесиной (древесной мукой) или другими измельчёнными горючими веществами и смачивают эту горючую массу жидким кислородом. При поджигании такой смеси горение происходит очень быстро, образуется большое количество газов, нагретых до очень высокой температуры. Давлением этих газов могут быть взорваны скалы, или выброшено большое количество грунта. Этой взрывчатой смесью пользуются при строительстве каналов, при проходке тоннелей и пр.
В последнее время кислород добавляют к воздуху для повышения температуры в печах при выплавке чугуна и стали. Благодаря этому ускоряется выплавка стали и повышается её качество.
Следует заметить, что кислород приносит не только пользу, но и вред современному человеку: он окисляет и тем портит металлические изделия. Особенно много гибнет железа от ржавления, в котором кислород принимает активное участие.
Современная наука решает вопросы не только о том, как получить и лучше использовать кислород, но также и о том, как защитить некоторые вещества я предметы от химического действия кислорода.
Получить кислород можно из сложных веществ или из воздуха. В небольших количествах для учебных целей получают кислород разложением некоторых сложных веществ, например марганцевокислого калия KMnO4.
Так как кислород немного тяжелее воздуха, то он собирается сначала на дне стеклянной банки и вытесняет из неё воздух. Чтобы следить за наполнением банки кислородом, нужно опускать в неё тлеющую лучинку: лучинка загорается ,в той части банки, которая заполнилась кислородом.
Для промышленных целей кислород получают в больших количествах из воздуха или из воды.
Источник: Д.М. Кирюшкин, учебник уроков по химии для 7 класса средней школы.
Применение кислорода. Методическая разработка
Урок посвящен изучению основных областей применения кислорода. Из материалов урока вы узнаете, на каких свойствах кислорода основано его применение в металлургии, медицине, пищевой промышленности и других областях.
Тема: Вещества и их превращения
Урок: Применение кислорода
1. В металлургии, для резки и сварки металлов
Применение любого вещества связано с его свойствами. Так и применение кислорода обусловлено, в основном, его способностями поддерживать дыхание и обеспечивать горение.
Рассмотрим основные области применения кислорода.
В МЕТАЛЛУРГИИ, ДЛЯ РЕЗКИ И СВАРКИ МЕТАЛЛОВ
Кислород используют в металлургии при производстве стали. Также, во многих металлургических агрегатах для более эффективного сжигания топлива вместо воздуха в горелках используют кислородо-воздушную смесь, т. е. обогащают воздух кислородом.

Рис. 1. Производство стали
Кислород в баллонах широко используется для газопламенной резки и сварки металлов. Горючий газ ацетилен, сгорая в токе кислорода, позволяет получить температуру выше 3000°С! Это приблизительно вдвое больше температуры плавления железа.
2. Окислитель топлива
Кислород, входящий в состав воздуха, применяют для сжигания топлива: например, в двигателях автомобилей, тепловозов и теплоходов.
В качестве окислителя для ракетного топлива применяется жидкий кислород. Смесь жидкого кислорода и жидкого озона — один из самых мощных окислителей ракетного топлива.
3. Применение в медицинских целях
В медицине кислород тоже нашел свое применение. Кислород используется для обогащения дыхательных газовых смесей при нарушении дыхания, для лечения астмы, профилактики гипоксии в виде кислородных коктейлей, кислородных подушек. Однако чистым кислородом при нормальном давлении долго дышать нельзя – это опасно для здоровья.
4. Применение в пищевой промышленности
В пищевой промышленности кислород зарегистрирован в качестве пищевой добавки E948, как пропеллент и упаковочный газ. Пропелленты — газы, выдавливающие пищевые продукты из ёмкости (контейнера, баллончика со спреем, танка или хранилища для сыпучих продуктов).
5. Биологическая роль
Кислород выполняет бесценную биологическую роль.
Кислород необходим практически всем живым существам для дыхания. Дыхание – это окислительно-восстановительный процесс, где кислород является окислителем. С помощью дыхания живые существа вырабатывают энергию, необходимую для поддержания жизни.
6. Обобщение
 |
Рис. 2. Основные области применения кислорода
Список рекомендованной литературы
1. Сборник задач и упражнений по химии: 8-й кл.: к учеб. П. А. Оржековского и др. «Химия. 8 класс» / П. А. Оржековский, Н. А. Титов, Ф. Ф. Гегеле. – М.: АСТ: Астрель, 2006. (с.70-84)
2. Ушакова О. В. Рабочая тетрадь по химии: 8-й кл.: к учебнику П. А. Оржековского и др. «Химия. 8 класс» / О. В. Ушакова, П. И. Беспалов, П. А. Оржековский; под. ред. проф. П. А. Оржековского - М.: АСТ: Астрель: Профиздат, 2006. (с. 70-72)
3. Химия. 8 класс. Учеб. для общеобр. учреждений / П. А. Оржековский, Л. М. Мещерякова, М. М. Шалашова. – М.:Астрель, 2013. (§22)
4. Химия: 8-й класс: учеб. для общеобр. учреждений / П. А. Оржековский, Л. М. Мещерякова, Л. С. Понтак. М.: АСТ: Астрель, 2005. (§28)
5. Химия: неорган. химия: учеб. для 8кл. общеобр. учрежд. /Г. Е. Рудзитис, Ф. Г. Фельдман. – М.: Просвещение, ОАО «Московские учебники», 2009. (§21)
6. Энциклопедия для детей. Том 17. Химия / Глав. ред. В.А. Володин, вед. науч. ред. И. Леенсон. – М.: Аванта+, 2003.
Дополнительные веб-ресурсы
1. Тесты по химии (онлайн) .
2. Единая коллекция цифровых образовательных ресурсов: .
3. Получение и применение кислорода .
4. Применение кислорода .
Домашнее задание:
1) с. 70-72 №№ 1,2,4 из Рабочей тетради по химии: 8-й кл.: к учебнику П. А. Оржековского и др. «Химия. 8 класс» / О. В. Ушакова, П. И. Беспалов, П. А. Оржековский; под. ред. проф. П. А. Оржековского - М.: АСТ: Астрель: Профиздат, 2006.
2) с.128 №№ 5,8 из учебника П. А. Оржековского, Л. М. Мещеряковой, М. М. Шалашовой «Химия: 8кл.», 2013 г.
dp-adilet.kz
Кислород — Мегаэнциклопедия Кирилла и Мефодия — статья
В свободном виде кислород — газ без цвета, запаха и вкуса.
История открытия кислорода, как и азота, связана с продолжавшимся несколько веков изучением атмосферного воздуха. О том, что воздух по своей природе не однороден, а включает части, одна из которых поддерживает горение и дыхание, а другая — нет, знали еще в 8 веке китайский алхимик Мао Хоа, а позднее в Европе — Леонардо да Винчи. В 1665 английский естествоиспытатель Р. Гук писал, что воздух состоит из газа, содержащегося в селитре, а также из неактивного газа, составляющего большую часть воздуха. О том, что воздух содержит элемент, поддерживающий жизнь, в 18 веке было известно многим химикам. Шведский аптекарь и химик Карл Шееле начал изучать состав воздуха в 1768. В течение трех лет он разлагал нагреванием селитры (KNO3, NaNO3) и другие вещества и получал «огненный воздух», поддерживающий дыхание и горение. Но результаты своих опытов Шееле обнародовал только в 1777 году в книге «Химический трактат о воздухе и огне». В 1774 английский священник и натуралист Дж. Пристли нагреванием «жженой ртути» (оксида ртути HgO) получил газ, поддерживающий горение. Будучи в Париже, Пристли, не знавший, что полученный им газ входит в состав воздуха, сообщил о своем открытии А. Лавуазье и другим ученым. К этому времени был открыт и азот. В 1775 Лавуазье пришел к выводу, что обычный воздух состоит из двух газов — газа, необходимого для дыхания и поддерживающего горение, и газа «противоположного характера» — азота. Лавуазье назвал поддерживающий горение газ oxygene — «образующий кислоты» (от греч. oxys — кислый и gennao — рождаю; отсюда и русское название «кислород»), так как он тогда считал, что все кислоты содержат кислород. Давно уже известно, что кислоты бывают как кислородсодержащими, так и бескислородными, но название, данное элементу Лавуазье, осталось неизменным. На протяжении почти полутора веков 1/16 часть массы атома кислорода служила единицей сравнения масс различных атомов между собой и использовалась при численной характеристике масс атомов различных элементов (так называемая кислородная шкала атомных масс).Кислород — самый распространенный на Земле элемент, на его долю (в составе различных соединений, главным образом силикатов), приходится около 47, 4% массы твердой земной коры. Морские и пресные воды содержат огромное количество связанного кислорода — 88, 8% (по массе), в атмосфере содержание свободного кислорода составляет 20, 95 % (по объему). Элемент кислород входит в состав более 1500 соединений земной коры.В настоящее время кислород в промышленности получают за счет разделения воздуха при низких температурах. Сначала воздух сжимают компрессором, при этом воздух разогревается. Сжатому газу дают охладиться до комнатной температуры, а затем обеспечивают его свободное расширение. При расширении температура газа резко понижается. Охлажденный воздух, температура которого на несколько десятков градусов ниже температуры окружающей среды, вновь подвергают сжатию до 10-15 МПа. Затем снова отбирают выделившуюся теплоту. Через несколько циклов «сжатие—расширение» температура падает ниже температуры кипения и кислорода, и азота. Образуется жидкий воздух, который затем подвергают перегонке (дистилляции). Температура кипения кислорода (–182, 9°C) более чем на 10 градусов выше, чем температура кипения азота (–195, 8°C). Поэтому из жидкости азот испаряется первым, а в остатке накапливается кислород. За счет медленной (фракционной) дистилляции удается получить чистый кислород, в котором содержание примеси азота составляет менее 0, 1 объемного процента.
Еще более чистый кислород можно получить при электролизе водных растворов щелочей (NaOH или KOH) или солей кислородсодержащих кислот (обычно используют раствор сульфата натрия Na2SO4). В лаборатории небольшие количества не очень чистого кислорода можно получить при нагревании перманганата калия KMnO4:
2KMnO4 = K2MnO4 + MnO2 + O2.
Более чистый кислород получают разложением пероксида водорода Н2О2 в присутствии каталитических количеств твердого диоксида марганца MnO2:
2Н2О2 = 2Н2О + О2.
Кислород образуется при сильном (выше 600°C) прокаливании нитрата натрия NaNO3:
2NaNO3 =2NaNO2 + О2,
при нагревании некоторых высших оксидов:
4CrO3= 2Cr2O3 + 3О2;
2PbO2 = 2PbO + О2;
3MnO2 = Mn3O4 + О2.
Ранее кислород получали разложением бертолетовой соли KClO3 в присутствии каталитических количеств диоксида марганца MnO2:2KClO3 = 2KCl + 3О2.
Однако бертолетова соль образует взрывчатые смеси, поэтому ее для получения кислорода в лабораториях теперь не используют. Разумеется, сейчас никому в голову не придет использовать для получения кислорода прокаливание оксида ртути HgO, так как образующийся в этой реакции кислород загрязнен ядовитыми парами ртути.
Источником кислорода в космических кораблях, подводных лодках и т. п. замкнутых помещениях служит смесь пероксида натрия Na2O2 и супероксида калия KO2. При взаимодействии этих соединений с углекислым газом освобождается кислород:
2Na2O2 + 2CO2 = 2Na2CO3 + O2,
4КО2 + 2СО2 = 2К2СО3 + 3О2.
Если использовать смесь Na2O2 и КО2, взятых в молярном отношении 1:1, то на каждый моль поглощенного из воздуха углекислого газа будет выделяться 1 моль кислорода, так что состав воздуха не будет изменяться за счет поглощения при дыхании кислорода и выделения СО2.
Атмосферный кислород состоит из двухатомных молекул. Межатомное расстояние в молекуле О2 0, 12074 нм. Молекулярный кислород (газообразный и жидкий) — парамагнитное вещество, в каждой молекуле О2 имеется по 2 неспаренных электрона. Этот факт можно объяснить тем, что в молекуле на каждой из двух разрыхляющих орбиталей находится по одному неспаренному электрону.
Энергия диссоциации молекулы О2 на атомы довольно высока и составляет 493, 57 кДж/моль.
При нормальных условиях плотность газа кислорода 1, 42897 кг/м3. Температура кипения жидкого кислорода (жидкость имеет голубой цвет) –182, 9°C. При температурах от –218, 7°C до –229, 4°C существует твердый кислород с кубической решеткой (α-модификация), при температурах от –229, 4°C до –249, 3°C — β-модификация с гексагональной решеткой и при температурах ниже –249, 3°C — кубическая γ-модификация. При повышенном давлении и низких температурах получены и другие модификации твердого кислорода.
При 20°C растворимость газа О2: 3, 1 мл на 100 мл воды, 22 мл на 100 мл этанола, 23, 1 мл на 100 мл ацетона. Существуют органические фторсодержащие жидкости (например, перфторбутилтетрагидрофуран), в которых растворимость кислорода значительно более высокая.
Высокая прочность химической связи между атомами в молекуле О2приводит к тому, что при комнатной температуре газообразный кислород химически довольно малоактивен. В природе он медленно вступает в превращения при процессах гниения. Кроме того, кислород при комнатной температуре способен реагировать с гемоглобином крови (точнее с железом II гема), что обеспечивает перенос кислорода от органов дыхания к другим органам.Со многими веществами кислород вступает во взаимодействие без нагревания, например, с щелочными и щелочноземельными металлами (образуются соответствующие оксиды типа Li2O, CaO и др., пероксиды типа Na2O2, BaO2 и др. и супероксиды типа КО2, RbO2 и др.), вызывает образование ржавчины на поверхности стальных изделий. Без нагревания кислород реагирует с белым фосфором, с некоторыми альдегидами и другими органическими веществами.
При нагревании, даже небольшом, химическая активность кислорода резко возрастает. При поджигании он реагирует со взрывом с водородом, метаном, другими горючими газами, с большим числом простых и сложных веществ. Известно, что при нагревании в атмосфере кислорода или на воздухе многие простые и сложные вещества сгорают, причем образуются различные оксиды, например:
S+O2 = SO2; С + O2 = СО2
4Fe + 3O2 = 2Fe2O3; 2Cu + O2 = 2CuO
4Nh4 + 3O2 = 2N2 + 6h3O; 2h3S + 3O2 = 2h3O + 2SO2
Если смесь кислорода и водорода хранить в стеклянном сосуде при комнатной температуре, то экзотермическая реакция образования воды
2Н2 + О2= 2Н2О + 571 кДжпротекает крайне медленно; по расчету, первые капельки воды должны появиться в сосуде примерно через миллион лет. Но при внесении в сосуд со смесью этих газов платины или палладия (играющих роль катализатора), а также при поджигании реакция протекает со взрывом.
С азотом N2 кислород реагирует или при высокой температуре (около 1500-2000°C), или при пропускании через смесь азота и кислорода электрического разряда. При этих условиях обратимо образуется оксид азота (II):
N2 + O2 = 2NO
Возникший NO затем реагирует с кислородом с образованием бурого газа (диоксида азота):
2NO + О2 = 2NO2
Из неметаллов кислород напрямую ни при каких условиях не взаимодействует с галогенами, из металлов — с благородными металлами серебром, золотом, платиной и др.
Бинарные соединения кислорода, в которых степень окисления атомов кислорода равна –2, называют оксидами (прежнее название — окислы). Примеры оксидов: оксид углерода (IV) CO2, оксид серы (VI) SO3, оксид меди (I) Cu2O, оксид алюминия Al2O3, оксид марганца (VII) Mn2O7.Кислород образует также соединения, в которых его степень окисления равна –1. Это — пероксиды (старое название — перекиси), например, пероксид водорода Н2О2, пероксид бария ВаО2, пероксид натрия Na2O2 и другие. В этих соединениях содержится пероксидная группировка — О — О —. С активными щелочными металлами, например, с калием, кислород может образовывать также супероксиды, например, КО2 (супероксид калия), RbO2 (супероксид рубидия). В супероксидах степень окисления кислорода –1/2. Можно отметить, что часто формулы супероксидов записывают как К2О4, Rb2O4 и т.д.
С самым активным неметаллом фтором кислород образует соединения в положительных степенях окисления. Так, в соединении O2F2 степень окисления кислорода +1, а в соединении O2F — +2. Эти соединения принадлежат не к оксидам, а к фторидам. Фториды кислорода можно синтезировать только косвенным путем, например, действуя фтором F2 на разбавленные водные растворы КОН.
Применение кислорода очень разнообразно. Основные количества получаемого из воздуха кислорода используются в металлургии. Кислородное (а не воздушное) дутье в домнах позволяет существенно повышать скорость доменного процесса, экономить кокс и получать чугун лучшего качества. Кислородное дутье применяют в кислородных конвертерах при переделе чугуна в сталь (см. ст. Железо). Чистый кислород или воздух, обогащенный кислородом, используется при получении и многих других металлов (меди, никеля, свинца и др.). Кислород используют при резке и сварке металлов. При этом применяют «баллонный» кислород. В баллоне кислород может находиться под давлением до 15 МПа. Баллоны с кислородом окрашены в голубой цвет.Жидкий кислород — мощный окислитель, его используют как компонент ракетного топлива. Пропитанные жидким кислородом такие легко окисляющиеся материалы, как древесные опилки, вата, угольный порошок и др. (эти смеси называют оксиликвитами), используют как взрывчатые вещества, применяемые, например, при прокладке дорог в горах.Кислород в атмосфере Земли начал накапливаться в результате деятельности первичных фотосинтезирующих организмов, появившихся, вероятно, около 2, 8 млрд. лет назад. Полагают, что 2 млрд. лет назад атмосфера уже содержала около 1% кислорода; постепенно из восстановительной она превращалась в окислительную и примерно 400 млн. лет назад приобрела современный состав. Наличие в атмосфере кислорода в значительной степени определило характер биологической эволюции. Аэробный (с участием О2) обмен веществ возник позже анаэробного (без участия О2), но именно реакции биологического окисления, более эффективные, чем древние энергетические процессы брожения и гликолиза, снабжают живые организмы большей частью необходимой им энергии. Исключение составляют облигатные анаэробы, например, некоторые паразиты, для которых кислород является ядом. Использование кислорода, обладающего высоким окислительно-восстановительным потенциалом, в качестве конечного акцептора электронов в цепи дыхательных ферментов, привело к возникновению биохимического механизма дыхания современного типа. Этот механизм и обеспечивает энергией аэробные организмы.
Кислород — основной биогенный элемент, входящий в состав молекул всех важнейших веществ, обеспечивающих структуру и функции клеток — белков, нуклеиновых кислот, углеводов, липидов, а также множества низкомолекулярных соединений. В каждом растении или животном кислорода гораздо больше, чем любого другого элемента (в среднем около 70%). Мышечная ткань человека содержит 16% кислорода, костная ткань — 28.5%; всего в организме среднего человека (масса тела 70 кг) содержится 43 кг кислорода. В организм животных и человека кислород поступает в основном через органы дыхания (свободный кислород) и с водой (связанный кислород). Потребность организма в кислороде определяется уровнем (интенсивностью) обмена веществ, который зависит от массы и поверхности тела, возраста, пола, характера питания, внешних условий и др. В экологии как важную энергетическую характеристику определяют отношение суммарного дыхания (то есть суммарных окислительных процессов) сообщества организмов к его суммарной биомассе.Небольшие количества кислорода используют в медицине: кислородом (из так называемых кислородных подушек) дают некоторое время дышать больным, у которых затруднено дыхание. Нужно, однако, иметь в виду, что длительное вдыхание воздуха, обогащенного кислородом, опасно для здоровья человека. Высокие концентрации кислорода вызывают в тканях образование свободных радикалов, нарушающих структуру и функции биополимеров. Сходным действием на организм обладают и ионизирующие излучения. Поэтому понижение содержания кислорода (гипоксия) в тканях и клетках при облучении организма ионизирующей радиацией обладает защитным действием — так называемый кислородный эффект. Этот эффект используют в лучевой терапии: повышая содержание кислорода в опухоли и понижая его содержание в окружающих тканях усиливают лучевое поражение опухолевых клеток и уменьшают повреждение здоровых. При некоторых заболеваниях применяют насыщение организма кислородом под повышенным давлением — гипербарическую оксигенацию.- Разумовский С. Д. Кислород — элементарные формы и свойства. М. 1979.
- Разумовский С. Д. Кислород - элементарные формы и свойства. М., 1979.
- Проссер Л. Кислород, дыхание и метаболизм // В кн.: Сравнительная физиология животных: пер. с англ. Т. 1. М., 1977.
- Термодинамические свойства кислорода. М., 1981.
megabook.ru
Применение кислорода - Helperia
Публичная статья
582
Создано 25 декабря 2016 года
В металлургии, для резки и сварки металлов
Применение любого вещества связано с его свойствами. Так и применение кислорода обусловлено, в основном, его способностями поддерживать дыхание и обеспечивать горение.
Рассмотрим основные области применения кислорода.
В МЕТАЛЛУРГИИ, ДЛЯ РЕЗКИ И СВАРКИ МЕТАЛЛОВ
Кислород используют в металлургии при производстве стали. Также, во многих металлургических агрегатах для более эффективного сжигания топлива вместо воздуха в горелках используют кислородо-воздушную смесь, т.е. обогащают воздух кислородом.
Кислород в баллонах широко используется для газопламенной резки и сварки металлов. Горючий газ ацетилен, сгорая в токе кислорода, позволяет получить температуру выше 3000°С! Это приблизительно вдвое больше температуры плавления железа.
Окислитель топлива
Кислород, входящий в состав воздуха, применяют для сжигания топлива: например, в двигателях автомобилей, тепловозов и теплоходов.
В качестве окислителя для ракетного топлива применяется жидкий кислород. Смесь жидкого кислорода и жидкого озона — один из самых мощных окислителей ракетного топлива.
Применение в медицинских целях
В медицине кислород тоже нашел свое применение. Кислород используется для обогащения дыхательных газовых смесей при нарушении дыхания, для лечения астмы, профилактики гипоксии в виде кислородных коктейлей, кислородных подушек. Однако чистым кислородом при нормальном давлении долго дышать нельзя – это опасно для здоровья.
Применение в пищевой промышленности
В пищевой промышленности кислород зарегистрирован в качестве пищевой добавки E948, как пропеллент и упаковочный газ. Пропелленты — газы, выдавливающие пищевые продукты из ёмкости (контейнера, баллончика со спреем, танка или хранилища для сыпучих продуктов).
Биологическая роль
Кислород выполняет бесценную биологическую роль.
Кислород необходим практически всем живым существам для дыхания. Дыхание – это окислительно-восстановительный процесс, где кислород является окислителем. С помощью дыхания живые существа вырабатывают энергию, необходимую для поддержания жизни.
Список рекомендованной литературы
1. Сборник задач и упражнений по химии: 8-й кл.: к учеб. П.А. Оржековского и др. «Химия. 8 класс» / П.А. Оржековский, Н.А. Титов, Ф.Ф. Гегеле. – М.: АСТ: Астрель, 2006. (с.70-84)
2. Ушакова О.В. Рабочая тетрадь по химии: 8-й кл.: к учебнику П.А. Оржековского и др. «Химия. 8 класс» / О.В. Ушакова, П.И. Беспалов, П.А. Оржековский; под. ред. проф. П.А. Оржековского - М.: АСТ: Астрель: Профиздат, 2006. (с. 70-72)
3. Химия. 8 класс. Учеб. для общеобр. учреждений / П.А. Оржековский, Л.М. Мещерякова, М.М. Шалашова. – М.:Астрель, 2013. (§22)
4. Химия: 8-й класс: учеб. для общеобр. учреждений / П.А. Оржековский, Л.М. Мещерякова, Л.С. Понтак. М.: АСТ: Астрель, 2005. (§28)
5. Химия: неорган. химия: учеб. для 8кл. общеобр. учрежд. /Г.Е. Рудзитис, Ф.Г. Фельдман. – М.: Просвещение, ОАО «Московские учебники», 2009. (§21)
6. Энциклопедия для детей. Том 17. Химия / Глав. ред.В.А. Володин, вед. науч. ред. И. Леенсон. – М.: Аванта , 2003.
Источник
helperia.ru
Свойства и применение кислорода

Разделы: Химия, Конкурс «Презентация к уроку»
Презентация к уроку
Загрузить презентацию (7,2 МБ)
Внимание! Предварительный просмотр слайдов используется исключительно в ознакомительных целях и может не давать представления о всех возможностях презентации. Если вас заинтересовала данная работа, пожалуйста, загрузите полную версию.
Цель урока: изучить физические и химические свойства кислорода, дать общее понятие об оксидах, реакциях горения; рассмотреть практическую значимость и применение; доказать, что кислород - один из важнейших элементов на Земле.
Задачи урока:
Образовательные:
- Расширить представления обучающихся о кислороде.
- Познакомить со свойствами и применением кислорода.
- Совершенствовать умения составлять уравнения химических реакций.
Воспитательные:
- Формировать умения работать в парах у каждого обучающегося, считаться с мнением соседа и отстаивать свою точку зрения корректно, выполняя упражнения.
- Воспитывать бережное отношение к своему здоровью, окружающей природе, учить понимать прекрасное, ценить произведения искусства.
Развивающие:
- Способствовать продолжению развития устойчивого интереса к химической науке и практике.
- Совершенствовать навыки самостоятельной работы, развивать умения наблюдать, формулировать высказывания.
- Способствовать развитию исследовательских навыков, соблюдая правила техники безопасности.
- Совершенствовать умения обобщать и делать выводы.
Планируемые результаты:
- личностные: готовность и способность учащихся к саморазвитию, самоопределению; ответственное отношение к учению; способность ставить цели и строить жизненные планы; формирование коммуникативной культуры, ценности здорового и безопасного образа жизни;
- метапредметные: уметь ставить цель и планировать пути её достижения, выбирая более рациональные способы решения данной проблемы; учиться корректировать свои действия в связи с изменением создавшейся ситуации; уметь создавать, применять и преобразовывать знаки и символы, модели и схемы для решения учебных и познавательных задач; уметь осознанно использовать речевые средства в соответствии с задачей коммуникации для выражения своих мыслей и потребностей; уметь организовывать совместную работу со сверстниками в парах; уметь находить информацию в различных источниках; владеть навыками самоконтроля, самооценки;
- предметные:
- знать: основные химические понятия “катализаторы”, “оксиды”, “реакции горения”, “реакции окисления”; физические и химические свойства кислорода; области применения кислорода.
- уметь: отличить кислород от других газов; составлять уравнения реакций горения веществ в кислороде; записывать химические формулы оксидов и давать им названия; объяснять, как происходит круговорот кислорода в природе.
Тип урока: урок формирования умений и навыков.
Форма работы: фронтальная,
групповая, работа в парах, игровая.Методы обучения: словесный,
частично-поисковый, наглядный, демонстрационный, интерактивный.Приемы обучения: постановка проблемных вопросов.
Оборудование: компьютер, проектор, презентация “Свойства и применение кислорода. Круговорот кислорода в природе”, колбы, пинцет, ложки для сжигания веществ, спиртовка.
Реактивы: уголь, сера, красный фосфор, железная пластина, вода, известковая вода.
ХОД УРОКА
І. Организационный момент. (1 мин.)
(Слайд № 1) Учитель: Добрый день! Прошу всех садиться. Тема сегодняшнего урока “Свойства и применение кислорода”.
(Слайд № 2) Мы с вами рассмотрим физические и химические свойства кислорода, сформулируем общие понятия об оксидах, реакциях горения, окисления; ознакомимся с практической значимостью и применением кислорода; а также докажем, что кислород - один из важнейших элементов на Земле.
ІІ. Актуализация знаний. (7 мин.).
Работа с карточками. От 2 до 4 обучающихся получают задание на карточках и выполняют его у доски.
(Слайд № 3) Фронтальный опрос “А ну-ка, химики”.
Учитель: Но перед тем как приступить к изучению новой темы, вам следует ответить на следующие вопросы:
Химический знак кислорода? Ответ: О
Относительная атомная масса кислорода? Ответ: 16.
Химическая формула кислорода? Ответ: О2.
Относительная молекулярная масса кислорода? Ответ: 32.
В соединениях кислород обычно какой валентности? Ответ: II.
Расскажите о нахождении кислорода в природе. Ответ: Кислород — самый распространенный химический элемент в земной коре. Кислород — самый распространенный на Земле элемент, на его долю приходится около 49% массы твердой земной коры. Морские и пресные воды содержат огромное количество связанного кислорода — 85,5% (по массе), в атмосфере содержание свободного кислорода составляет 21% по объёму и 23% по массе. Более 1500 соединений земной коры в своем составе содержат кислород. Кислород входит в состав многих органических веществ и присутствует во всех живых клетках. По числу атомов в живых клетках он составляет 20,9%, по массовой доле — около 65 %.
Перечислите способы получения кислорода в лаборатории? Ответ: В лаборатории кислород получают следующими способами:
1) Разложение перманганата калия. 2KMnO4 = K2MnO4+MnO2+O2
2) Разложение перекиси водорода. 2h3O2 = 2h3O + O2
3) Разложение бертолетовой соли. 2KClO3 = 2KCl + 3O2
8. Перечислите способы получения кислорода в промышленности. Ответ: В промышленности кислород получают:
1) Электролиз воды. 2h3O = 2h3 + O2
2) Из воздуха. ВОЗДУХ давление, -183oC=O2 (голубая жидкость).
В настоящее время в промышленности кислород получают из воздуха. В лабораториях небольшие количества кислорода можно получать нагреванием перманганата калия (марганцовка) KMnO4. Кислород мало растворим в воде и тяжелее воздуха, поэтому его можно получать двумя способами:
(Слайд № 4). 9. Установите соответствие между способом получения кислорода и уравнением химической реакцией. Работа в парах.
| Способы получения кислорода | Уравнения химических реакций |
| А. Разложение перманганата калия. Б. Разложение перекиси водорода. В. Разложение бертолетовой соли. Г. Электролиз воды. Д. Из воздуха. | 1) 2KClO3 = 2KCl + 3O2 2) 2h3O2 = 2h3O + O2 3) ВОЗДУХ = O2 4) 2KMnO4 = K2MnO4 + MnO2 + O2 5) 2h3O = 2h3 + O2 |
Ответ: А-4; Б-2; В-1; Г-5; Д-3.
10. Что называют катализаторами? Где эти вещества применяются? Ответ: Вещества, которые ускоряют химические реакции, но сами при этом не расходуются, называют катализаторами. Катализаторы широко применяют в химической промышленности. С их помощью удается повысить производительность химических процессов, снизить себестоимость выпускаемой продукции и более полно использовать сырье.
(Слайд № 5). На какой диаграмме распределение массовых долей элементов отвечает количественному составу (Nh5)3PO4? Ответ: 4.
ІІІ. Изучение нового материала. (12 мин.)
(Слайд № 6) Учитель: Физические свойства. Кислород - бесцветный газ, без вкуса и запаха, относительно малорастворим в воде (в 100 объемах воды при температуре 20?С растворяется 3,1 объема кислорода). Кислород немного тяжелее воздуха: 1л кислорода при нормальных условиях весит 1,43 г, а 1л воздуха — 1,29г. (Нормальные условия - сокращенно: н.у. - температура 0oС и давление 760 мм.рт.ст., или 1 атм. 0,1 МПа). При давлении 760 мм.рт.ст. и температуре -183oС кислород сжижается, а при снижении температуры до -218,8oС затвердевает.
(Слайд № 7) Химические свойства. Техника безопасности (провести инструктаж!)
Кислород при нагревании энергично реагирует со многими веществами, при этом выделяются теплота и свет. Такие реакции называют реакциями горения. Если опустить в сосуд с кислородом O2 тлеющий уголек, то он раскаляется добела и сгорает, образуя оксид углерода (IV) СO2. Чтобы определить, какое образовалось вещество, в сосуд наливают известковую воду — раствор гидроксида кальция Са(ОН)2. Она мутнеет, так как при этом образуется нерастворимый карбонат кальция СаСO3:
CO2 + Ca(OH)2 = CaCO3 + h3O
Видеодемонстрация №1 “Горение угля в кислороде” http://files.school-collection.edu.ru/dlrstore/695aa82a-e84a-fa4d-7b04-16d28ded2fbb/index.htm
(Слайд № 8) Сера горит в O2 ярким синим пламенем с образованием газа с резким запахом — оксида серы (IV)
S + O2 = SO2
Видеодемонтсрация №2 “Горение серы в кислороде” http://files.school-collection.edu.ru/dlrstore/600cd365-f9f2-ae10-56e4-98ee0af7e4c6/index.htm
(Слайд № 9) Горение фосфора в кислороде
Видеодемонстрация №3 “Горение фосфора в кислороде” http://files.school-collection.edu.ru/dlrstore/f83beda5-449d-d3dc-442c-a474a89eeca6/index.htm
Опыт следует проводить под тягой. Следует соблюдать правила обращения с нагревательными приборами. Не допускать попадания горящего фосфора на рабочую поверхность стола. Не вдыхать выделяющийся дым фосфорного ангидрида.
Фосфор Р сгорает в O2 ярким пламенем с образованием белого дыма, состоящего из твердых частиц оксида фосфора (V).
4P + 5O2 = 2P2O5
(Слайд № 10) Горение железа в кислороде
Видеодемонстрация №4 “Горение железа в кислороде” http://files.school-collection.edu.ru/dlrstore/deb6e939-f8c8-fea7-fe24-7b2c80013fd7/index.htm
В кислороде горят и такие вещества, которые обычно считают негорючими, например железо. Если к тонкой стальной проволоке прикрепить спичку, зажечь ее и опустить в сосуд с кислородом, то от спички загорится и железо. Горение железа происходит с треском и разбрасыванием ярких раскаленных искр — расплавленных капель железной окалины Fe3O4. В этом соединении два атома железа трехвалентны и один двухвалентен. Поэтому реакцию горения железа в кислороде можно выразить следующим уравнением:
3Fe + 2O2 = FeO * Fe2O3 или Fe3O4
(Слайд № 11) Взаимодействие вещества с кислородом относится к реакциям окисления.
(Слайд № 12) Горение — это химическая реакция, при которой происходит окисление веществ с выделением теплоты и света.
(Слайд № 13) В большинстве случаев при взаимодействии веществ с кислородом образуются оксиды. Оксиды — это сложные вещества, которые состоят из двух элементов, одним из которых является кислород.
(Слайд № 14) Известны химические элементы, которые непосредственно с кислородом не соединяются. К ним относятся золото Au и некоторые другие. Оксиды этих элементов получают косвенным путем.
(Слайд № 15) Применение кислорода. Основано на его химических свойствах. В больших количествах кислород используют для ускорения химических реакций в разных отраслях химической промышленности и в металлургии. Например, при выплавке чугуна для повышения производительности доменных печей в них подают воздух, обогащенный кислородом.
(Слайд № 16) При сжигании смеси ацетилена или водорода с кислородом в специальных горелках температура пламени достигает 3000oС. Такое пламя используется для сварки металлов. Если берут кислород в избытке, то пламенем можно резать металл.
(Слайд № 17) Жидкий кислород применяют в ракетных двигателях.
(Слайд № 18) В медицине кислород служит для облегчения затрудненного дыхания. В этом случае кислородом заполняют специальные подушки. Кислородные маски необходимы в высотных полетах, в космосе и при работе под водой.
Кислород расходуется в громадных количествах на многие химические реакции, например на сжигание топлива.
(Слайд № 19) Из сказанного видно, что очень много кислорода расходуется на разнообразную деятельность человека, тратится на процессы дыхания человека, животных, растений, а также на процессы гниения. Человек при дыхании в течение 1 мин в среднем употребляет 0,5 дм3 кислорода, в течении суток — 720 дм3, а в год — 262,8 м3 кислорода, что все жители земного шара (5 миллиардов) в течение года для дыхания используют 1578 миллиардов кубических метров кислорода. Если такой объем кислорода при нормальном давлении поместить в железнодорожные цистерны, то поезд был бы протяженностью более 300 млн км, что равняется расстоянию до Солнца и обратно.
(Слайд № 20) Но все же общая масса кислорода в воздухе заметно не изменяется. Это объясняется процессом фотосинтеза, происходящим в зеленых растениях на свету. В результате этого процесса выделяется кислород. С фотосинтезом вы уже знакомились в курсе ботаники. Упрощенно процесс фотосинтеза изображают так:
6CO2 + 6h3O = C6h22O6 + 6O2.
Так в природе происходит непрерывный круговорот кислорода.
В целях сохранения кислорода в воздухе вокруг городов и крупных промышленных центров создаются зоны зеленых насаждений. Специальная служба систематически контролирует содержание кислорода в воздухе. При необходимости применяют меры по устранению загрязнения воздуха.
Физкультминутка. (1 мин.)
IV. Закрепление знаний. (6 мин.)
(Слайд № 21) Задание №1. “Правда или ложь? Если знаешь - разберешь”
Для кислорода верны следующие утверждения:
а) Кислород – бесцветный газ, без вкуса и запаха.
б) Кислород немного легче воздуха.
в) В кислороде горят и такие вещества, которые обычно считают негорючими, например железо.
г) Известны химические элементы, которые непосредственно с кислородом соединяются. К ним относятся золото Au и некоторые другие.
д) Применение кислорода основано на его физических свойствах.
е) Непрерывный круговорот кислорода непосредственно связан с таким процессом, как фотосинтез.
Ответ: а; в; е.
(Слайд № 22) Задание №2. “Скорая помощь”
Вставьте пропущенные вещества в уравнениях реакций:
а) ........ + Ca(OH)2 = CaCO3 + h3O
б) S + ....... = SO2
в) ..... + 2O2 = FeO * Fe2O3 или Fe3O4
Ответ: а)CO2 б)O2 в) 3Fe
(Слайд № 23) Задание №3. “Мозговой штурм”
Расставьте коэффициенты в уравнениях реакций.
а) CO2 + h3O = C6h22O6 + O2
б) P + O2 = P2O5
(Слайды № 24-25) Задание №4. “Ассоциации”
С каким применением кислорода ассоциируется данное изображение?
1) в металлургии;
2) для резки металлов;
3) в авиации для дыхания;
4) в авиации для двигателей;
5) для сварки металлов;
6) на взрывных работах;
7) в медицине.
(Слайд № 26) V. Домашнее задание. (1 мин.)
Параграф 20, 21; №6-9 (с.60). Решите задачи 1-2 (с.60).
Творческое задание: подготовить сообщение №10 с. 60 “Что делается в вашей местности для поддержания определенного содержания кислорода в воздухе? В чем может заключаться ваше участие в этой деятельности?”
(Слайд № 27) VI. Рефлексия. (1 мин.)
Учитель:
- Сегодня я узнал...
- было трудно...
- я понял, что...
- я научился...
- я смог...
- было интересно узнать, что...
- меня удивило...
- мне захотелось...
VII. Подведение итогов урока. (1 мин.)
(Слайд № 28)
В чём горят дрова и газ,Фосфор, водород, алмаз?Дышит чем любой из насКаждый миг и каждый час?Без чего мертва природа?Правильно, без....
Обучающиеся: кислорода
(Слайд № 29) Учитель: Правильно. Спасибо за урок! До свидания!
Литература
[1] Горковенко М. Ю. Поурочные разработки по химии 8 класс к учебникам О. С. Габриеляна, Л. С. Гузея, Г. Е. Рудзитиса. - М: “ВАКО”, 2004;
[2] Радецкий А. М., Горшкова В. П. Дидактический материал: химия 8-9 классы — М: Просвещение, 1997.
[3] Химия: неорганическая химия: учебник для 8 класса общеобразовательных учреждений/ Г. Е. Рудзитис, Ф.Г. Фельдман. - М: “Просвещение”, 2014 г.
Интернет-ресурсы
- http://files.school-collection.edu.ru/
- http://www.e-osnova.ru/
xn--i1abbnckbmcl9fb.xn--p1ai