31. Химические свойства неорганических веществ. Кон со2
Применение газовых смесей
Полученную таким путем необходимую концентрацию компонентов среды в дальнейшем регулируют одновременным добавлением кислорода и удалением из камеры избытков углекислого газа.
Добавление кислорода осуществляется вентилированием камеры, а отвод углекислого газа чаще всего поглощением в специальных аппаратах — скрубберах.
В качестве поглотителей, связывающих углекислый газ, первоначально использовали щелочи: едкий калий (КОН), едкий натрий (NaOH), а иногда и известковое молоко (раствор Са (ОН)2 в воде). Происходящая при этом химическая реакция основывается на превращении гидроокисей в карбонаты:
КОН + СO2 = КНСO3; КНСO3 + КОН = К2СО2 + Н2O
Однако щелочи после определенного времени использования теряют поглотительные свойства и должны заменяться. Кроме того, они вызывают быструю коррозию оборудования, что требует применения специальных материалов.
Позднее вместо щелочей стали применять сухую порошкообразную или гранулированную известь. В этом случае химическая реакция поглощения углекислого газа основывается на образовании углекислой извести:
Са(ОН)2 + СO2 = СаСO3 + Н2O
Однако возникает значительная теплота реакции и невозможна регенерация поглотителя. Отходы реакции после соответствующей обработки могут быть использованы в сельском хозяйстве в качестве удобрений.
Скруббер, работающий на сухой извести, представляет собой герметически закрытый металлический резервуар с несколькими решетчатыми полками по высоте. На полки укладывают пористые мешки с известью, предохраняющие последнюю от осыпания и уноса в камеру циркулирующим воздухом.
Такие скрубберы ввиду простоты устройства и экономичности в эксплуатации находят довольно широкое распространение на холодильниках для фруктов ряда стран. В частности, в Англии от 80 до 85% скрубберов работают на сухой извести.
В ФРГ в качестве поглощающего средства используется поташ — углекислый калий (К2СО3) — материал весьма дешевый, не имеющий запаха, не ядовитый и хорошо поддающийся регенерации с помощью наружного воздуха.
В этом случае химическая реакция процесса поглощения углекислого газа выражается уравнением:
К2СO3 + Н2O + СO2 = 2КНСO3
При регенерации раствора эта реакция происходит в обратном направлении. Установки, работающие на поташе, экономичны, не нуждаются в дополнительном тепле для регенерации, конструктивно просты и не слишком громоздки. Недостаток их — относительно низкая поглотительная способность раствора поташа.
В некоторых установках, созданных за последнее время за рубежом, применяется раствор триэтаноламина, который обладает высокими абсорбционными свойствами и может непрерывно регенерироваться с помощью электронагрева.
Процесс поглощения углекислого газа происходит в абсорбере, а регенерация раствора триэтаноламина — в специальном регенерационном аппарате, расположенном ниже абсорбера. Подача воздуха из холодильной камеры в абсорбер производится небольшим компрессором.
В абсорбере воздух промывается раствором триэтаноламина, освобождается от углекислого газа и возвращается обратно в камеру. Водный раствор триэтаноламина, обогащенный углекислым газом, стекает из абсорбера в регенератор и нагревается в нем до 95° С. Выделяющийся при нагревании углекислый газ выводится наружу, а теплый восстановленный раствор насосом через теплообменник-охладитель снова подается в абсорбер.
В Италии для поглощения углекислого газа применен диэтанол амин, отличающийся высокой поглотительной способностью даже при незначительной концентрации СO2 в воздухе и обеспечивающий почти полное удаление углекислого газа из воздушной смеси и, следовательно, быстрое повышение содержания азота в камере,
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
www.activestudy.info
Все об СО2 для аквариума

| Рано или поздно любой аквариумист сталкивается с вопросом о подаче СО2 в свой аквариум. В интернете можно найти много статей, форумов на эту тему, однако все они посвящены одному из вопросов касающихся СО2. Поэтому в данной статье мы решили собрать все воедино, доступно изложить материал, сделав при этом упор на те методы и способы подачи СО2 в аквариум, которые не требуют особых денежных вливаний и для которых необходимы лишь ваши умелые руки. |
Что такое СО2, зачем нужен СО2 для аквариума?
СО2 – это газ, который необходим аквариумным растениям. Растения на 50% состоят из углерода. В естественных условиях концентрация СО2 в воде составляет от 15-40 мг/л. А вот в аквариуме этот показатель стремиться к нулю, даже несмотря на то, что рыбки и другие обитатели аквариума вырабатывают его в процессе жизнедеятельности, однако в очень незначительных количествах. Сам механизм потребления СО2 растениями заключается в процессе фотосинтеза. Фотосинтез - процесс преобразования энергии света в энергию химических связей органических веществ на свету фотоавтотрофами при участии фотосинтетических пигментов (хлорофилл у растений, бактериохлорофилл и бактериородопсин у бактерий). В современной физиологии растений под фотосинтезом чаще понимается фотоавтотрофная функция - совокупность процессов поглощения, превращения и использования энергии квантов света в различных эндэргонических реакциях, в том числе превращения углекислого газа в органические вещества.
6СO2 + 6h3O = С6Н12O6 (глюкоза) + 6O2
В темноте происходит обратный процесс:
С6Н12O6 + 6O2 = 6CO2 + 6h3O
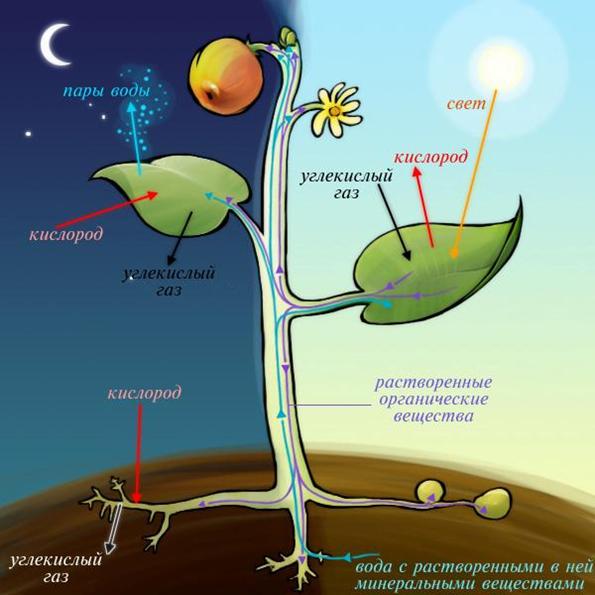
Из вышесказанного можно сделать выводы, что СО2: - Это основной строительный материал организма растений! Растения в аквариуме, при грамотной подаче СО2 становятся: красивыми и здоровыми, быстрорастущими. - В процессе фотосинтеза растения выделяют кислород О2! Этот процесс в народе называют пузырянием или перлингом растений. В свою очередь, выделяемый растениями кислород потребляется рыбками и другими гидробионтами, что нивелирует необходимость в механической аэрации аквариума в световой день. - кроме того, при подаче СО2 в аквариуме понижается уровень pH. Что нравиться фактически всем растениям и некоторым мягководным рыбкам.
Предостережения и опасности СО2 в аквариуме.
Если вы решили приобрести систему СО2 для аквариума, то должны понимать, что после ее установки придется более тщательнее следить за аквариумом: нужно будет контролировать уровень СО2 при помощи тестов или дропчекера, контролировать уровень pH, регулировать освещение, осуществлять грамотную подкормку растений макро и микро-удобрениями и т.д. Если этого не делать, то возникнут проблемы из-за неслаженной работы фотосинтеза: возможно удушение рыб, помутнение воды, водорослевая вспышка и прочие неприятности. Учтите, что даже самая безобидная самодельная система СО2 по типу бражка может навредить аквариуму. Поэтому все тщательно взвесьте и с умом подойти к вопросу установки СО2 для своего аквариума.
Выращивание аквариумные растения - это комплексное мероприятие.
Формула их успешного содержания заключается в балансе:+
+
+
При этом, выпадение хотя бы одного элемента приведенной формулы, влечет за собой плохое состояние растений. А также различные негативные последствия для аквариума в целом.
В отношении каждого элемента формулы даны ссылки, ниже кратко:
ОСВЕЩЕНИЕ. Какая бы ни была концентрация СО2 в аквариуме, без освещения углекислый газ в процесс фотосинтеза вступать не будет. Только баланс освещения и СО2 благоприятно влияют на растения.
УДОБРЕНИЯ. Растениям жизненно необходимы макро и микроэлементы. Макро-удобрения (NPK) - нитрат (NO3), фосфат (P/PO4), калий (K). Микро-удобрения - Fe, K, Mg, Mn, Cu, Zn, Mo, B, Co и др. ПАРАМЕТРЫ ВОДЫ. Большинство растений любят мягкую, слабокислую воду. Если говорить точнее, то в такой воде происходит наилучшее усвоение удобрений растениями. Для начинающих аквариумистов, вот еще базовый материал по растениям: АКВАРИУМНЫЕ РАСТЕНИЯ ДЛЯ НАЧИНАЮЩИХ. На этом считаем необходимым завершить изложение основ. Думаем, что вы сложили свое впечатление о необходимости СО2 в аквариуме.Способы подачи СО2 в аквариум.
Существуют три способа подачи углекислого газ в аквариум:- система брожения;
- баллоны со сжиженным газом;
- углеродосодержащие препараты.
Статья по этому поводу находиться - здесь. Кратко, баллонный способ – это самый оптимальный вариант. Изначально баллонная система СО2 дороговато обходится. Но зато потом окупает себя с лихвой, т.к. служат они долго, а перезаправка баллонов стоит копейки. Сахар, дрожжи, сода и т.д. стоят в разы дороже =) баллонная система со2 Углеродосодержащие препараты. К таким препаратам можно отнести, например, Tetra CO2 Plus - насыщает воду углеродом в форме, которая легко усваивается растениями.
баллонная система со2 Углеродосодержащие препараты. К таким препаратам можно отнести, например, Tetra CO2 Plus - насыщает воду углеродом в форме, которая легко усваивается растениями. 
СИСТЕМА БРОЖЕНИЯ. Вот мы и добрались до ее.
На наш взгляд – это самый интересный способ подачи углекислого газа для начинающего аквариумиста. Бражку можно сделать самому и посмотреть как она будет работать, вырастить на ней свой первый травник. А уж потом принимать решение о баллонах и акваскейпе =). У данного способа, есть два недостатка: - подходит для небольших аквариумов до 100 литров; - в бражке не возможно регулировать подачу газа и перекрыть ее на ночью; Однако, на захват объема аквариума в 200 литров можно поставить две бражки. А относительно второго пункта, можно вынимать на ночь распылитель СО2 и шланг из аквариума. Стоит отметить, что такой системой подачи СО2 сложно перенасытит аквариум углекислым газом. Она слабенькая. Кроме того, вы же всегда наблюдаете за аквариумом и в случае, чего-то сможете остановить процесс. Существует великое множество бражных агрегатов СО2, все они блещут новаторством и простотой. Еще больше существует рецептов, ингредиентов для системы брожения. Например, СО2 установка на лимонной кислоте. В данном материале, предлагаем вам пошаговую инструкцию бражной системы СО2 для аквариума, которую можно сделать своими руками. Такая установка не потребует от вас особых знаний и усилий, каких-то специфических деталей и обойдется в копейки. Отчасти именно поэтому, мы рекомендуем ее новичкам.ИТАК, ВОТ СПИСОК ТОГО, ЧТО ПОНАДОБИТЬСЯ.
 Литровая бутылочка из под сока с широким горлышком. Используется в качестве своеобразного фильтра, чтобы сопутствующая бражная бяка не попала в аквариум. Такой префильтр обязателен! Иначе погубите рыбу.
Литровая бутылочка из под сока с широким горлышком. Используется в качестве своеобразного фильтра, чтобы сопутствующая бражная бяка не попала в аквариум. Такой префильтр обязателен! Иначе погубите рыбу.
 Шприц пятикубовый. Используется в качестве пузырькового счетчика.
Шприц пятикубовый. Используется в качестве пузырькового счетчика.  Капельница. Продается в любой аптеке. Нужна в качестве шлангов для системы СО2.
Капельница. Продается в любой аптеке. Нужна в качестве шлангов для системы СО2. Силикон аквариумный или строительный. Нужен для герметизации агрегата.
Силикон аквариумный или строительный. Нужен для герметизации агрегата. Клапан обратного давления 1 шт., можно 2шт. Продается в любом отделе аквариумистики, предназначен для закупорки бражки, а также для того, чтобы вода из аквариума не полилась в систему или на пол.
Клапан обратного давления 1 шт., можно 2шт. Продается в любом отделе аквариумистики, предназначен для закупорки бражки, а также для того, чтобы вода из аквариума не полилась в систему или на пол.
 Трубка или шланг аквариумный.
Трубка или шланг аквариумный. Он чуть толще шлангов капельницы, может понадобиться.
Присоски. Чтобы прикрепить шлаг подачи СО2 в аквариуме. Итого, стоимость бражной системы СО2 выйдет примерно в 7-8 $.
Итого, стоимость бражной системы СО2 выйдет примерно в 7-8 $. ПОШАГОВАЯ СБОРКА СИСТЕМЫ СО2 ДЛЯ АКВАРИУМА.
Примечание: можно обойтись и без счетчика пузырьков. И подсоединить трубку капельницы напрямую в крышку 2х литровой бутылки, стык сильно засиликонить. Берем капельницу. Отсоединяем переходничок. Сразу же можно снять с капельницы регулятор подачи. Он не понадобится. Так как, если вы перекроете его бражка лопнет.
Берем капельницу. Отсоединяем переходничок. Сразу же можно снять с капельницы регулятор подачи. Он не понадобится. Так как, если вы перекроете его бражка лопнет. 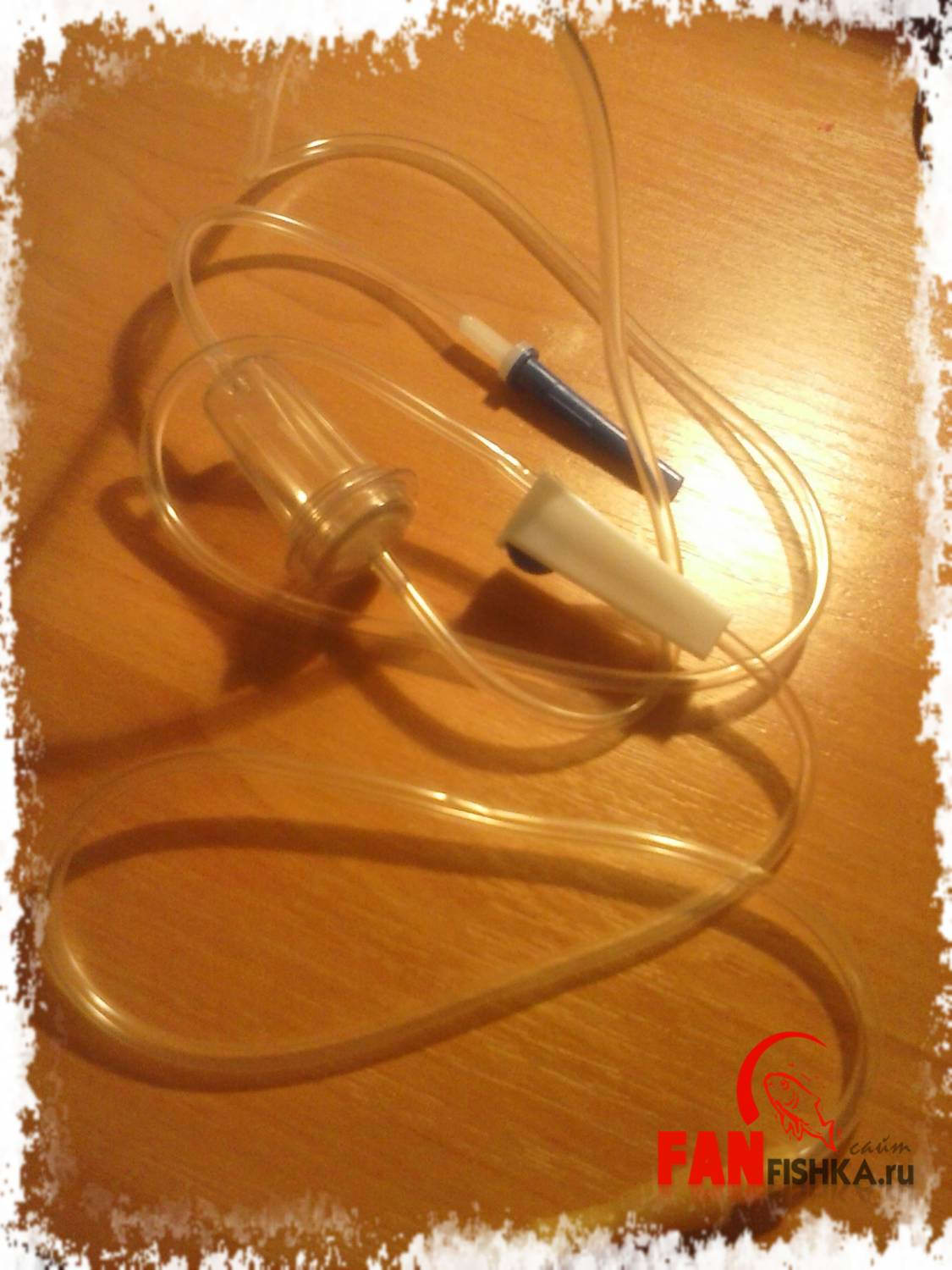



Реакция и СО2 пойдут примерно через 8-12 часов. Если до 24 часов газ не пойдет, значит что-то не так – либо травит система, либо реагентов мало, либо температура ниже 20-22 градусов. Проверьте герметичность установки, добавьте сахара и дрожжей, поставите бражку в теплое место (на батарею центрального отопления).
Теперь перед тем, как дать другие рецепты, кратко обсудим все ингредиенты для браги. Чтобы брага заработала нужен сахар, дрожжи и вода. Все остальное, это новаторство и доп.компоненты. САХАР. Можно использовать любой, но поговаривают, что тростниковый самый лучший. Чем больше будет сахара, тем больше будет чего есть дрожжевым грибкам. Тем сильнее будет проходить реакция. ДРОЖЖИ. Бывают хлебные (сухие и «мокрые»), можно использовать и те, и те! Разницы почти никакой. Рекомендуем сухие. Бывают также пивные и кормовые дрожжи. Для систем со2 рекомендуют пивные. ВОДА. Нужна чистая, чтобы дрожжевые грибки не боролись с другими конкурирующими культурами, хлоркой и другими примесями.Остальные элементы: Сода нужна для нейтрализации кислот. Делает бражку более щелочной, что продлевает ей жизнеспособность. Соду можно не использовать – это дополнительный элемент. Корм для рыбок и удобрения для растений. Участвуют в процессе брожения, стимулируя его и подкармливая дрожжевые грибки. Кусочки хлеба – так же улучшает процесс брожения. Их количество индивидуально. Можно также кидают в бражку изюм, урюк, кусочки фруктов и так далее.Другие рецепты СО2 для бражки.
Сахар - 40 столовых ложек; Крахмал - 16 столовых ложек; Сода - 13 столовых ложек; Воды – 2 литра; Все ингредиенты варятся в кастрюле до загустевшего состояния. После остужают и переливают в пяти литровую тару, добавляют 1 столовую ложку растворенных дрожжей на стакан воды. Работоспособность 3 месяца.Сахар -150 грамм; 1 чайная ложка дрожжей; 2 чайные ложки соды; 2 столовые ложки муки; 1,5 литра воды; 2 л. бутыль; Работоспособность 1-1,5 недели.
10 гр. лимонной кислоты; 10 гр. питьевой соды; Ингредиенты смешиваются в сухом состоянии, пересыпаются во влажную (без воды) браготару. Тару герметизируют. Работает 6-10 часов (на весь световой день).
На двухлитровую бутыль: Сахар 3 стакана; 30 грамм желатина; 1-н л. воды; 1 ст.л. питьевой соды; 1 ч.ложка дрожжей; Желатин замачивают на один час в 0,5л. воды. После добавляют еще 0,5 литра воды, добавляют сахар, соду. Подогревают на медленном огне до полного растворения. После остывания «желе» переливают в браготару, поверх (не размешивая) добавляют растворенные дрожжи. Работоспособность 2-4 недели.
5 ст. ложек сахара; 2 ст. ложки крахмала; 1 ст. ложка соды; ? литра воды; 1 ч.ложка дрожжей; Растворить в воде сахар, соду и крахмал. Поставить на водяную баню до загустения. Далее, залить поверх дрожжи, растворенные в стакане воды. Работоспособность 2-4 недели и более, если положить крахмал больше.Напоследок о распылителя СО2 для аквариума.
Двуокись углерода можно подавать в аквариум при помощи распылителя: каменного, веточки рябины, колокола, а также непосредственно присоединять трубку СО2 во внешний фильтр. Какой способ лучше, какой применить, выбор за вами. Отметим, что большинство стеклянных, фирменных диффузоров пробиваются бражкой. Тугие диффузоры, например, Флюваловские нет. Камешковый распылитель. Продается в любом зоомагазине. Недостаток – крупные пузырьки СО2, газ будет хуже растворяться. Веточка рябины. Дает мелкие пузырьки, но быстро забивается. Колокол. Покупной или самодельный. Некий колпачок-купол, задерживающий подаваемый СО2.СО2 лесенки - хороший вариант для бражки.
Диффузоры - стеклянные пробиваются. Советуем при покупке изучить отзывы. Распылитель СО2 устанавливает как можно ближе ко дну аквариума.
О результатах подачи СО2.
- после подачи СО2 и при должном освещении, аквариумные растения должны начать пузырять кислородом. Или как еще говорят - происходит перлинг растений. Наблюдается активный рост растений. - рыбки должны прекрасно себя чувствовать. В случае ухудшения самочувствия, СО2 отключают. Усиливают течение и аэрацию. Можно воспользоваться перекисью.- появление водорослей – признак избытка СО2. Необходимо уменьшить подачу углекислого газа. Или увеличить объем растений.- как убедиться в нормальной концентрации СО2. Сделать pH тест утром до включения света и второй вечером. Сравнить результаты и определиться все ли нормально. А лучше, приобрести дропчекер, о котором писали выше.Рекомендуем так же почитать:
fanfishka.ru
2Кон и 1н2со3, 1к2о и 1н2со3, 2кон и 1со2.
| Основание + Кислота = Соль и Вода |
1а) Основной гидроксид + кислотный гидроксид = …
2NaOH + h3SO4 = Na2SO4 + Н2О
1б)Амфотерный гидроксид + кислотный гидроксид = …
2Al(OH)3 + 3h3SO4 = Al2(SO4)3 + 6Н2О
1в) Основной гидроксид + амфотерный гидроксид = …
NaOH+Al(OH)3=NaAlО2+ 2Н2О
| Основной оксид + Кислота = Соль и Вода |
2а) Основной оксид + кислотный гидроксид = …
Na2О + h3SO4 = Na2SO4 + Н2О
2б) Амфотерный оксид + кислотный гидроксид = …
Al2О3 + 3h3SO4 = Al2(SO4)3 + 3Н2О
2в) Основной оксид + амфотерный гидроксид = …
Na2О + 2Al(OH)3= 2NaAlО2+ 3Н2О
| Основание + Кислотный оксид = Соль и Вода |
3а) Основной гидроксид + кислотный оксид = …
2NaOH + SO3 = Na2SO4 + Н2О
3б) Амфотерный гидроксид + кислотный оксид = …
Al(OH)3 + 3SO3 = Al2(SO4)3 + 3Н2О
3в) Основной гидроксид + амфотерный оксид = …
2NaOH+Al2О3= 2NaAlО2+ Н2О
Реакция 1в, если она протекает в растворе, сопровождается образованием других продуктов – комплексных солей, например,
NaOH(конц.)+ Al(OH)3 = Na[Al(OH)4]
Все средние соли в растворе – сильные электролиты (диссоциируют нацело).
Двойные соли. Двойные соли содержат два химически важных катиона; например СаMg(CO3)2, КАl(SO4)2,Fe(Nh5)2(SO4)2и др. Многие двойные соли образуются в виде кристаллогидратов при совместной кристаллизации соответствующих средних солей из насыщенного раствора:
К2SO4 + MgSO4 + 6h3O = К2Mg(SO4)2. 6h3O
Часто двойные соли менее растворимы в воде по сравнению с отдельными средними солями
IV Бинарные соединения.Бинарные соединения – это сложные вещест-ва, не относящиеся к классам оксидов, гидроксидов и солей и состоящие из катионов и бескислородных анионов (реальных или условных).
Их химические свойства разнообразны и рассматриваются в неорганической химии отдельно для неметаллов разных групп Периодической системы; в этом случае классификация прорводится по виду аниона.
П р и м е р ы :
а)галогениды: OF2, HF, KBr, PbI2, Nh5Cl, BrF3, IF7
б)хальгогениды: h3S, Na2S, ZnS, As2S3, Nh5HS, K2Se, NiSe
в)нитриды: Nh4, Li3N, Mg3N, AlN, Si3N4
г)карбиды: Be2C, Al4C3, Na2C2, CaC2, Fe3C, SiC
д)силициды: Li4Si, Mg2Si, ThSi2
е)гидриды: LiH, Cah3, Alh4, Sih5
ж)пероксидыН2О2,Na2О2, СаО2
з)надпероксиды: НО2, КО2, Ва(О2)2
По типу химической связи среди этих бинарных соединений различают:
ковалентные: OF2, IF7, h3S, Р2S5, Nh4, Н2О2
ионные:K2Se,Mg3N,Na2О2, СаО2,CaC2
Встречаются двойные (с двумя разными катионами) и смешанные (с двумя разными анионами).
По аналогии со взаимосвязью гидроксидов и солей из всех бинарных соединений выделяют бескислородные кислоты и соли (остальные соединения классифицируют как прочие).
Бескислородные кислоты. Содержат (как и оксокислоты) подвижный водород Н+и поэтому проявляют некоторые химические свойства кислотных гидроксидов (диссоциация в воде, участие в реакциях солеобразования в роли кислоты). Распространённые бескислородные кислоты – этоHI,HBr,HCl,HF,HCN,h3S, из нихHF,HCN,h3S– слабые кислоты, остальные – сильные.
Пример реакции солеобразования:
2h3S+ Ва(ОН)2= Ва(HS)2+ 2НО2
Металлы и амфигены, стоящие в ряду напряжений левее водорода, и не реагирующие с водой, вступают во взаимодействие с сильными кислотами HI,HBr,HClв разбавленном растворе и вытесняют из них водород , например, Ве + 2HCl= ВеCl2+ Н2
2 Al + 6HI = 2AlI3 + h3
Бескислородные соли. Образованы катионами металлов и амфигенов (а также катионом аммонияNh5+) и анионами (остатками) бескислородных кислот, например,AgCl,NaF,KBr,PbI2и др. Проявляют некоторые химические свойства оксосолей.
Общий способ получения бескислородных солей с одноэлементными анионами – взаимодействие металлов и амфигенов с неметаллами F2,Cl2,Br2иI2(в общем виде Г2) иS(приведены реально протекающие реакции):
2Me + Г2 = 2MeГ (Me = Li, K, Rb, Cs, Ag)
Me + Г2 = MeГ2 (Me = Be, Mg, Ca, Sr, Ba, Zn, Mn, Co)
2Me + 3Г2 = 2MeГ3 (Me = Al, Ga, Cr)
2Me + S = Me2S (Me = Li, K, Rb, Cs, Ag)
Me + S= MeS (Me = Be, Mg, Ca, Sr, Ba, Zn, Mn, Co, Fe,Ni)
2Me + 3S = Me2S3 (Me = Al, Ga, Cr)
studfiles.net
Характерные химические свойства неорганических веществ
Характерные химические свойства неорганических веществ:
простых веществ-металлов: щелочных, щелочноземельных, алюминия, переходных металлов - меди, цинка, хрома, железа:
простых веществ-неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния; оксидов: основных, амфотерных, кислотных; основании н амфотерных гидроксидов: кислот;
солей: средних, кислых, основных; комплексных (на примере соединений алюминия н цинка).
1. Установите соответствие между реагирующими веществами и продуктами их взаимодействия.
| НАЗВАНИЕ ВЕЩЕСТВА | ПРОДУКТЫ |
| A) KOH + S03 | 1) KHS04 |
| Б) КОН + S02 | 2) K2S03 |
| В) кон + со2 (изб.) - | 3) K2C03 и н2о |
| Г) кон + со2(недост.) | 4) K2S04 |
|
| 5) КНС03 |
|
| 6) KHS03 |
2. Установите соответствие между реагирующими веществами и продуктами их взаимодействия.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОДУКТЫ ВЗАИМОДЕЙСТВИЯ |
| А) СО2 + Н20 | 1) СаСО3 |
| Б) СО2 + СаО | 2) СаС03 + Н20 |
| В) СО2 + Са(ОН)2 | 3) Са(НСО3)2 |
| Г) СО2(из6ыток) + Са(ОН)2 | 4) Са(НС03)2+ Н20 |
|
| 5) СО + Н2 |
|
| 6) н2со3 |
3. Установите соответствие между реагирующими веществами и продуктами их взаимодействия.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОДУКТЫ ВЗАИМОДЕЙСТВИЯ |
| А) Са(ОН)2 + h3SO4
Б) Са(ОН)2 + h3SO3 | 1) СаО + Н2
2) СаО + Н2О |
| В) Са(ОН)2 + SO2 | 3) CaS + Н2О |
| Г) Са(ОН)2 + SO3 | 4) CaSO3 + Н2 |
|
| 5) CaSO3 + Н2O |
|
| 6) CaSO4 + Н2O |
4. Установите соответствие между реагирующими веществами и продуктами реакции.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОДУКТЫ РЕАКЦИИ |
| A) Si + Mg | 1) Sih5 |
| Б) Si + NaOH(водн.) | 2) h3SiO3 |
| В) Ca2Si + Н2О | 3) Na2SiO3 |
| Г) SiО2 + Mg | 4) Mg2Si |
|
| 5) CaSiO3 |
|
| 6) Si |
5. Установите соответствие между реагирующими веществами и продуктами реакции, содержащими азот.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА A) N2 + 02 | ПРОДУКТЫ РЕАКЦИИ 1) N2 |
| B)Nh5N02(Kp) | 2) N20 |
| B)Nh5NO3(Kp) | 3) N0 |
| Г) HNO3(KOHц) + Р(красный) | 4) N02 |
|
| 5) N203 |
6. Установите соответствие между веществами, вступающими в реакцию и продуктами их взаимодействия.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОДУКТЫ РЕАКЦИИ |
| А) КНСО3 + КОН | 1) KN03 + со2 + н2о |
| Б) КНСО3 + НС1 | 2) КСl + Na2C03 |
| В) К2СО3 + HNO3 | 3) к2со3 + Н20 |
| Г) K2C03 + ВаС12 | 4) KC1 + Н20 + С02 |
|
| 5) ВаС03+КС1 |
7. Установите соответствие между реагирующими веществами и продуктами их взаимодействия.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОДУКТЫ ВЗАИМОДЕЙСТВИЯ |
| A) AI2O3 + NaOH сплавление | 1) NaA1О2 |
| Б) А1203 + NaOH + Н20 | 2) NaA1O2 + Н2O |
| В) Аl2О3 + Na2CO3 сплавление | 3) NaA1O2 + СO2 |
| Г) А1203 + HC1 | 4) Na[AI(OH)4l |
|
| 5) AIC13 + Н2O |
|
| 6) А1С13 + Н2 |
8. Установите соответствие между реагирующими веществами и продуктами их взаимодействия.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОЛУК1Ы ВЗАИМОДЕЙСТВИЯ |
| А) Р203 + Н2O | 1) Н3РO3 |
| Б) P2Os + Н2O | 2) НРО2 |
| В) P2Os + MgO | 3) Н3РO4 |
| Г) Р2O5 + Mg(OH)2 | 4) Mg3(PO4)2 |
|
| 5) Mg3(PO4)2 + Н2 |
|
| 6) Mg3(PO4)2 + Н2O |
9. Установите соответствие между реагирующими веществами и продуктами их взаимодействия.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОДУКТЫ ВЗАИМОДЕЙСТВИЯ |
| A) SO2 + Н2O | 1) CaSO3 + Н2 |
| Б) SO3+ Н2O | 2) CaSO3 + Н2O |
| В) SO2 + Са(ОН)2 | 3) CaSO4 |
maratakm.narod.ru
получение, применение и химические свойства :: SYL.ru
Карбонат калия также известен как пищевая добавка Е501. Это мелкий кристаллический порошок, образующийся в результате химической реакции диоксида углерода и гидроксида калия. Вещество это достаточно давно известно. В старину его называли «поташ».
Историческая справка
Углекислый калий с давних времен назывался поташ. Слово это имеет латинское происхождение. Дословно его можно перевести так: потт - горшок, аш - зола. Вот такой получается интересный перевод – горшок золы. Почему такое странное название? Это связано со старинным способом его получения.
Большую популярность поташ приобрел в 17-19 веках. Он выступал как основной химический реагент. Его использовали практически во всех отраслях промышленности тех лет. В Российской империи небезызвестный своими новаторскими идеями Петр Первый ввел монополию на производство поташа в 1721 году. Сегодня же карбонат калия относится к 3-му классу опасных веществ. Его производят во многих странах.
Применения поташа в истории
Итак, история исследования и использования такого вещества, как поташ, насчитывает не один век. Интересно, что он был известен еще древним римлянам. Они по достоинству оценили свойства данного вещества и использовали его для стирки. Именно они впервые подметили, что зола способна удалить даже сильные жирные пятна с вещей. Только спустя несколько веков этому нашли научное подтверждение. Оказывается, что поташ, попадая в воду, создает щелочную среду. Жирные вещества в ней просто напросто расщепляются.
Примечательно, что в больших объемах научились добывать карбонат калия уже в начале семнадцатого века. Такое производство по праву можно было назвать промышленным. Процесс его получения был трудоемок. Сначала строились большие каменные очаги. В них раздували сильный костер, поддерживая его дровами. Затем в специальном деревянном корыте смешивали сильно горячую воду и приготовленную древесную золу. Получался раствор, которым, как ни странно это звучит, поливали костер, следя, чтобы он не потух. Конечно, здесь требовалось мастерство и умение. Появились даже специальные люди обученные ремеслу, которых называли «поливала». Но как же получали сам поташ? Под костром, который долгое время периодически поливали раствором золы, появлялся слой карбоната калия. И чем больше по времени протекал этот процесс, тем наслоение было толще. Теперь только оставалось дождаться, пока он остынет. Потом его долбили и закатывали по небольшим бочкам. Но экономичным этот процесс нельзя было назвать. Чтобы получить один килограмм поташа уходил кубометр древесины.
Современные способы получения
Легче всего карбонат калия получить из щелочи в процессе выщелачивания водой золы из водорослей и злаков. Поташа больше всего содержится в растворимой составляющей растительных остатков. Еще сравнительно недавно принцип получения этого вещества был такой. В глиняный сосуд с маленьким отверстием на дне помещали золу. Затем ее утрамбовывали. Заливали строго отмеренным количеством горячей воды. Она должна была пройти через весь слой золы и стечь в емкость. Потом ее снова заливали в сосуд, так до тех пор, пока жидкость не приобретала густую консистенцию. Затем лишнюю воду выпаривали и после остывания получали поташ. Весь процесс был куда более экономичным, чем предыдущий. Требовалось уже не так много золы.
Сегодня это вещество получают в результате электролиза KCl. Это цепь сложных химических реакций. В итоге осуществляется гидролиз карбоната калия. Во взаимодействие вступают гидроксид К и углекислый газ. Формула реакции выглядит следующим образом: 2(КОН) + СО2 → К2СО3 + Н2О
Общие свойства карбоната калия
Это химическое вещество обладает следующими свойствами:
- Оно мгновенно растворяется в воде.
- Данное вещество не расщепляется в этаноле.
- Температура плавления кристаллического карбоната калия составляет 891 градус по Цельсию.
- Вещество обладает выраженным вкусом щелочи.
- Углекислый калий не имеет запаха.
Важно знать, в кристаллическом состоянии карбонат калия оказывает кератолитическое и выраженное противомикробное действие. Его бактерицидные свойства можно объяснить тем, что сухое вещество и его раствор – это сильная щелочь. При этом чем выше его температура, тем сильнее проявляются эти свойства. Поташ издревле использовался как средство, убивающее микробов и микроскопических вредителей.
Применение
Благодаря своим щелочным свойствам углекислый калий способен регулировать уровень кислотности. Также ему под силу бороться с избытком влаги, перемешивать масляные и водные растворы в однородную массу. Он может применяться в качестве разрыхлителя теста в выпечке. Данное вещество используют в производстве алкогольных напитков. Здесь его применяют как стабилизатор. Естественно, что карбонат калия - вещество опасное, поэтому в пищевой промышленности он используется в малых количествах.
В сельском хозяйстве уже достаточно долгое время поташ известен как удобрение. Он препятствует размножению на культурных растениях насекомых и прочих вредителей. Раствор углекислого калия способен значительно улучшить качество пашни. Его свойства способствуют тому, что из почвы выводится излишняя кислотность. Раствором этого вещества дезинфицируют помещения. Особенно там, где долгое время содержится скот. Это курятники, конюшни, свинарники.
Нашел свое применение карбонат калия и в фармацевтике. Это активное вещество противопаразитарных мазей и суспензий. Они эффективно борются с такими паразитами, как вши и чесоточные клещи.
Пищевая добавка Е501
Пищевая добавка Е501 – это мелкозернистый порошок. Его используют как компонент кулинарных изделий и алкогольных напитков. Он является примесью питьевой соды. В настоящее время она признана во многих странах опасной. В старину карбонат калия добавляли в малых количествах в пряники.
Помимо своего основного названия, эта пищевая добавка скрывается и под другими не менее известными наименованиями. Это и дикалий карбонат, и поташ, и калий углекислый. Но в действительности это одно и то же вещество. Оно небезопасно для здоровья человека и может спровоцировать сильные раздражения.
Вред
В результате исследований доказано, что карбонат калия (формула К2СО3) наносит вред организму человека. Но справедливости ради нужно отметить, что опасен он только во взвешенном состоянии. Если он попадает в верхние дыхательные пути, то непременно вызовет сильнейшее раздражение и аллергическую реакцию. Могут также проявиться астматические приступы у больных с хронической формой.
Это вещество также вызывает местное раздражение и зуд, если попадает на влажные кожные покровы и слизистую рта и глаз. Проявляется и в форме экземы. Если порошок попадает на руки или лицо, его необходимо немедленно смыть водой.
Первая помощь при вдыхании и попадании на кожу карбоната калия
Данное вещество не угрожает жизненно важным процессам в организме. Но между тем оно может спровоцировать массу негативных симптомов. При вдыхании наблюдается раздражение и отек. Поэтому необходимо незамедлительно вызвать скорую помощь. Затем вынести пострадавшего на свежий воздух.
Если вещество попало на слизистые или кожу, то его нужно сразу же смыть. Промывают холодной проточной водой в течение 15 минут. Если вещество попало по каким-то причинам в желудок, то делают промывание.
www.syl.ru